
Читайте также:
|
1 В процессе изучения окисления железа на воздухе при 580 К были получены результаты, представленные в таблице. Найти уравнение, описывающее закон роста оксидной пленки и сделать вывод о механизме процесса окисления.
Время 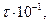 С С
| 6,72 | 15,06 | 18,96 | 37,72 | 133,8 | |
Толщина пленки 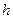 ,мкм ,мкм
| 54,2 | 59,6 | 62,1 | 65,8 | 76,0 |
2 Сульфидная коррозия, имеющая место при испытании образцов кобальта в атмосфере сероводорода 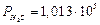 Па при 993 К, описывается уравнением квадратичной параболы с константой скорости
Па при 993 К, описывается уравнением квадратичной параболы с константой скорости 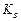 = 6,67
= 6,67  10-6 г
10-6 г 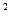 /(cм4
/(cм4  c). Процесс окисления образцов кобальта в кислороде (
c). Процесс окисления образцов кобальта в кислороде (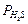 = 1,013
= 1,013  105 Па) при 1223 К протекает по аналогичному закону с константой скорости
105 Па) при 1223 К протекает по аналогичному закону с константой скорости 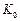 = 1,6
= 1,6  10
10 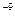 г2/(см4
г2/(см4  с). Определить время, за которое при указанных температурных режимах удельный прирост массы образца после окисления кислородом окажется равным приросту масcы за счет образования сульфида после выдержки в сероводороде в течение 0,5 ч.
с). Определить время, за которое при указанных температурных режимах удельный прирост массы образца после окисления кислородом окажется равным приросту масcы за счет образования сульфида после выдержки в сероводороде в течение 0,5 ч.
3 При окислении железа и сплавов на его основе на поверхности образуется несколько оксидных слоев различного состава: FeO, Fe2O3 и Fe3O4. По экспериментальным данным, приведенным в таблице зависимости изменения общей толщины окалины и толщины слоя FeO от времени окисления образцов армко-железа на воздухе при 1123 К (металлографические исследования), установить закон роста окалины и отдельно оксида FeO, сделать вывод о механизмах окисления, определить отношение толщины слоя FeO к суммарной толщине оксидов Fe2O3 и Fe3O4 после 100 ч выдержки образца при указанной температуре.
Время 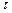 , час , час
| 1,25 | 2,50 | 5.0 | 10,0 | 18,0 | |
| Толщина слоя окалины h, мкм | ||||||
Толщина слоя 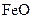 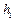 , мкм , мкм
|
4 Исследования по окислению вольфрама в атмосфере кислорода в интервале температур 973-1273 К при различной продолжительности показали, что процесс протекает сначала по параболическому закону, а затем постепенно переходит к линейному. Объясните наблюдаемое явление. Ответ подтвердите результатами проверки выполнения условия сплошности образующимися оксидами WO и WO3. Плотности оксидов соответственно равны 11,4 и 6,47 (г/смэ). Масса грамм-атома вольфрама составляет 183,85 г, плотность вольфрама 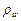 = 19,3 г/см3.
= 19,3 г/см3.
5 На основании экспериментальных данных по изучению окисления cтали У6 (0,6% С) при 1073 К в сухом воздухе и воздухе, насыщенном водяным паром, установить различие в кинетике газовой коррозии стали в выбранных средах и дать возможное объяснение наблюдаемых различий.
Удельное увеличение массы в в-хе  , г/м2 , г/м2
| Время, час | |||
| 2,5 | ||||
| сухом | - | |||
| насыщенном водяными парами | - |
6 Установить закон роста толщины оксидной пленки на армко-железе в воздухе при 423 К, используя результаты, представленные в таблице. Пояснить, каким процессом контролируется скорость окисления металла в данном случае, и определить толщину оксидной пленки после 50 ч окисления.
| Толщина пленки h, нм | 3,4 | 4,8 | 5,7 | 6,0 | 6,5 | 7,0 | 7,45 |
Время 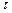 , час , час
| 0,5 | 1,0 | 2,0 | 3,0 | 4,0 | 5,0 | 6,0 |
7 При окислении кобальта в чистом кислороде (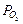 = 1,013
= 1,013  105 Па) при температурах выше 1173 К образуется окалина, состоящая только из слоя оксида кобальта СоO. Найдите уравнение, описывающее закон роста СоO при 1293 К, используя результаты измерений количества поглощенного металлом кислорода в зависимости от времени выдержки образца при данной температуре.
105 Па) при температурах выше 1173 К образуется окалина, состоящая только из слоя оксида кобальта СоO. Найдите уравнение, описывающее закон роста СоO при 1293 К, используя результаты измерений количества поглощенного металлом кислорода в зависимости от времени выдержки образца при данной температуре.
| Количество поглощенного кислорода Q, г/см2 | 0,0120 | 0,0208 | 0,0343 | 0,0452 | 0,0588 | |
Время 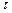 , час , час
| 1,0 | 2,0 | 4,0 | 6,0 | 9,0 |
8 При изучении взаимодействия тантала с кислородом при давлении газа 7,7∙103 Па было показано, что процесс окисления в интервале температур 523–723 К подчиняется параболическому закону. Определить уравнение температурной зависимости скорости параболического окисления тантала, используя данные, приведенные в таблице.
| Параболическая константа скорости К, г2/(см4 ч) | 6,6∙10-16 | 5,7∙10-15 | 3,37∙10-14 | 2,17∙10-13 | 1,21∙10-12 |
| Температура Т, К |
9 Определить удельный прирост массы образца Ni–Cr (20%) сплава при выдержке его в течении 100ч в атмосфере кислорода при 1473 К, если значения констант параболического окисления при 1273 К и 1073 К составляют соответственно 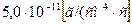 и
и 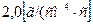 . Энергия активации процесса окисления данного сплава в заданном температурном интервале постоянна в течении всего времени окисления.
. Энергия активации процесса окисления данного сплава в заданном температурном интервале постоянна в течении всего времени окисления.
10 Стойкость молибдена против окисления определяется поведением образующейся пленки MoO3, температура плавления которой 1068 К, но при Т>773 К имеет место значительное испарение оксида.
Рассчитать удельное изменение массы образца (мг/см2) подвергнутого испытанию на воздухе при 977 К в течении 4 часов, если известно, что увеличение массы молибдена, которое должно было бы происходить за счет окисления, отвечает линейному закону с КЛ = 2,78 10-3 мг/(см2 с), а температурная зависимость линейной скорости испарения (возгонки) оксида MoO3 в интервале температур 923 – 1073 К отвечает уравнению 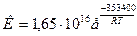
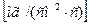 .
.
11 Определить удельный прирост массы образца Ni–Cr сплава при выдержке в течении 100 часов в атмосфере кислорода при температуре 1473 К, если температурная зависимость параболической константы скорости окисления данного сплава отвечает уравнению Аррениуса с параметрами Q = =182,749 кДж/моль, А = 5,7 108 [г2/(м4 ч) ].
Дата добавления: 2015-07-11; просмотров: 164 | Нарушение авторских прав