
Читайте также:
|
Пример 1. Определить возможно ли окисление палладия в воздухе (Ро2 =0,21 атм) и кислороде при 1123 К, если упругость (давление) диссоциации его оксида при этой температуре (Ро2)р = 0,667 105 Па (0,658 атм), R= 8,31 Дж/(моль К)
Решение.
Реакция окисления палладия может быть записана в виде
Pd+1/2O2 <=> PdO
Так как в воздухе Ро2 = 0,213∙105 Па (0,21 атм), и (Ро2)р > Ро2, то процесс окисления невозможен.
К тому же результату приводит и расчет изменения энергии Гиббса для реакции
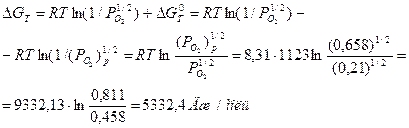 В кислороде этот процесс возможен, т.к. (Ро2)р < Ро2 = 1,013∙105 Па (1 атм). Расчет энергии Гиббса приводит к подобному результату.
В кислороде этот процесс возможен, т.к. (Ро2)р < Ро2 = 1,013∙105 Па (1 атм). Расчет энергии Гиббса приводит к подобному результату.
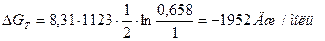
Пример 2. Определить температуру, при которой возможна диссоциация оксида серебра на воздухе ((РО 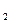 =
= 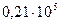 Па) и в чистом кислороде (РО
Па) и в чистом кислороде (РО 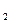 =
= 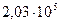 Па). Температурная зависимость стандартного изменения энергии Гиббса реакции 2Ag + ½O2 ↔Ag2O задана уравнением
Па). Температурная зависимость стандартного изменения энергии Гиббса реакции 2Ag + ½O2 ↔Ag2O задана уравнением 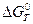 = –28226 + 60,72 Т (Дж/моль).
= –28226 + 60,72 Т (Дж/моль).
Решение.
Для определения температуры необходимо использовать уравнение изотермы Вант-Гоффа для равновесных условий: 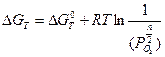 = 0. Тогда, подставляя в это уравнение вместо
= 0. Тогда, подставляя в это уравнение вместо 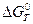 выражение для температурной зависимости (см. условие задачи), получим 28226 –60,72 Т =
выражение для температурной зависимости (см. условие задачи), получим 28226 –60,72 Т = 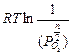 или 28226 = Т (60,72+
или 28226 = Т (60,72+ 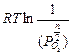 ) = Т (60,72 –
) = Т (60,72 – 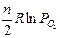 ). Отсюда
). Отсюда  Подставляя значение R = 8,31 Дж/моль; n =1; РО
Подставляя значение R = 8,31 Дж/моль; n =1; РО 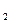 =
= 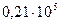 Па = 0,21 атм (воздух) и РО
Па = 0,21 атм (воздух) и РО 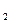 =
= 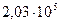 Па = 2 атм (кислород) получаем значения температур диссоциации серебра в воздухе и кислороде.
Па = 2 атм (кислород) получаем значения температур диссоциации серебра в воздухе и кислороде.
Температура диссоциации оксида серебра на воздухе
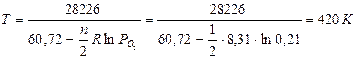
в кислороде
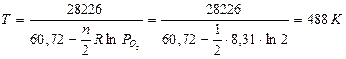
Дата добавления: 2015-07-11; просмотров: 234 | Нарушение авторских прав