
Читайте также:
|
Закон эквивалентов для данной реакции:
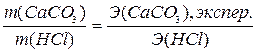 Э(CaCO3),экспер. -?
Э(CaCO3),экспер. -?
m(CaCO3) - навеска (г), дана; Э(HCl) = 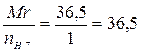
МЭ(HCl) = 36,5 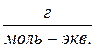
1 л 1н. раствора кислоты содержит 1 моль-экв. HCl, масса которого
m = nэ × Мэ = 1 моль-экв. × 36,5 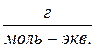 =36,5 г
=36,5 г
Масса кислоты вступившей в реакцию с CaCO3 будет равна:
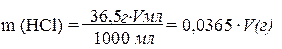
Подставив числовые значения m(CaCO3), m(HCl), Э(HCl) в выражение закона эквивалентов, рассчитайте величину Э(CaCO3),экспер. Сопоставьте значение Э(CaCO3), экспер. с теоретическим значением, определите абсолютную и относительную ошибки эксперимента.
Абсолютная ошибка D = | Ээксп. – Этеор.|
Относительная ошибка = 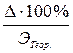
При качественном выполнении эксперимента относительная ошибка не превышает 0,5 – 1%.
Дата добавления: 2015-07-12; просмотров: 151 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Эквивалент ВЕЩЕСТВ | | | Упражнения и задачи |