
|
Читайте также: |
Полимером называется органическое вещество, имеющее длинные молекулы, построенные из одинаковых многократно повторяющихся звеньев – мономеров. Классификация полимеров по различным признакам представлена на рис. 1.6.
По происхождению полимеры делятся на три группы (рис. 1.6.).
Природные образуются в результате жизнедеятельности растений и животных и содержатся в древесине, шерсти, коже: протеин, целлюлоза, крахмал, латекс. Обычно природные полимеры подвергаются операциям выделения, очистки, при которых структура основных цепей остаётся неизменной. Продуктом такой переработки являются искусственные полимеры: натуральный каучук, целлулоид и др. Синтетические полимеры получают синтезом из низкомолекулярных веществ и не имеют аналогов в природе.
По химической структуре полимеры делятся на линейные и пространственные (рис.1.6.). Сравнительный анализ этих двух групп полимеров дан в таблице 1.4.
Полимеры могут быть получены с помощью реакций полимеризации (рис. 1.7,а) либо поликонденсации (рис. 1.7,б).

а)

б)
Рис. 1.7. Реакции образования полимеров: а – полимеризации, б – поликонденсации

Рис. 1.6. Различные методы классификации полимеров
Таблица 1.4 − Сравнительный анализ линейных и пространственных полимеров.
| Линейные полимеры | Пространственные полимеры | |
| Макромолекулы Свойства При нагревании проявляют | цепочечные последовательности повторяющихся звеньев между цепочками, действуют силы Ван-дер-Ваальса. гибкость, эластичность, легко размягчаются и расплавляются, растворяются в растворителях термопластичность – при нагревании размягчаются, при охлаждении затвердевают без химических изменений | Связаны в общую пространственную сетку большая жесткость, высокая температура плавления, значительная часть не растворяется термореактивность – при нагревании необратимо изменяют свойства |
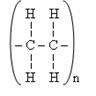
Реакция полимеризации протекает по схеме nM = M, где M – молекула мономера; n – степень полимеризации. При цепной полимеризации молекулярная масса нарастает почти мгновенно, реакция чувствительна к присутствию примесей и требует, как правило, высоких давлений. Такой процесс в естественных условиях невозможен, и все природные полимеры образованы иным путём. Реакция полимеризации проводится в сложной аппаратуре специализированных производств. С помощью полимеризации получают, например, полиэтилен, поливинилхлорид, полиметилметакрила (органическое стекло) и т.д.
Полимеры могут образовываться более простым путём – постепенно от мономера к димеру, затем к триммеру, тетрамеру и т.д. Такое объединение мономеров, их “конденсацию”, называют реакцией поликонденсации, она не требует высоких давлений, но сопровождается изменением химического состава, а часто и выделением побочных продуктов. Эта реакция реализуется в природе, она может быть легко осуществлена за счёт небольшого нагрева в самых простых условиях.
Поликонденсационные полимеры обладают, как правило, пониженными электрическими свойствами по сравнению с материалами, полученными по реакции полимеризации. Основной причиной этого является наличие в поликонденсационных диэлектриках остатков побочных низкомолекулярных веществ (воды, кислот, спирта), которые, распадаясь на ионы, увеличивают проводимость материала. Кроме того, молекулы конденсационных полимеров содержат полярные группы, что повышает их угол диэлектрических потерь и гигроскопичность.
Путём поликонденсации получают, например, фенолформальдегидные и полиэфирные смолы.
1.6.1. Природные полимеры
К числу природных полимеров, имеющих значение в РЭА, относятся канифоль, шеллак и янтарь. При нагревании они размягчаются и плавятся, в воде нерастворимы, а в спирте, эфире и других органических растворителях растворимы.
Основные характеристики и области применения полимеров, встречающихся в природе, приведены в таблице 1.5.
Таблица 1.5 − Основные свойства и области применения природных полимеров.
| Название | Происхождение | Тип диэлектрика | Область применения |
| Канифоль Шеллак Янтарь | Хрупкая смола, получаемая из смолы хвойных деревьев Продукт жизнедеятельности тропических насекомых Ископаемая смола растений | Слабополярный Слабополярный Слабополярный с высоким ρ | Для изготовления лаков и компаундов, а также как составная часть электроизоляционных смол В виде спиртового раствора для изготовления клеящих лаков, для слюдяной изоляции, а также для лакирования деталей В электроизмерительных приборах, требующих высокое значение сопротивления изоляции (ограничена из-за дороговизны) |
1.6.2. Линейные полимеры
Химическая структура и основные параметры некоторых важнейших линейных полимеров, применяемых в РЭА, представлены в таблице 1.6., а основные достоинства и недостатки, области применения этих материалов приведены в таблице 1.7.
Как следует из таблицы 1.6., полиэтилен и фторопласт-4 относятся к неполярным диэлектрикам, полистирол – к слабополярным, а поливинилхлорид и фторопласт-3 – это полярные диэлектрики.
Таблица 1.6 -Структура и основные параметры линейных полимеров.
| Материал | Полиэтилен | Полистирол | Фторопласт-4 | Поливинил -хлорид | Фторопласт-3 |
| Структура |
|

|

|

|

|
| Параметры: ρv, Ом·м ρδ, Ом εr (1 МГц) tg δ (1МГц) Епр, МВ/м Нагревостойкость,°С | 1013-1015 1015 2,3-2,4 (1-5)·10-4 15-20 80-90 | 1014-1015 – 2,4-2,6 (1-5)·10-4 20-35 70-80 | 1015-1016 1017 1,9-2,1 (1-3)·10-4 20-30 | 1013-1014 1012-1014 3,0-5,0 (3-8)·10-2 15-20 60-70 | 1014-1015 1016-1017 2,3-2,8 (1-2)·10-2 23-25 |
Таблица 1.7 - Особенности и области применения линейных полимеров.
| Материал | Достоинства | Недостатки | Области применения |
| Полиэтилен | Химическая инертность, водостойкость, легко обрабатывается | Низкая нагревостойкость, старение под действием света | “Король пластмасс”: широко используется для изоляции. Изоляция высокочастотных кабелей, изоляционные плёнки. |
| Полистирол | С различными добавками приобретает ударопрочность, атмосферостойкость, пенистость | Хрупкость, малая устойчивость к действию органических растворителей | Полистироловая плёнка – для производства конденсаторов. Вспененный полистирол – для теплоизоляции и герметизации изделий. |
| Фторопласт-4 | Негорючесть, химическая и радиационная стойкость, негигроскопичность, несмачиваемость водой и другими жидкостями, не изменяет электрическую длину в широком диапазоне температур и частот. | Адгезионно инертен: трудно поддаётся склеиванию. Обладает холодной текучестью и работает плохо под нагрузкой. Дорог из-за обработки на прецизионных станках. | Сплошная или плёночная изоляция, изоляция проводов на атомных станциях, проводов используемых в качестве нагревателей в растворах кислот и щелочей. Диэлектрические части СВЧ волноводов, разъёмов. Подложки тонкоплёночных ГИС СВЧ. Использование в РЭА с фазово-импульсной модуляцией и измерительных фазочувствительных системах. |
| Поливинилхлорид | Хорошие механические свойства, высокая химическая стойкость. | Большие потери на высоких частотах. | Изоляция монтажных проводов, кабелей. Использование как конструкционного материала. |
| Фторопласт-3 | Химическая стойкость | Большие потери. | Для изоляции проводов, плёнки для конденсаторов. |
1.6.3. Полимеры, получаемые поликонденсацией
В зависимости от особенностей проведения реакции поликонденсации могут быть получены полимеры, как с линейной, так и с пространственной структурой. Так как при поликонденсации выделяются побочные продукты (см. 1.6), которые не всегда могут быть удалены из полимера, диэлектрические характеристики поликонденсационных полимеров несколько ниже, чем у получаемых с помощью реакции полимеризации. Основными поликонденсационными полимерами являются фенолформальдегидные смолы (ФФС), эпоксидные и кремнийорганические смолы (рис. 1.8).

Рис. 1.8. Виды полимеров, получаемых реакцией поликонденсации.
Фенолформальдегидные смолы – продукты полимеризации фенола H5C6OH с формальдегидом H2CO. При проведении реакции с избытком фенола в кислотной среде можно получить термопластичные смолы, называемые новолаком, а с избытком формальдегида в щелочной среде - термореактивные смолы, называемые бакелитом. Эти материалы являются сильно полярными диэлектриками из-за наличия гидроксильной группы OH. Новолак используется для производства лаков и пластмасс, а бакелит – для пропитки различных материалов.
Эпоксидные смолы – продукт поликонденсации многоатомных соединений, включающих эпоксигруппу кольца

В исходном состоянии эпоксидные смолы представляют собой вязкие жидкости, переходящие под действием особых веществ – отвердителей – в твердое состояние. В результате они становятся термореактивными материалами. В процессе отверждения, происходящем без выделения побочных продуктов, эпоксидные смолы приобретают пространственное строение. Выбор отвердителя сильно влияет на такие свойства смол, как эластичность, нагревостойкость и др. При изготовлении изделий важно избегать как недоотверждения, которое проявляется в повышенных диэлектрических потерях и недостаточной жесткости, так и переотверждения, сопровождающегося потерей эластичности.
Достоинства эпоксидов состоят в очень малой усадке (0,2 – 0,5%), адгезии к различным материалам, механической прочности, химической стойкости, совместимости с другими видами смол (ФФС, кремнийорганическими), большом выборе отвердителей и других добавок. Данные качества делают эти материалы незаменимыми во многих отраслях техники.
Если же учесть высокие диэлектрические и влагозащитные свойства эпоксидов, становится понятным, почему именно они стали основным герметизирующим материалом радиокомпонентов и микроэлектронной аппаратуры (см. также 1.5.3) и связующим главного слоистого пластика РЭА - стеклотекстолита (см. далее).
Наконец, отверждённые эпоксидные смолы оптически прозрачны и широко применяются в оптоэлектронных приборах (фотоприёмниках, светодиодах, оптопарах).
Кремнийорганические смолы представляют собой неорганические цепи, состоящие из атомов кремния и кислорода и обрамлённые органическими радикалами. Основа строения – силоксановая цепочка:
|
Эти материалы могут быть как термопластичными и иметь линейную структуру молекул,
|
так и термореактивными с пространственной структурой типа

где под Н подразумеваются органические радикалы: этил – С2Н5, метил - СH3, фенил - C6H5.
Свойства кремнийорганических соединений зависят от характера силоксановой связи и наличия органических радикалов у атома кремния. Химическая связь кремний - кислород термически более устойчива, чем углерод - углеродная связь, что определяет более высокую нагревостойкость кремнийорганических полимеров по сравнению с большинством органических. Органические радикалы у атомов кремния снижают термическую стойкость материалов, но одновременно придают им водостойкость и эластичность, характерные для органических веществ.
Благодаря высокой нагревостойкости кремнийорганические соединения используются в сочетании с нагревостойкими неорганическими материалами (слюдой, стекловолокном) в виде миканитов, стеклотканей, пластмасс. Кроме того, кремнийорганические полимеры применяются в лаках, компаундах, пластмассах. Вследствие того, что кремнийорганические соединения практически не смачиваются водой, они используются для гидрофобизации, т.е. придания водоотталкивающих свойств пластмассам, керамике и другим материалам. К недостаткам этих смол относятся их сравнительная дороговизна, низкая механическая прочность, плохая адгезия к большинству других материалов.
Параметры термореактивных полимеров без наполнителей приведены в таблице 1.8.
Таблица 1.8 - Основные параметры термореактивных полимеров.
| Параметры | Фенолформальде-гидные смолы | Эпоксидные смолы | Кремнийорганические смолы |
| ρv, Ом · м e (50 Гц) tgδ (50 Гц) Епр, МВ/м Нагревостойкость, °С | 109 – 1010 5,0 – 6,5 0,06 – 0,1 12 - 16 105 - 120 | 1012 - 1013 3,0 – 4,0 0,01 – 0,03 20 - 80 120 - 140 | 1012 - 1014 3,5-5,0 0,01 – 0,03 15 - 2 5 180 - 220 |
1. 7. Композиционные пластмассы и слоистые пластики
Пластмассы - многокомпонентные вещества, состоящие в большинстве случаев из связующего и наполнителя, а также включающие в себя и другие материалы (рис.1.9).
Выбирая состав и количество компонентов пластмассы можно получать детали с теми или иными механическими и электрическими свойствами. Изготовление деталей из пластмасс производится на специальном оборудовании. Исходными материалами являются пресс-порошки. Термопласты перерабатывают литьем под давлением, экструзией, прямым прессованием и обрабатывают различными способами, реактопласты - прямым и литьевым прессованием, литьем под давлением, обрабатывают механическим путем, склеиванием и иногда химической сваркой.

Рисунок 1.9. Состав композиционных порошковых пластмасс.
Композиционные пластмассы широко применяются в РЭА в качестве электроизоляционных и чисто конструкционных материалов: для изготовления корпусов радиоприемников, телевизоров, видеомагнитофонов, измерительных приборов, наушников, ламповых панелек, клеммных щитков, головок кнопок, рукояток, штепсельных разъемов и др. Производство таких деталей механической обработкой было бы весьма трудоемко, прессование же из пластмассы позволяет получить их за одну технологическую операцию.
Слоистые пластики - это разновидность композиционных пластмасс, в которых в качестве наполнителя используется волокнистые листовые материалы (бумага, ткань, стеклоткань), пропитанные и склеенные между собой различными полимерными связующими. Слоистые пластики отличаются от других материалов тем, что применяемый наполнитель располагается параллельными слоями. Такая структура обеспечивает высокие механические характеристики, а использование полимерных связующих - достаточно высокое удельное сопротивление и электрическую прочность.
В зависимости от материала связующего и наполнителя различают несколько типов слоистых пластиков (таблица 1.9).
Таблица 1.9 - Состав основных типов слоистых пластиков.
| Слоистый пластик | Наполнитель | Связующее |
| Гетинакс Текстолит Стеклотекстолит | Пропиточная бумага толщиной 0,1 мм. Хлопчатобумажная и синтетическая ткани (саржа, бязь, шифон, лавсан). Стеклоткани из бесщелочного алюмоборосиликатного стекла. | ФФС ФФС Совмещённая эпоксидная и ФФС. Совмещённая эпоксикремнийорганическая смола. |
Слоистые пластики являются сильнополярными диэлектриками, так как и связующее, и наполнитель обладают полярными свойствами. Основные параметры слоистых пластиков представлены втаблице 1.10.
Таблица 1.10 - Параметры слоистых пластиков.
| Материал | ρv, Ом·м | er | tg δ | Рабочая температура, °С |
| Гетинакс Текстолит Стеклотекстолит | 1011 - 1012 1011 - 1012 1012 - 1013 | 5,3 4,5 5,0 | (6-10)·10-3 (8-30)·10-3 (5-10)·10-3 | -60 + 100 -60 + 105 -60 + 120 |
Слоистые пластики используются как диэлектрические основания печатных плат (ПП), которые являются типовыми несущими конструкциями современной РЭА. Печатные платы - это слоистая структура, в состав которой, кроме основания, входят печатные проводники (медная фольга).
Самый дешевый материал диэлектрических оснований - гетинакс - широко применяется в бытовой радиоаппаратуре. Его недостаток - повышенное влагопоглощение через слои бумаги или из открытых их торцевых срезов, а также сквозь полимерное связующее. Выпускается гетинакс на основе ацетилированной бумаги, имеющей повышенную влагостойкость и способной заменить стеклотекстолиты.
Текстолит обладает более высокой прочностью при сжатии и ударной вязкостью, поэтому он используется также в качестве конструкционного материала. Его выпускают не только в виде листов, но и плит толщиной до 50 мм. Текстолит в 5-6 раз дороже гетинакса.
Стеклотекстолиты благодаря ценным свойствам наполнителя имеют наиболее высокую механическую прочность, теплостойкость и минимальное водопоглощение. У них лучшая стабильность размеров, а электрические свойства остаются высокими и во влажной среде. Из-за необычной твердости поверхности стеклотекстолиты износоустойчивы.
Качество ПП характеризуется следующими свойствами (рис. 1.10).
Рис. 1.10
Прочность - одно из основных свойств, так как печатные платы выполняют роль не только диэлектрического основания, но и несущей конструкции.
Нагревостойкость фольгированных слоистых пластиков определяется по отсутствию вздутий, расслаивания и отклеивания фольги, возникающих при пайке. Критерием является время в секундах, в течение которого разрушения не наблюдаются при нагреве до 260° С. Минимальная нагревостойкость - 5 с., у лучших марок - 20 с.
Стабильность размеров - изменение длины при смене температур в процессе пайки, когда вся плата перегревается примерно до 120° С; ТКЛР стеклотекстолита при толщине 1,5 мм составляет 8·10 1/град, т.е. отличается от ТКЛР меди более чей в 2 раза, поэтому при больших размерах плат возможен обрыв или отслоение фольги. Нестабильность размеров проявляется также в виде неплоскостности - прогиба, коробления, скручивания, возникающих из-за механических напряжений.
Электрическая прочность стеклотекстолита анизотропна: в продольном направлении она в несколько раз выше, чем в направлении толщины. Причина этому - анизотропия самого материала и наличие микротрещин, уменьшающих эффективную толщину, но не длину и ширину. С увеличением толщины электрическая прочность падает: для плат толщиной 0,5 и 10 мм значение Епр соответственно 30 и 10 кВ/мм.
Недостатки фольгированных стеклотекстолитов - коробление, нестабильность размеров, растрескивание, отслаивание, воспламеняемость - обусловлены неоднородной структурой и используемыми для их изготовления материалами.
Кроме того, повышение плотности монтажа, применение групповых методов пайки, тяжелые условия эксплуатации требуют связующих, обладающих большей теплостойкостью. Наконец, стеклотекстолит из-за высокого tgδ непригоден для СВЧ-техники.
По этой причине для изготовления ПП применяются термопласты, которые позволяют повысить нагревостойкость до 400° С и существенно уменьшить тангенс угла диэлектрических потерь для применения в СВЧ-аппаратуре. При этом лучшим материалом является фторопласт, армированный стеклотканью и фольгированный с двух сторон. Его выпускают в виде листов толщиной 0,5 мм под маркой фторопласт-4Д армированный фольгированный (ТУ 6-05-164-78). Он нагревостоек до 250 °С, имеет tgδ = 0,0007 при частоте 10 ГГц и пригоден для СВЧ-техники. Однако применение фторопласта должно быть строго обосновано, так как он примерно в 10 раз дороже стеклотекстолита.
1.8. Полимерные клеи и адгезивы
Клеи - это вещества, обладающие высокой адгезионной способностью, которые используются для соединения между собой материалов разных классов. Преимущество склеивания (в отличие от сварки и пайки) заключается в том, что изделие не требуется нагревать до высоких температур. При этом само соединение может обладать эластичностью. Это обеспечивает прочность в условиях термоударов, динамических нагрузок, при большой разнице ТКЛР.
Универсальных клеев не существует; труднее поддаются склеиванию металлы, легче - неметаллы. Поэтому клей, предназначенный для металлов, пригоден и для неметаллов, но гораздо реже бывает обратное. Так, эпоксидные клеи применимы для всех материалов, а не модифицированные фенолформальдегидные, кремнийорганические, поливинилацетатные (ПВА) хорошо склеивают только неметаллы.
В клеи на основе термореактивных смол часто вводятся наполнители и добавки, которые придают им следующие свойства:
- биостойкость (соединения мышьяка и ртути);
- негорючесть (оксид сурьмы):
- способность вспениваться (фреоны, карбонаты);
- электропроводность (порошки серебра или никеля);
- теплопроводность (нитрид бора).
Химическая промышленность поставляет большое количество клеев, причем их исходное состояние может быть различным:
- жидкость, содержащая летучий растворитель, или без него;
- твердое тело в форме легкоплавких порошков, таблеток, гранул;
- расплав на основе термопластов;
- липкая лента с постоянной липкостью или активируемая растворителями, водой, повышением температуры.
Особое значение в технологии РЭА имеют тепло- и электропроводящие клеи. Они используются для крепления полупроводниковых кристаллов ИС к металлизированным корпусам с обеспечением теплового и электрического контакта, а также выводов к контактным площадкам. Назначение электропроводящего покрытия состоит в экранировании РЭА от электромагнитных полей.
Главной проблемой при разработке электропроводящих клеев-контактолов - является выбор наполнителя. Тонкодисперсная медь очень быстро окисляется в составе полимерной композиции и годится только в посеребренном виде. Для экономии серебра (наполнитель в электропроводящем клее составляет 60 - 80 % по массе) можно использовать также посеребренный графит.
Поскольку ассортимент клеев очень велик, выбор оптимального из них для данного назначения представляет собой довольно сложную задачу. Клеи, предназначенные для металлов, не должны содержать анионов Сlֿ,Iֿ, Fֿ,  ,
,  , способные вызвать их коррозию. Эластичные материалы можно клеить только эластичными клеями на основе кремнийорганических полимеров. Пластмассы лучше клеить материалами, близкими по химической природе. Разнородные материалы можно склеить надежнее, если использовать не один вид клея, а два, более соответствующие двум склеиваемым материалам по природе. Если соединяемые поверхности плохо подогнаны, целесообразно применить вспенивающиеся клеи.
, способные вызвать их коррозию. Эластичные материалы можно клеить только эластичными клеями на основе кремнийорганических полимеров. Пластмассы лучше клеить материалами, близкими по химической природе. Разнородные материалы можно склеить надежнее, если использовать не один вид клея, а два, более соответствующие двум склеиваемым материалам по природе. Если соединяемые поверхности плохо подогнаны, целесообразно применить вспенивающиеся клеи.
Оптимальная толщина слоя клея, обеспечивающая наиболее прочное соединение, - 0,1...О,2 мм.
Недостатки клеевых соединений:
- невысокая механическая прочность, особенно сопротивление отдиранию;
- высокое тепловое сопротивление;
- непригодность для СВЧ аппаратуры (за исключением клеев-расплавов).
1.9. Стекла.
1.9.1 Способы аморфизации материалов
Как известно, для аморфных твердых тел характерны полная изотропия свойств и отсутствие определенной температуры плавления. Такими истинно аморфными веществами являются многие природные и искусственные полимеры. Естественное стремление этих веществ к кристаллизации подавляется тем, что длинные молекулы полимеров неудобны для правильной упаковки.
Кроме полимеров, в аморфное состояние можно перевести и другие вещества - диэлектрики, полупроводники и даже металлы, для которых наиболее характерным является кристаллическое состояние. Различные способы аморфизации материалов представлены на рис. 1.11.
При естественном охлаждении получить аморфную структуру удается у расплавов, обладающих высокой вязкостью. При их затвердевании частицы не успевают проделать даже минимальное смещение, необходимое для кристаллизации, и твердое тело сохраняет неупорядоченность, свойственную расплаву. Высокой вязкостью, обладают расплавы смесей многих оксидов, типичным компонентом которых является кварц SiO2. Подсчитано, что высоковязкие стеклообразующие расплавы могли бы кристаллизоваться со скоростями в несколько атомных рядов в сутки, т.е. 1 мкм примерно за 3 года.
Такую большую вязкость стеклообразующих расплавов, постепенно возрастающую при снижении температуры, можно объяснить тем, что входящие в их состав атомы или ионы объединяются в крупные молекулы и в комплексы (кластеры). По мере роста кластеров вязкость плавно увеличивается. Так образуется типичное стекло - неорганический гомогенный изотропный продукт затвердевания вязкого расплава при естественном охлаждении.
Гораздо труднее реализовать аморфное состояние металлов, не склонных образовывать кластеры в расплаве, а в твердом состоянии имеющих наиболее плотную упаковку с координационным числом 8-12 и ненаправленную металлическую связь. Получить аморфные металлы (металлостекла) удается при огромных скоростях охлаждения - около 10 град/с, что можно обеспечить, если толщина затвердевающего слоя не превышает 50 мкм; получением тонких лент пока и ограничиваются возможности этого метода.
Наконец, аморфизацию многих материалов можно осуществить осаждением из газовой фазы или в вакууме из молекулярного пучка на холодную подложку. Как правило, чем ниже температура подложки, тем, меньше проявляется способность пленочного материала кристаллизоваться. Поэтому при достаточно глубоком охлаждении можно получать даже аморфные металлы (например, медь).
Аморфизация в последнее время выступает как метод, позволяющий значительно расширить возможности известных материалов и получить оригинальные сплавы с совершенно новыми необычными свойствами. Это пример интенсивного развития, когда новые материалы создаются без использования дефицитных и редких элементов, а за счет лишь более искусного управления структурой.

Рис. 1.11. Способы аморфизации материалов.
1.9.2. Общая характеристика стекол
Силикатное стекло являются одним из старейших материалов, известных человечеству. Тем не менее, наука о стекле все ещё не может ответить на многие важные вопросы. Шутят, что о стеклах легче сказать, чем они не являются, нежели определить, что же это такое. Стекла представляют собой неупорядоченные структуры, не имеют определенного химического состава (за исключением кварцевых стекол), температуры плавления.
Установлено, что основой строения силикатных стекол является комплекс SiO4 - тетраэдр с очень прочными связями Si=0. Отдельные тетраэдры могут быть скреплены в цепи так называемым "мостиковым кислородом" (рис.1.12).

Рис. 1.12. Основа строения силикатных стекол.
Благодаря некоторой закономерности строения силикатных колец стекло нельзя считать бесструктурным материалом. В нем имеется ближний порядок, т.е. правильная ориентация атомов распространяется на значительно меньшее, чем в кристалле, расстояние.
Влияние ближнего порядка на свойства материала наименее поддается теоретическому изучению, и, хотя экспериментировать со стеклом сравнительно несложно, интерпретация полученных данных крайне затруднительна. Это усложняет предсказание свойств новых стекол и объяснение их поведения в тех или иных условиях обработки и эксплуатации. Однако накопленный практический опыт позволяет использовать стекла во всех сферах науки и техники.
Преимущества и недостатки стекол по сравнение с другими материалами показаны на рис.1.13.
Рис. 1.13. Характеристика стекол.
1.9.3. Химический состав и свойства оксидных стекол
 |  |  |
Рис. 1.14. Состав оксидных стекол.
Стеклообразующими, т.е. способными создавать пространственную сетку, являются помимо SiO2 также, например, B2O3, GeO, P2O3.
Однако свойства стекол определяются не только стеклообразующими оксидами, они сильно зависят от других примесей, называемых модификаторами. Не образуя в стекле собственных каркасов, многие примеси способны нарушать структуру стеклообразующих оксидов и вследствие этого менять, модифицировать свойства стекла.
Например, оксиды щелочных металлов (Na2O, K2O) вводятся в стекла для снижения температуры варки, обработки и подавления склонности стекла к кристаллизации (расстекловыванию).
Однако слабо связанные щелочные ионы под действием теплового движения могут срываться с мест закрепления и перемещаться из одной ячейки пространственной сетки в другую, что приводит к усилению ионно-релаксационной поляризации и сопровождается ростом tgδ. При этом уменьшается ρ, так как возрастает количество ионов, участвующих в процессе электропроводности (рис.1.15).
В то же время присутствие в составе стекла двух различных щелочных оксидов увеличивает eи уменьшает tgδ по сравнению со стеклом, содержащим только один щелочной оксид. Такое явление называется нейтрализационным или полищелочным эффектом. Для уменьшения вредного влияния оксидов щелочных металлов на электрические свойства в стекло вводят оксид щелочноземельных металлов (СаО, ВаО).
Третью группу компонентов стекла составляют оксиды, способные в зависимости от состава и условия получения входить в каркас стеклообразователя и разрушать его структуру. Кним относятся Al2O3, РbО, ZnO и другие оксиды, не вошедшие в 1-ю и 2-ю группы.


Рис. 1.15. Влияние оксидов щелочных металлов на электрические свойства стекол.
Таблица 1.11.
Влияние различных оксидов на свойства стекол.
| Параметр | Оксиды, входящие в состав стекла | |
| повышают параметр | понижают параметр | |
| 1. Механические: модуль упругости твердость 2. Теплофизические. нагревостойкость теплопроводность ТКЛР 3. Электрические er, tgδ,Eпр | Al2O3 SiO2 SiO2, Al2O3 SiO2, B2O3, Al2O3 Na2O Na2O, K2O, TiO2, PbO Na2O, K2O SiO2, Al2O3 | B2O3, PbO PbO, Na2O PbO, Na2O SiO2, B2O3, TiO2 SiO2 SiO2, B2O3 Na2O |
Изменение свойств и параметров стекол в зависимости от вводимых в их состав оксидов качественно показано в табл.1.11.
Рассмотрим подробнее теплофизические свойства стекол, отличающиеся наибольшим своеобразием. В связи с неупорядоченным состоянием и отсутствием свободных электронов стекла обладают очень низкой теплопроводностью, в сотни раз меньшей, чем металлы. Поэтому стеклянные детали - подложки, стенки корпусов, даже пленки - имеют высокое тепловое сопротивление и плохо пригодны для отвода тепла.
Уже в процессе формования изделия из-за опережающего охлаждения поверхностных слоев и низкой теплопроводности создается перепад температуры. По мере охлаждения внешние слои стекла теряют пластичность и создают сжимающие напряжения в объеме, а сами растягиваются. Если эти усилия превысят предел прочности стекла, произойдет его разрушение. Наличие остаточных напряжений характерно для стекла, поэтому изделия могут разрушаться как самопроизвольно, так и под действием даже небольших перепадов температуры или очень малых механических нагрузок. Для снятия остаточных напряжений стеклянные изделия необходимо подвергнуть отжигу - длительной термообработке при равномерном по объему детали нагреве.
Но и после этого прочность стекла составляет лишь около 0,01 от теоретической (рассчитанной по энергии связи электронов) из-за микротрещин на поверхности - очагов хрупкого разрушения.
Способность материала сохранять прочность при быстрой смене температур (термоударах) тем выше, чем меньше температурный коэффициент линейного расширения. Кварцевое стекло, обладающее самим низким из всех материалов ТКЛР = 5·10-7 1/град, не разрушаясь, выдерживает смену температур 1000° С - вода.
От значения ТКЛР зависит также способность стекла к соединению с другими материалами сваркой. Расхождение в значениях ТКЛР стекла и свариваемого с ним материала не должно превышать 5%, и этот параметр служит основной характеристикой стекла, содержащейся в самом обозначении его марки согласно ГОСТ.
В зависимости от состава стекло обрабатывают при 600-1600° С, причем ценность представляют как тугоплавкие кварцевые стекла, использующиеся в качестве контейнеров и реакторов в полупроводниковом производстве и в составе паст для металлизации керамики, так и легкоплавкие, необходимые для герметизации приборов иИС, изготовления корпусов, проводниковых и резистивных паст.
1.9.4. Техническое назначение стекол
В зависимости от назначения стекла делятся на электровакуумные, изоляторные, герметизирующие, конденсаторные (рис.1.16).
Электровакуумные стекла применяются для баллонов, ножек и других деталей электровакуумных приборов. Определяющим параметром является ТКЛР стекла, который должен быть близок к ТКЛР соединяемых с ним материалов. Эти стекла делятся на вольфрамовую, молибденовую и платиновую группы, причем эти названия определяются не составом стекла, а близостью значений ТКЛР стекол к ТКЛР вольфрама, молибдена и платины.
Изоляторные стекла - наиболее массовая продукция среди электротехнических стекол, поэтому одно из главных требования к ним - доступность сырья, низкая стоимость. Из стекла изготавливают около половины изоляторов простой формы - штыревых и подвесных, изоляторы более сложной конфигурации делают из фарфора.
Герметизирующие стекла широко используются в качестве тонких покрытий, наносимых на поверхность полупроводниковых приборов и ИС для защиты областей p-n-переходов от диффузии извне примесей. Они также должны предохранять кристалл от механических повреждений, а алюминиевую разводку ИС - от коррозии. Стеклянные корпуса ИС значительно дешевле металлических и керамических. Через них проще вывести контакты, так как стекло - диэлектрик и достаточно лишь спая металл - стекло (в металлических корпусах необходим трехслойный спай - металл-стекло-металл). Недостатки стеклянных корпусов заключаются в низкой теплопроводности и механической прочности.
Широкий диапазон значений er, низкий tgδ, высокие ρ и Епр стекол позволяют их использовать в конденсаторах.
1.9.5. Кварцевое стекло высокой чистоты
Рассмотренные стекла не является "чистыми", поскольку содержат примеси, способные загрязнить контактирующие с ними полупроводники. Посуда из обычного стекла непригодна для химической обработки полупроводников даже при комнатной температуре из-за выщелачивания его компонентов. Поэтому в технологии ИС широко применяется кварцевое стекло, состоящее на 99,99% и более из SiO2. Применение такого стекла в виде труб, тиглей и реакторов особенно уместно при обработке кремния, так как при этом снимается проблема поступления примесей от реакторов и контейнеров - наиболее близкого и потенциально опасного источника загрязнения. Для получения и обработки других полупроводников, например, GaAs, пришлось также использовать кварцевую аппаратуру, что сразу же проявилось в высоком уровне загрязнения кремнием, являющимся электрически активной примесью - донором в GaAs.
Помимо высокой чистоты кварцевое стекло обладает такими ценными свойствами, как нагревостойкость (длительно 1200° С, в течение нескольких часов - 1400° С), предельно низкий ТКЛР - 5·10-7 1/град, гарантирующий стойкость кварца к термоударам.
Из-за высокой температуры изготовления деталей из кварцевого стекла (более 1700° С) оно является наиболее дорогим среди других силикатных стекол. К другим недостаткам также относятся сравнительно низкий срок службы из-за частичной кристаллизации (расстекловывания) и низкая механическая прочность. Непосредственно в изделиях РЭА кварц используется как подложки ГИС СВЧ.
1.10. Стеклокристаллические материалы – ситаллы
Стремление избавиться от главных недостатков стекла, повысить его устойчивость к механическим и термическим воздействиям привело к созданию стеклокристаллического материала - ситалла. Если в состав стекол, склонных к кристаллизации, ввести одну или несколько добавок веществ, дающих зародыши кристаллизации, то удается стимулировать процесс кристаллизации стекла по всему объему изделия иполучить материал с однородно» мелкокристаллической структурой.
Ситаллы получают преимущественно по стекольной технологии из вязкой стекломассы специального состава (рис.1.17).
Стекломассы


|
Рис. 1.17. Технологическая схема изготовления ситалла.
Таким образом, ситалл отличается от стекла мелкокристаллической микроструктурой, причем размеры кристаллитов около 1 мкм, а их содержание достигает 50 – 90% по объему. Отличие ситаллов от керамики - значительно меньший размер кристаллитов.
Кристаллизация стекла может быть обусловлена фотохимическими и каталитическими процессами. В первом случае центрами кристаллизации служат мельчайшие частицы металлов (серебра, золота, меди, алюминия и др.), которые выделяются под влиянием ультрафиолетового излучения из соответствующих оксидов, входящих в состав стекла. Затем проводится термообработка, при которой происходит образование и рост кристаллитов вокруг металлических частиц. Одновременно материал приобретает определенную окраску. Полученные таким способом материалы называют фотоситаллами.
При каталитической кристаллизации технология изготовления ситаллов упрощается, так как отпадает необходимость в предварительном облучении. В этом случае в качестве катализаторов кристаллизации используются соединения, ограниченно растворимые в стекломассе или легко кристаллизующиеся из расплава, например, FeS, TiO2, фториды и фосфаты щелочных и щелочно-земельных металлов. Полученные при этом материалы называются термоситаллами.
В процессе ситаллизации стекла наиболее существенно изменяются следующие его свойства:
- повышается механическая прочность из-за того, что поверхностные трещины, наталкиваюсь на кристаллиты, не могут развиваться так интенсивно, как в стекле;
- растет нагревостойкость, так как диапазон температур размягчения-плавления значительно сужается по сравнению со стеклами;
- появляется возможность регулировать параметры (например, ТКЛР) за счет изменения степени ситаллизации, т.е. доли кристаллической фазы.
В табл.1.12 приведено сравнение параметров литиевого ситалла и аналогичного по значению ТКЛР стекла. Видно, что по многим параметрам ситалл превосходит стекло. Его недостатком является меньшая химическая стойкость вследствие неоднородной структуры. От керамики ситаллы отличаются хорошей обрабатываемостью, отсутствием пористости, меньшей стоимостью.
Ситаллы марок Ст32, Ст38, Ст50 (цифра обозначает ТКЛР) в виде полированных пластин толщиной 0,5-1 мм размером 60·48 мм являются основным материалом подложек тонкопленочных ГИС.
Таблица 1.12
Сравнение параметров стекол и ситаллов.
| Параметр | Стекло С-52-1 | Ситалл ПГБ-30 |
| Прочность, МПа ТКЛР, 1/град tgδ Епр, МВ/м Нагревостойкость,°С | 0,3-0,5 52·10-7 4,9·10-3 | 1,1-1,2 58·10-7 1,0·10-3 |
Дата добавления: 2015-10-21; просмотров: 155 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Твердеющие диэлектрики | | | ТЕХНИЧЕСКАЯ КЕРАМИКА |