
|
Читайте также: |
В процессе обмена веществ пищевые продукты (углеводы, липиды) подвергаются катаболизму.
Катаболизм – это процесс расщепления высокомолекулярных веществ до низкомолекулярных веществ, идущий с выделением энергии. В процессе катаболизма происходит упрощение структуры высокомолекулярных веществ.
Энергия, выделившаяся в процессе катаболизма, используется для синтеза новых веществ, т.е. в процессе анаболизма.
Взаимодействие превращения вещества и энергии называются метаболизмом.
Процессы окисления протекают в организме и вне организма. Эти процессы имеют сходства и различия.
Сходство между окислением в организме и вне организма.
Различия между окислением в организме и вне организма.
1. Вне организма энергия выделяется за счет окисления атомов углерода, а в организме за счет окисления атомов водорода.
Процесс окисления субстратов в биологических объектах называется биологическим окислением.
Виды биологического окисления.
Тканевое дыхание – многоступенчатый ферментативный процесс, в котором конечным акцептором электронов является кислород.
В процессе тканевого дыхания участвую ферменты – оксидоредуктазы, образующие дыхательную цепь.
Дыхательная цепь – это комплекс оксидоредуктаз, участвующих в переносе протонов и электронов от окисляемого субстрата к кислороду.
Дыхательная цепь локализована в кристах митохондрий.
Строение дыхательной цепи.
Дыхательная цепь включает 4 группы ферментов:
1. Пиридинзависимые дегидрогеназы – коферментом является НАД, НАДФ.
2. Флавинзависимые дегидрогеназы – коферментом является ФАД, ФМН.
3. Коэнзим Q или убихинон.
4. Цитохромы b, c, a, a3.
Цитохромы являются геминовыми белками, в качестве небелковой части содержат гем. В составе гема содержатся атом железа, который может изменять степень окисления с +3 до +2, присоединяя или отдавая электрон.
В составе дыхательной цепи выделяют два участка:
1. Участок, включающий пиридинзависимые дегидрогеназы – коэнзим Q обеспечивает перенос протонов и электронов. На уровне коэнзима Q протоны уходят в среду митохондрий, т.к. цитохромы по своему строению способны переносить только электроны.
2. Участок цитохромов, обеспечивающий перенос только электронов.
Основное значение цитохромной системы перенос электронов от окисляемого субстрата на молекулярный кислород с образованием воды:
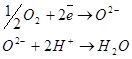
Схема переноса электронов и протонов по дыхательной цепи.
 По дыхательной цепи от окисляемого субстрата до кислорода передается 2 протона и два электрона.
По дыхательной цепи от окисляемого субстрата до кислорода передается 2 протона и два электрона.
Коферменты дыхательной цепи принимая протоны и электроны превращаются в восстановленную форму, а отдавая их снова превращается в окисленную форму.
Движущей силой, обеспечивающей перенос протонов и электронов от субстрата к кислороду, является разность редокс-потенциалов. В дыхательной цепи происходит нарастание редокс-потенциала (от –0,32 в до +0,81 в О2)
Для синтеза одной макроэргической связи АТФ требуется перепад редокс-потенциалов между участками дыхательной цепи примерно в 0,22 в на пару перенесенных электронов.
Длина дыхательной цепи (количество ферментов) может быть различна и зависит от природы окисляемого субстрата.
Для клетки важно, чтобы молекула кислорода, присоединив 4 электрона, полностью восстановилась до двух молекул воды. При неполном восстановлении кислорода в случае присоединения двух электронов образуется перекись водорода, а в случае присоединения одного электрона – супероксидный радикал  . Перекись водорода и супероксидный радикал токсичны для клетки, т.к. повреждают клеточные мембраны, взаимодействую с остатками ненасыщенных жирных кислот мембранных липидов.
. Перекись водорода и супероксидный радикал токсичны для клетки, т.к. повреждают клеточные мембраны, взаимодействую с остатками ненасыщенных жирных кислот мембранных липидов.
Аэробные клетки защищают себя от действия перекиси и супероксида с помощью двух ферментов: супероксиддисмутазы и каталазы.

Пути использования энергии переноса электронов.
При переносе пары электронов происходит изменение свободной энергии и эта энергия используется по двум путям:
1. Энергия переноса электронов используется на синтез АТФ.
2. Энергия переноса электронов используется для выработки тепла.
При переносе пары электронов по дыхательной цепи происходит изменение свободной энергии, равная 52,6 ккал. Этой энергии достаточно для синтеза 3 молекул АТФ. Синтез трех молекул АТФ в стандартных условиях требует затраты 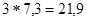 ккал.
ккал.
В трех пунктах переноса электронов происходит наибольшее изменение свободной энергии и эти пункты называются пунктами сопряжения тканевого дыхания и окислительного фосфорилирования.
Окислительное фосфорилирование это процесс ресинтеза АТФ из АДФ и Фн, сопряженный с тканевым дыханием.
Пункты сопряжения находятся на участках:
1. НАД/ФАД
2. ц в/ц с
3. ц а/а3  О2
О2
Пункты сопряжения постоянны, но их количество зависит от природы окисляемого субстрата.
При окисления НАД – зависимых субстратов имеет место 3 пункта сопряжения, т.е. выделяется 3АТФ, при окислении ФАД – зависимых субстратов имеет место 2 пункта сопряжения и выделяется 3 АТФ, при окислении цитохромзависимых субстратов, количество АТФ, зависит от того, на какой цитохром сбрасываются электроны: при сбросе электронов на цитохром b выделяется 2АТФ в процессе окислительного фосфорилирования, а на цитохром с – 1АТФ.
 Коэффициент фосфорилирования – это соотношение Р/О как показатель сопряжения дыхания и фосфорилирования.
Коэффициент фосфорилирования – это соотношение Р/О как показатель сопряжения дыхания и фосфорилирования.
Было установлено, что при поглощении одного атома кислорода (или при переносе пары электронов от субстрата к кислороду) поглощается не один атом неорганического фосфата, а примерно три т.е. коэффициент Р/О примерно равен 3. Т.е. в дыхательной цепи имеется как минимум три пункта сопряжения, где неорганический фосфат участвует в образовании АТФ.
Процесс биологического окисления может не сопровождаться синтезом АТФ.
Окисление, не сопровождающееся синтезом АТФ, называется свободным окислением. В этом случае энергия выделяется в виде тепла. Это может наблюдаться при действии токсинов и сопровождается повышением температуры тела.
Причины нарушения биологического окисления.
1. Недостаток субстратов окисления (углеводов, липидов, т.е. пищи).
2. Нарушение работы ферментов в дыхательной цепи:
1. Дефект апофермента (нарушен синтез белковой части фермента).
2. Дефект кофермента (нарушение синтеза коферментов из-зи недостатка витаминов В2,В5, К).
3. Недостаток кислорода.
4. Действие ингибиторов.
Аминобарбитал ингибирует перенос протонов и электронов на участке НАД/ФАД, окисление НАДзависимых субстратов прекращается.
Антимицин ингибирует перенос электронов на участке цитохром b, цитохром с.
Цианады ингибируют перенос электронов на участке цитохромоксидазы/кислород.
При большинстве физиологических состояний перенос электронов сопряжен с окслительным фосфорилированием.
Ряд соединений может вызвать разобщение тканевого дыхания и окислительного фосфорилирования. Разобщителями этих процессов являются следующие соединения: 2,4 – динитрофенол, гормон щитовидной железы – тироксин, дикумарин и его производные, жирные кислоты.
Разобщение окислительного фосфорилирования и тканевого дыхания может быть биологически полезным. Разобщение представляет собой способ генерирования тепла для поддержания температуры тела у зимнеспящих животных и млекопитающих адаптированных к холоду. В качестве разобщителя выступают жирные кислоты, которые накапливаются в бурой жировой ткани. Такой бурый жир есть и у новорожденных детей, что позволяет поддерживать температуру тела при еще несовершенной системе терморегуляции.
У больных с гиперфункцией щитовидной железы отмечается повышение температуры тела, что обусловлено разобщением процессов тканевого дыхания и окислительного фосфорилирования, вызванного тироксином.
При недостатке кислорода в тканях процесс тканевого дыхания затруднен и в тканях протекает субстратное окисление.
Субстратное окисление – это процесс окисления, при котором конечным акцептором электронов является субстрат, а не кислород.
Субстратное окисление – это аварийный источник получения энергии при недостатке кислорода.
Недостаток кислорода (гипоксия) возникает в организме при физической работе, при подъеме в горы, опускании под воду, при заболеваниях органов дыхания, сердечно-сосудистой системы и кроветворной системы.
Субстратное окисление энергетически менее выгодно, чем тканевое дыхание, т.к. редокс-потенциалы субстратов отличаются незначительно.
В организме наряду с окислительным фосфорилированием процессом, дающим энергию является субстратное фосфорилирование.
Субстратное фосфорилирование – это процесс образования макроэргических соединений за счет макроэргических связей субстрата.
Важнейшим макроэргическим соединением является АТФ.
Энергия макроэргических связей аккумулируется в ряде соединений: креатинфосфат, 1,3-дифосфоглицерат, ГТФ и др.
Биологическое окисление
Тканевое дыхание Свободное окисление Субстратное окисление
Связано с Энергия
окислительным выделяется
фосфорилированием в виде тепла
Энергия выделяется
в виде АТФ
Фосфорилирование
Окислительное фосфорилирование Субстратное фосфорилирование
связано с мембранами митохондрий не связано с мембранами
митохондрий
| Процесс | Ингибиторы тканевого дыхания | Разобщители тканевого дыхания и окислительного фосфорилирования | Ингибиторы синтеза АТФ |
| Аминобарбитал, ротенон, антимизин, цианиды | 2,4-динитрофенол, жирные кислоты, дикумарин и его производные, тироксин | Антибиотики олигомицин, рутамицин | |
| Ионофоры: | Валиномицин, грамицидин |
Одно время пытались использовать некоторые разобщающие агенты для борьбы с ожирением за счет понижения эффективности синтеза АТФ. Но эти вещества оказались крайне токсичны, и потому от такого их применения отказались.
Существует еще группа веществ как ионофоры, т.е. переносчики ионов. Это жирорастворимые вещества, способные связывать определенные ионы и переносить их через мембрану. Ионофоры отличаются от разобщителей тем, что ионофоры переносят через мембрану не ионы водорода, а какие-нибудь другие катионы. Например, токсичный антибиотик валиномицин образует жирорастворимый комплекс с ионами К+, легко проходящий через внутреннюю мембрану митохондрий, тогда как в отсутствие валиномицина ионы К+ проникают сквозь нее с трудом. Ионофор грамицидин облегчает проникновение ионов К+ и Na+.
Ионофоры и разобщители подавляют окислительное фосфорилирование, увеличивая проницаемость мембраны для ионов Н+, К+ или Na+.
Окислительное фосфорилирование
Ферменты ЦПЭ фиксированы в митохондриальной мембране и их действие характеризуется не только величиной, но и пространственной направленностью, т.е. действуют векторно.
Проявлением векторности является перенос ионов Н+ с внутренней стороны мембраны (со стороны матрикса) на наружную. С НАДН электроны переходят на ФМН, а протоны освобождаются с внутренней стороны мембраны. Протоны, необходимые для восстановления ФМН, поступают из матрикса. На следующем этапе электроны с ФМН Н2 переходят на убихинон, а протоны – в межмембранное пространство; убихинон получает протоны из матрикса и так далее. ЦПЭ работает как протонный насос, перекачивая ионы Н+ из матрикса на наружную сторону мембраны. В результате по сторонам мембраны возникает разность концентраций протонов и одновременно разность электрических потенциалов со знаком + на наружной повехности.
Электрохимический потенциал заставляет протоны двигаться в обратном направлении – с наружной поверхности внутрь. Движение протонов идет по протонным каналам, где располагается АТФ-аза, катализирующая реакщию:
АДФ + Н3РО4 = АТФ + Н2О
АТФ при участии транслоказы поступает из матрикса на наружную сторону мембраны, а затем в цитозоль.
Гипотеза Митчелла
Согласно этой гипотезе, цепь переноса электронов – насос, перекачивающий ионы Н+. Энергия, высвобождаемая при переносе электронов используется для перемещения ионов Н+ из митохондриального матрикса наружу, что приводит к возникновению электрохимического Н+- градиента сболее высокой концентрацией ионов Н+ в наружной водной фазе. Этот же процесс ведет к появлению трансмембранного электрического потенциала – наружная сторона мембраны оказывается электроположительной. Ионы Н+ из окружающей среды вновь устремляются внутрь, т.е. в митохондриальный матрикс, на этот раз по электрохимическому градиенту. Этот переход ионов Н+ из зоны с более высокой в зону с более низкой их концентрацией сопровождается выделением свободной энергии, за счет которой синтезируется АТФ.
Электрохимический Н+-градиент с более высокой концентрацией Н+ на наружной мембране.
Трансмембранный электрический потенциал – наружная мембрана заряжена положительно, а внутренняя – отрицательно.
Ионы Н+ из окружающей среды по электрическому градиенту идут внутрь митохондрии и этот процесс сопровождается выделением свободной энергии, которая идет на синтез АТФ.
Обмен углеводов.
Обмен углеводов в организме человека складывается из следующих процессов:
1. Расщепление в желудочно-кишечном тракте до моносахаридов поступающих с пищей полисахаридов с пищей полисахаридов и дисахаридов. Всасывание моносахаридов из кишечника в кровь.
2. Синтез и распад гликогена.
3. Анаэробное окисление глюкозы. В тканях существует два основных пути распада глюкозы: анаэробный путь гликолиза, который идет без потребления кислорода, и аэробный путь прямого окисления глюкозы или пентозофосфатный путь.
4. Аэробный метаболизм пирувата, включающий окислительное декарбоксилирование пирувата и превращение ацетил-КоА в ЦТК.
5. Глюкогенез, т.е. образование углеводов из неуглеводных продуктов, таких как пируват, лактат, глицерин, аминокислоты.
Обмен углеводов.
| Обмен углеводов | |||
| Распад (гликогенолиз) и синтез (гликогенез) гликогена | Гликолиз | Пентозо- фосфатный путь | глюконеогенез |
| Окислительное декарбоксилирование пирувата | |||
| ЦКТ |
Значение углеводов в организме:
1. Углеводы – это основной энергетический материал.
2. Углеводы выполняют пластическую функцию. К ним относятся пентозы нуклеотидов и гликопротеинов, гетерополисахариды межклеточного вещества.
3. Углеводы могут превращаться в липиды и некоторые аминокислоты.
Источником углеводов организма служат углеводы пищи – крахмал, сахароза и лактоза. Кроме того, глюкоза, может образовываться в организме из аминокислот, глицерина.
Углеводы пищи в пищеварительном тракте распадаются на мономеры. В переваривании принимают участие гидролазы.
Специфические гидролазы: мальтаза, сахараза, лактаза вырабатываются клетками кишечника и содержатся в кишечном соке.
Продукты полного переваривания углеводов – глюкоза, галактоза и фруктоза – через клетки кишечника поступают в кровь. При всасывании из кишечника в кровь моносахариды проникают через клеточные мембраны путем облегченной диффузии и с помощью активного транспорта. Активный транспорт обеспечивает перенос моносахаридов против градиента концентрации, и поэтому может функционировать тогда, когда концентрация глюкозы или галактозы в кишечнике невелика.
Важнейшие сахара через воротную вену проникают в печень, где идет превращение фру и гал в глю.
Гликолиз.
Гликолиз (от греч. glykys – сладкий, lysis - распад) – один из центральных путей катаболизма глюкозы.
В процессе гликолиза происходит расщепление шестиуглеродной молекулы пирувата. Первые пять этапов составляют подготовительную стадию гликолиза. Продуктом первой стадии гликолиза является глицеральдегид-3-фосфат. Подготовительная стадия гликолиза служит для того, чтобы превратить углеродные цепочки всех метаболизируемых гексоз в один общий продукт – глицеральдегид-3-фосфат.
Вторая стадия гликолиза, состоящая тоже из 5 ферментативных реакций, сопровождается образованием энергии.
Стадии гликолиза.
I. 1. Фосфорилирование глюкозы: реакция протекает необратимо, катализируется гексокиназой и требует затраты АТФ:

Необратимые реакции – это реакции, протекающие в прямом направлении под действием одного фермента, а в обратном под действием другого.
Связывание гексогеназы с гексозой происходит по типу индуцированного соответствия: молекула фермента претерпевает конформационные изменения. Активность гексокиназы ингибируется глю-6-фосфатом.
В печени присутсвует другая форма фермента – глюкокиназа. Глюкокиназа специфична в отношении D-глюкозы. Глюкокиназа печени действует при возрастании концентрации глюкозы, например после приема пищи, богатой углеводами.
Гликолиз включает химические превращения 3 разных типов:
1. Распад углеродного скелета глюкозы с образованием пирувата (путь атомов углерода).
2. Фосфорилирование АДФ высокоэнергетическими фосфорилированными содинениями с образованием АТФ (путь фосфатных групп).
3. Перенос водородных атомов или электронов.
Ферменты, катализикующие гликолиз, локализованы в цитозоле.
Ферменты, катализирующие те этапы окисления углеводов, которые требуют присутствия О2, локализируются в митохондриальных мембранах.
В этих условиях глюкокиназа действует на избыточную глюкозу крови и переводит ее в глюкозо-6-фосфат для отложения в запас в виде гликогена.
В мышечной ткани глюкокиназа отсутствует.
2.Превращение глю-6-ф во фру-6-ф

3. фосфорилирование фру-6-ф во фру-1,6-дф
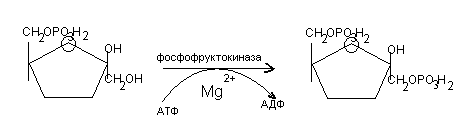
4. Расщепление фру-1,6-дф на триозы:

В дальнейших превращениях принимает участие глицеральдегид-3-ф, который образуется в результате изомеризации дигидроксиацетонфосфата:
Дигидроксиацетонфосфат  глицеральдегид-3-фосфат
глицеральдегид-3-фосфат
В количественном отношении больше образуется дигидроксиацетонфосфата.
II. На второй стадии гликолиза запасается энергия.
Из одной молекулы глю образуется две молекулы глицеральдегид-3-фосфата, которые участвуют в дальнейших превращениях.
1. Окисление глицеральдегид-3-фосфата до 1,3-фосфоглицероилфосфата: дифосфоглицериновая кислота (гликолитическая оксидоредуктация)
СН2ОРО3Н2 СН2ОРО3Н2
| глицеральдегид- 2 |
СНОН фосфатдегидрогеназа CHOH


 | |
| |
С=О C=O
| 2НАД++Фн 2НАДН+Н+ |
Н OPO3H2
3-ФГА 1,3-фосфоглицератфосфат
Коферментом глицеральдегидфосфатдегидрогеназы является НАД+. Механизм действия этого фермента очень сложен.
2. Образование 3-фосфоглицерата:

3. Образование 2-фосфоглицерата:

4. Образование фосфоенолпирувата – субстратное фосфорилирование:
 Высокоэнергетическое фосфорилированное соединение фосфоенолпируват.
Высокоэнергетическое фосфорилированное соединение фосфоенолпируват.
5. Образование пирувата:

Дальше процесс идет в зависимости от наличия или отсутствия кислорода в клетке.
При анаэробных условиях, например в напряженно работающих скелетных мышцах. Пируват превращается в лактат:

В этих условиях образовавшийся при гликолизе НАДН регенерируется за счет пирувата, d восстанавливается до лактата.
Электроны, пришедшие сначала от глицеральдегид-3-фосфат к НАД+, переносятся в форме НАДН на пируват. Восстановление НАД катализируется ЛДГ.
С накоплением лактата в скелетных мышцах связано возникновение чувства усталости. ЛДГ представлена 5 различными изоферментами. ЛДГ сердечной мышцы характеризуется низкой Кm для пирувата, а ЛДГ мышечной ткани имеет более высокую величину Кm для пирувата.
Суммарная реакция:
Глю + 2АДФ + 2Фн  2Лак + 2 АТФ
2Лак + 2 АТФ
При анаэробном гликолизе образуется 4 молекулы АТФ, но выделяется только 2 молекулы, т.к. 2 молекулы АТФ затрачиваются в процессе фосфорилирования.
Значение анаэробного гликолиза:
Окисление глю в условиях недостатка кислорода в тканях позволяет получить энергию клеткой при гипоксии, которая может быть вызвана физической нагрузкой, а также нарушениями со стороны сердечно-сосудистой и дыхательной систем. При ИБС наблюдается анаэробный гликолиз, т.к. нарушается при дефиците О2 работа дыхвтельной цепи, а следовательно окисление глю и жирных кислот, которые является главнейшими источниками энергии.
II. При достаточном содержании О2 в клетке глю окисляется до конечных продуктов – СО2, Н2О и этот процесс называется аэробным окислением глю.

Конечным продуктом аэробного гликолиза является пируват, а энергетический баланс складывается из 3 молекул АТФ образовавшихся в результате субстратного фосфорилирования и остается еще 2 молекулы восстановленного НАДН, от концентрации которого зависит активность процесса. Для продолжения процесса необходим сброс Н2 на ферменты дыхательной цепи, но сама молекула НАДН через мембрану митохондрий проникнуть не может, для этого используются переносчики и перенос осуществляется с помощью 2-х механизмов:
1. Глицерофосфатный челночный механизм;
2. Малатно-аспартатный челночный механизм.
Глицерофосфатный челночный механизм.
| Цитоплазма | Митохондрии | |
  
| 
|
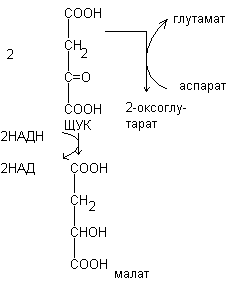
Малатный челночный механизм.
| Цитоплазма | Митохондрии | |
| 
|
В процессе гликолиза образуется восстановленная форма НАДН, которая не может непосредственно передавать водород на дыхательную цепь, т.к. митохондриальная мембрана непроницаема для НАДН. Перенос водорода с цитозольного НАДН в митохондрии происходит при участии специальных механизмов, называемых челночными. Суть механизмов сводится к тому, что НАДН в цитозоле восстанавливает какое-то соединение, способное проникать в митохондрию; в митохондрии это соединение окисляется, восстанавливая внутримитохондральный НАД, и вновь переходит в цитозоль.
Баланс аэробного гликолиза:
1. Анаэробный гликолиз – субстратное фосфорилирование – 2АТФ
Глю  2пир
2пир
2. 2Пир  2 СН3СОSKoА – окислительное декарбоксилирование 2 НАДН- 6АТФ
2 СН3СОSKoА – окислительное декарбоксилирование 2 НАДН- 6АТФ
3. Регенерация 2 НАДН в челночном механизме - 6 АТФ
4. ЦТК  2 СН3СОSKoА
2 СН3СОSKoА  СО2 24 АТФ
СО2 24 АТФ
 Н2О
Н2О
38 АТФ
СХЕМА ГЛИКОЛИЗА.

Включение в гликолиз других моносахаридов.
В гликолиз вовлекаются, кроме глюкозы и другие моносахара. Такие как D-фруктоза, манноза и галактоза.
Фруктоза и манноза фосфорилируются с помощью неспецифической гексокиназы с образованием фруктозо-6-фосфата и является метаболитом гликолиза. Маннозо-6-фосфат изомеризуется фосфоманнозоизомеразой во фруктозо-6-фосфат.
Имеется и другой путь включения фруктозы в гликолиз. Фруктоза под действием фруктокиназы печени превращается во фруктозо-1-фосфат, а под действием альдолазы расщепляется на дигидроксиацетонфосфат и глицеральдегид.
Галактоза сначала также фосфорилируется в печени с помощью галактокиназы: D-галактоза + АТФ  галактозо-1-Ф +АДФ Затем галактозо-1-фосфат превращается в глюкозо-1-фосфат. Для этой реакции изомеризации необходимы уридиндифосфат-глюкоза (УДФ-глюкоза) и фермент галактозо-1-фосфат-уридилтрансфераза:
галактозо-1-Ф +АДФ Затем галактозо-1-фосфат превращается в глюкозо-1-фосфат. Для этой реакции изомеризации необходимы уридиндифосфат-глюкоза (УДФ-глюкоза) и фермент галактозо-1-фосфат-уридилтрансфераза:
Галактозо-1-фосфат + УДФ-глюкозо  УДФ-галактоза + глюкозо-1-фосфат
УДФ-галактоза + глюкозо-1-фосфат
Глюкозо-1-фосфат подключается к гликолизу, а УДФ-галактоза превращается в УДФ-глюкозу с помощью УДФ-глюкозо-эпимеразы.

Пентозофосфатный (апотамический) путь окисления глюкозы.
Большая часть глюкозы расщепляется в тканях по гликолитическому пути с образованием пирувата. В свою очередь большая часть пирувата окисляется через цикл лимонной кислоты. Главный смысл расщепления глюкозы в процессе гликолиза заключается в обеспечении клетки энергией в форме АТФ. Наряду с этим существуют, однако, и другие пути катаболизма глюкозы, имеющие специальное назначение. На этих путях вырабатываются особые продукты, в d нуждается клетка.
Пентозофосфатный или фосфоглюконатный путь является источником в организме специальных продуктов:
Значение:
1. НАДФН, d используется как источник восстановительных эквивалентов в процессах биосинтеза жирных кислот, стероидов.
2. Рибозо-5-фосфата (пентозы), d используется для синтеза нуклеиновых кислот.

3. Образование АТФ.
По другому вторичному пути катаболизма глюкозы в животных тканях образуются два специализированных продукта: D-глюконат, важная роль которого связана с обезвреживанием и выведением из организма чужеродных органических веществ, и L-аскорбиновая кислота (витамин С).
Реакции пентозофосфатного пути протекают в цитозоле.
Взаимосвязь пентозного пути и гликолиза.

Обмен гликогена.
Глюкоза как моносахарид свободно диффундирует через мембрану печеночных клеток, она не может служить резервом углеводородов в печени. Так как фосфатные эфиры глюкозы и фруктозы не столь легко проникают через мембраны, фосфорилирование этих сахаров создает как бы ловушку для них, эффективно изолируя реакции гликолиза и фосфоглюконатного пути в пределах внутриклеточного отсека. Тем не менее фосфаты сахаров не могут накапливаться в больших количествах в печени, так как благодаря осмосу увеличение их запасов будет сопровождаться накоплением больших количеств воды.
В печени происходит превращение избытка углеводов в нерастворимый полимер – гликоген. Эта резервная форма глюкозы может составлять одну десятую всей массы печени. При голодании запас гликогена почти полностью истощается.
Обмен гликогена включает в себя 2 процесса: гликогенез или синтез гликогена и гликогенолиз или распад гликогена.
Гликогенез – синтез гликогена – это анаболический процесс, требующий затраты энергии в форме как АТФ, так и уридинтрифосфата (УТФ). Исходным источником для синтеза гликогена является глю, d под действием глюкокиназы превращается в глю-6-фосфат.
Глю -6-ф занимает ключевое положение как общий промежуточный продукт ряда процессов углеводного обмена: он способен к обратимому превращению в пируват путем гликолиза или глюконеогенеза, а также к необратимому – в пентозы в ходе фосфоглюконатного пути. Глю-6-ф может обратимо превращаться в гликоген.
Затем глю-6-ф превращается в глю-1-ф. В процессе активации глю-1-ф участвуют уридиннуклеотиды. В ходе этого процесса два концевых фосфорных остатка УДФ освобождаются в виде неорганического пирофосфата, остаток УМФ соединяется с глю-1-ф, образуя УДФ-глюкозу.
Источником глю при синтезе гликогена является УДФ-глю, d образуется из глюкозо-1-ф и УТФ:
Глю-1-ф + УТФ 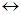 УДФ=глю + Н4Р2О7
УДФ=глю + Н4Р2О7
На следующей стадии происходит перенос остатка глю с УДФ-глю на затравку гликогена с помощью гликогенсинтетазы:
УДФ-глю + (глю)n  УДФ +(глю)n+1
УДФ +(глю)n+1
Гликогенсинтетаза катализирует образование только  -1,4-гликозидных связей. «Ветвящий» фермент образует
-1,4-гликозидных связей. «Ветвящий» фермент образует  -1-6 гликозидные S (точки ветвления).
-1-6 гликозидные S (точки ветвления).
Гликогенолиз – распад гликогена идет путем фосфоролиза.

Биосинтез углеводов.
Гликолиз, пентозофосфатный путь, гликгенолиз – это катаболические пути, которые сходятся в цикле лимонной кислоты, чтобы передать свои богатые энергией электроны в дыхательную цепь. Перемещаясь по дыхательной цепи к кислороду, эти электроны поставляют энергию для синтеза АТФ. Теперь нам предстоит рассмотреть анаболические пути. На этих путях химическая энергия в форме АТФ и НАДФН используется для синтеза клеточных компонентов из простых предшественников.
Организационные принципы биосинтеза.
1. Пути биосинтеза и пути расщепления тех или иных биомолекул, как правило, не идентичны. Эти пути могут включать какую-нибудь общую обратимую реакцию или даже несколько таких реакций, но у них всегда имеется хотя бы одна ферментативная стадия, по которым они различаются.
2. Биосинтетические пути и соответствующие им катаболические пути контролируется разными регуляторными ферментами. Обычно регуляция соответствующих биосинтетических и катаболитических путей осуществляется координированным образом, реципрокно, так что стимулирование биосинтетического пути сопровождается подавлением катаболитического пути и наоборот. Кроме того, биосинтетические пути регулируются обычно на одном из первых этапов. Это избавляет клетку от непроизводительных трат: она не расходует предшественники на синтез тех промежуточных продуктов, которые ей не понадобятся.
3. Требующие затраты энергии биосинтетические процессы обязательно сопряжены с поставляющем энергию расщеплением АТФ, вследствие чего весь процесс в целом является практически необратимым, точно также как в целом необратим катаболизм. Таким образом, общее количество АТФ (или НАДН), используемое на данном биосинтетическом пути, всегда превосходит то минимальное количество свободной энергии, которое требуется для превращения предшественника в биосинтетический продукт.
Центральным биосинтетическим путем является образование глюкозы из неуглеводных предшественников. У всех высших животных и человека биосинтез глюкозы абсолютно необходимый процесс. Глюкоза крови служит единственным или главным источником энергии для нервной системы (в том числе и для мозга), а также для почек, семенников, эритроцитов и для всех тканей эмбриона. У человека один только мозг потребляет 120 г глюкозы в сутки.
Образование глюкозы из неуглеводных предшественников называется глюконеогенезом (образование нового сахара).
В процессе глюконеогенеза глюкоза синтезируется из лактата, пирувата, глицерола, и большинства аминокислот, из промежуточных продуктов цикла лимонной кислоты.
Глюконеогенез протекает в печени и значительно менее интенсивно – корковом веществе почек.
При гликолизе глю превращается в пируват, при глюконеогенезе пируват превращается в глюкозу. Глюконеогенез это не обращение гликолиза, т.к. в гликолизе есть 3 необратимые стадии, катализируемые гексокиназой, фосфофруктокиназой и пируваткиназой.
Пути глюконеогенеза обходят эти 3 необратимые реакции гликолиза при помощи следующих новых этапов:
1. Фосфоенолпируват ббразуется из пирувата через оксалоацетат.
Первый этап в обходной последовательности реакций катализируется митохондриальной пируваткарбоксилазой. Этот биотинзависимый фермент катализирует образование оксалоацетата из пирувата:
Пируват + СО2+АТФ  оксалоацетат+АДФ+Рн
оксалоацетат+АДФ+Рн
Пируваткарбоксилаза – регуляторный фермент; в отсутствии ацетил-КоА который служит для нее положительным регулятором, она почти полностью лишена активности.
Оксалоацетат, образующийся в митохондриях из пирувата обратомо восстанавливается за счет НАДН с образованием малата:
Митох. НАДН+Н+ + Оксалоацетат  НАД+малат
НАД+малат
Малат из митохондрий поступает в цитозоль. В цитозоле малат под действием цитозольной НАД-зависимой малатдегидрогеназы превращается в оксалоацетат:
Цитозоль Малат + НАД+  Оксалоацетат+ НАДН+Н+
Оксалоацетат+ НАДН+Н+
Дальше оксалоацетат под действием фосфоенолпируваткарбоксикиназы превращается в фосфоенолпируват:
Оксолоацетат+ГТФ  ФЭП+СО2 +ГДФ
ФЭП+СО2 +ГДФ
Донором фосфата в этой реакции служит ГТФ – гуанозинтрифосфат.
2. Вторая реакция гликолиза, которая не может использоваться для глюконеогенеза – это реакция фосфорилирования фру-6-ф, катализируемая фосфофруктокиназой.
В глюконеогенезе действует обходной путь с участием фруктозодифасфатазы, которая катализирует необратимый гидролиз фру-1,6-дф с образованием фру-6-ф
Фру-1,6-дф  фру-6-ф
фру-6-ф
Фруктозодифосфотаза – регуляторный фермент, нуждается в ионах Mg2+. Ингибируется АМФ, активируется АТФ.
3. Третьей обходной реакции в синтезе глюкозы является дефосфорилирование глю-6-ф с образованием глю.
Дефосфорилирование осуществляется под действием глюкозы-6-фосфатазы:
Глю-6-ф  глю
глю
Глюконеогенез требует значительных затрат энергии. Стадии глюконеогенеза, требующие затрат энергии:
Пир + СО2 + АТФ  оксалоацетат + АДФ + Фн
оксалоацетат + АДФ + Фн
Оксалоацетат + ГТФ  ФЕП + СО2 + ГДФ
ФЕП + СО2 + ГДФ
3ФГК  1,3ФГК
1,3ФГК
На каждую молекулу глю потребуется 6 высокоэнергетических фосфатных групп – 4 от АТФ и 2 от ГТФ.
Кроме того, для восстановительных этапов требуется 2 молекулы НАДН:
1,3 ДФГК + НАДН + Н+  3ФГА + НАД+
3ФГА + НАД+
Суммарная реакция:
2Пир + 4 АТФ + 2 ГТФ + 2 НАДН + 2 Н+ + 4 Н2О  Глю + 2 НАД+ + 4 АДФ + 2 ГДФ + 6 Рн
Глю + 2 НАД+ + 4 АДФ + 2 ГДФ + 6 Рн
Главную роль из метаболитов ЦТК, используемых в глюконеогенезе играют: цитрат, изоцитрат,  -кетоглутарат, сукцинат, фумарат, малат.
-кетоглутарат, сукцинат, фумарат, малат.
Важно отметить, что в норме ацетил-КоА не используется как предшественник глю, так как он не может превратиться в пируват.
В глюкозу могут превращаться глюкогенные аминокислоты: аланин, глутамат, аспартат, которые превращаются соответственно в пируват, оксалоацетат и  -кетоглутарат:
-кетоглутарат:
Глукогенные аминокислоты
Превращаются в пир: ала, сер, цис, гли
Превращаются в оксалоацетат: асп, асн
Превращаются в сукцинил-КоА: вал, тре, мет
Превращаются в  -кетоглутарат: глу, глн, про, арг, гис.
-кетоглутарат: глу, глн, про, арг, гис.
Поставляют атомы углерода для синтеза глю и кетоновых тел: фен,тир, изолей, лиз, три
Синтез глю из малых молекул предшественников идет в период после восстановления после мышечной нагрузки, например после бега на сто метров. В этом случая в качестве источника энергии служит гли, который окисляется с образованием лак и выделением АТФ. Т.к. кислорода в тканях не хватает, лактат не может подвергаться дальнейшим превращениям и поступает в кровь.
Закончивший стометровку спринтер в начале дышит тяжело, но постепенно его дыхание выравнивается и становится нормальным. К этому периоду возвращается к норме и содержание лак. За время восстановления (до 30 мин) лактат удаляется из крови в печень и превращается в процессе гликонеогенеза в глю крови. Глю крови возвращается в мышцы:
Алкоголь тормозит глюконеогенез.
Потребление больших количеств алкоголя резко тормозит глюконеогенез в печени, вследствие чего понижается содержание глю в крови, т.е. возникает гипогликемия. Это особенно сказывается после тяжелой физической нагрузки и на голодный желудок, уровень глю может понизиться до 40 и даже 30% от нормы. Гипергликемия не благоприятно сказывается на функции мозга. Она особенно опасна для тех областей мозга, которые контролируют температуру тела. Температура тела может понизиься на 20С. Старый обычай, предписывающий давать спасенным на море или в пустыне голодным или обессилившим людям водку, физиологически неоправдан и даже опасен; в таких случаях следует давать глю.
Окислительное декарбоксилирование пирувата.
Протекает в митохондриальном матриксе и связывает гликолиз с циклом трикарбоновых кислот.
Превращение пирувата в ацетил-КоА является необратимым процессом и катализируется пируватдегидрогеназным комплексом. Пируватдегидрогеназный комплекс состоит из трех ферментов и содержит пять коферментов: НАД, ФАД, ТПФ, амид липоевой кислоты, СоА. Этот процесс включает 4 реакции, суммарное уравнение записывается так:

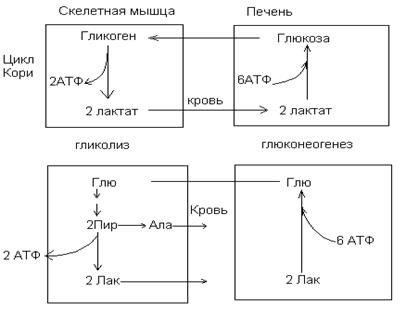
Цикл трикарбоновых кислот.
Цикл начинается с конденсации оксалоацетата (ЩУК) с ацетил –КоА с образованием цитрата и КоА. Реакция катализируется цитратсинтетазой. Далее цитрат изомеризуется в изоцитрат, через стадию образования цис-аконитата. Изоцитрат под действием изоцитратдегидногеназы превращается в  -кетоглуторат (2-оксоглутарат). Коферментом изоцитратдегидрогеназы является НАД. Дальше
-кетоглуторат (2-оксоглутарат). Коферментом изоцитратдегидрогеназы является НАД. Дальше  -кетоглутарат под действием
-кетоглутарат под действием  -кетоглутаратдегидрогеназного комплекса, содержащего НАД, ФАД, КоА, ТПФ и амид липоевой кислоты в качестве коферментов, превращается в сукцинил-КоА. На этом этапе происходит окислительное декарбоксилирование. В сукцинил-КоА имеется связь богатая энергией. При гидролизе сукцинил-КоА образуется около 8 ккал/моль, что сравнимо с величиной энергии, необходимой для синтеза АТФ (~7,3 ккал/моль).
-кетоглутаратдегидрогеназного комплекса, содержащего НАД, ФАД, КоА, ТПФ и амид липоевой кислоты в качестве коферментов, превращается в сукцинил-КоА. На этом этапе происходит окислительное декарбоксилирование. В сукцинил-КоА имеется связь богатая энергией. При гидролизе сукцинил-КоА образуется около 8 ккал/моль, что сравнимо с величиной энергии, необходимой для синтеза АТФ (~7,3 ккал/моль).
Расщепление тиоэфирной связи сукцинил-КоА сопряжено с фосфорилированием гуанозиндифосфата (ГДФ). Это реакция субстратного фосфорилирования, дающая 1моль АТФ. Это единственная реакция ЦТК, приводящая к образованию высокоэнергетической фосфатной связи. С циклом Кребса сопряжено окислительное фосфорилирование, где образование АТФ сопряжено с окислением НАД или ФАД под действием кислорода.
Затем сукцинат под действием сукцинатдегидрогеназы, содержащей ФАД в качестве кофермента превращается в фумарат. На следующей стадии фумарат подвергается реакции гидратации с образованием малата (яблочной кислоты). Малат под действием НАД-зависимой малатдегидрогеназы превращается в оксалоацетат. Следовательно, в цикле происходит регенерация оксалоацетата, что обеспечивает функционирование ЦТК.
3 НАДН и ФАДН2, образующиеся в цикле трикабоновых кислот, окисляются в дыхательной цепи (или в цепи переноса электронов). Генерирование АТФ происходит при транспорте электронов от этих переносчиков на О2. На каждую молекулу НАДН в митохондриях образуется 3 АТФ, а на молекулу ФАДН2 – 2 молекулы АТФ. Следовательно, в процессе окислительного фосфорилирования образуется 11 АТФ.
Молекулярный кислород непосредственно не участвует в цикле трикарбоновых кислот. Однако цикл функционирует лишь в аэробных условиях поскольку НАД+ и ФАД в митохондрии могут генерироваться только при переносе электронов на молекулярный кислород.
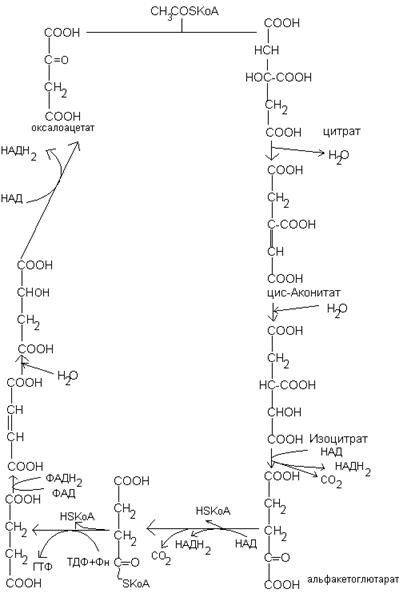
Значение ЦТК
1. * Цикл Кребса – основной путь расщепления обеспечивающий генерирование АТФ.
2. Амфиболическая – двойственная функция.
Катаболическая – распад ацетильных остатков
Анаболическая – субстраты цикла Кребса используются для синтеза.
3. Энергетическая функция – 1 АТФ
4. Водороддонорная функция – регенератор водорода для дыхательной цепи.
* Интегративная функция – объединение обмена углеводов, липидов и белков.

Патология обмена углеводов.
Нарушения обмена глюкозы проявляются в виде гипергликемии, глюкозурии и гипогликемии. Особую форму представляют нарушениями энергетического обмена при гипоксических состояниях.
Гипергликемия характеризуется повышением уровня глюкозы свыше 6 ммоль/л. Различают физиологические и патологические гипергликемии. К физиологическим гипергликемиям относятся алиментарные, возникающие при одномоментном приеме больших количеств углеводов, и нейтрогенные, например, при стрессовых ситуациях в результате выброса в кровь больших количеств адреналина. Физиологические гипергликемии носят транзиторный характер и быстро проходят.
Патологические гипергликемии обусловлены нарушением оптимального соотношения между секрецией гормонов гипо- и гипергликемического действия. Наиболее распространенное причина патологической гипергликемии – сахарный диабет, связанный с недостатком секреции инсулина поджелудочной железой. Кроме сахарного диабета гипергликемия сопутствует также заболеваниям гипофиза, сопровождающимся повышенной секрецией соматотропного гормона и АКТГ (акромегалия, опухоли гипофиза), опухолями мозгового слоя надпочечников, при которых усилено образование катехоламинов и коркового слоя надпочечников с усиленной продукцией глюкокортикоидов, гиперфункции щитовидной железы, некоторым болезням печени (инфекционный гепатит, цирроз печени).
Сахарный диабет – связан с недостаточностью инсулина, вырабатываемого  -клетками поджелудочной железы. Развитию сахарного диабета способствует избыточное потребление углеводов и жиров, малоподвижный образ жизни, стрессовые ситуации.
-клетками поджелудочной железы. Развитию сахарного диабета способствует избыточное потребление углеводов и жиров, малоподвижный образ жизни, стрессовые ситуации.
В основе сахарного диабета лежат следующие молекулярные дефекты:
1. Нарушение превращения проинсулина в инсулин в результате мутаций, затрагивающих аминокислотные остатки в участке соединения А-цепи (или В-цепи) с С-пептидом в проинсулине. У таких больных в крови высокое содержание проинсулина, лишенного гормональной активности.
2. Нарушение молекулярной структуры инсулина. Замена фен на лей сопровождается снижением гормональной активности в 10 раз.
3. Дефект рецепторов инсулина. У ряда больных секретируется нормальный инсулин, но нарушено его связывание с клетками-мишенями в результате дефекта рецепторов инсулина в плазматических мембранах.
4. Нарушение сопряжения рецепторов инсулина. У ряда больных секретируется нормальный инсулин, клетки-мишени содержат обычное количество рецепторов, но отсутствует сопряжение между инсулин-рецепторным комплексом и следующим компонентом в цепи передачи гормонального сигнала.
Важнейшими биохимическими признаками сахарного диабета являются:
1. Гипергликемия. В результате недостатка инсулина нарушается проникновение глюкозы в ткани и глюкоза накапливается в крови. В ответ на дефицит глюкозы в клетках печени усиливается распад гликогена и выход свободной глюкозы в кровь, что усугубляет гипергликемию. Возникает возможность развитие гипергликемической комы.
2. Глюкозурия и полиурия. Когда содержание глюкозы в крови превышает способность почечных канальцев к реабсорбции глюкозы она выделяется с мочой. Вместе с глюкозой выделяется много воды и больной испытывает голод и жажду.
3. Кетонемия и кетоурия. Вследствие дефицита глюкозы в тканях клетки начинают использовать в качестве энергии жиры. При  -окислении жирных кислот образуется Ацетил-КоА, который не сгорает с ЦТК полностью и из него синтезируются кетоновые тела: ацетоуксустная,
-окислении жирных кислот образуется Ацетил-КоА, который не сгорает с ЦТК полностью и из него синтезируются кетоновые тела: ацетоуксустная,  -оксимасляная кислоты и ацетон. Увеличение концентрации кетоновых тел в крови – кетонемия и выведение кетоновых тел с мочой – кетонурия.
-оксимасляная кислоты и ацетон. Увеличение концентрации кетоновых тел в крови – кетонемия и выведение кетоновых тел с мочой – кетонурия.
4. Нарушение кислотно-щелочного равновесия с развитием кетоацидоза.
Кетоновые тела сдвигают рН крови и тканевой жидкости в кислую сторону. Вначале буферные системы компенсируют сдвиг рН – компенсированный ацидоз. При тяжелых состояниях может возникнуть некомпенсированный ацидоз.
Методы диагностики сахарного диабета.
1. Определение глюкозы крови натощак.
2. Метод сахарной нагрузки (тест толерантности к глюкозе).
3. Диагностика неотложных состояний – определение глюкозы и ацетона в моче с помощью диагностических бумажных полосок – глюкотест и кетотест.
Метод сахарной нагрузки.
У больного берут кровь натощак, затем дают выпить сироп, содержащий 50г глюкозы в 200-250 мл воды. Далее через 30, 60, 150’ берут кровь и проводят определение глюкозы. У здорового человека (1) исходное содержание сахара в крови нормальное (< 5ммоль/л). После приема глюкозы в течении часа содержание глюкозы умеренно возрастает. В ответ на гипергликемию усиливается секреция инсулина, глюкоза переходит в ткани и ее содержание через 3 часа снижается до N и даже ниже.
У больного скрытым сахарным диабетом (2) содержание глюкозы на верхней границе нормы (5,7 ммоль/л). После нагрузки подъем сахара в крови более выражен и к 3 часу не достигает N из-за недостатка инсулина.
У больного явным сахарным диабетом (3) натощак определяется гипергликемия (9 ммоль/л). К 1 часу уровень глю достигает 15 ммоль/л и к 3 часу снижение незначительное, вследствие инсулинной недостаточности. Клинические симптомы: повышенный аппетит, чувство жажды, которое сопровождается полиурией. Поздние симптомы: мышечная слабость, судороги при физических нагрузках, полиневриты – т.к. нарушается использование глюкозы нервными клетками.

Особенности обмена глюкозы в клетках опухали.
В клетках опухоли отмечается повышенная активность гексокиназы, что приводит к быстрому поглощению и окислению глюкозы. Опухолевая клетка является насосом, который выкачивает глюкозу из кровотока. В условиях быстро растущей опухоли система кровеносных сосудов отстает от роста опухоли и в таких клетках протекает анаэробный гликолиз, который и дает энергию для роста клеток. Выход энергии при анаэробном гликолизе составляет 2 моль АТФ и поэтому процесс должен идти с большой скоростью, чтобы обеспечить клетки опухоли энергией. Вследствие быстрого окисления глюкозы возникает гипогликемия. Возникновение гипогликемии вызывает ускорение глюконеогенеза и глюкоза начинает синтезироваться из аминокислот. Следствием синтеза глюкозы из аминокислот является падение веса у больных и развивается раковая кахексия.
1. Мембранная гексокиназа – работает как насос.
2. Гипогликемия.
3. Анаэробный гликолиз.
4. «Принудительный» глюконеогенез.
5. Раковая кахексия.
Гликогенозы.
Гликогенозы – наследственные заболевания, характеризующиеся избыточным отложением гликогена.
| Виды гликогенозов | |
| Печеночные | Мышечные |
| Смешанные |
Гликогеноз I типа (болезнь Гирке) характеризуется дефектом фермента глюкозо-6-фосфатазы.
Признаки гликогеноза: низкий уровень глюкозы натощак в крови, в тяжелых случаях судороги, замедление роста в результате подавления выработки инсулина. Накопление гликогена из-за большого количества глюкозо-6-фосфата и активации гликогенсинтетазы. Увеличение печени, гибель гепатоцитов, низкий рост, ацидоз (лактат, пирват).
Гликогеноз VI типа (болезнь Херса).
Дефект фосфорилазы. Накопление гликогена, характерны симптомы I типа, но менее выражены (глюкоза в кровь поступает).
Мышечные гликогенозы
Гликогеноз V типа – дефект или отсутствие фосфорилазы в мышцах. Мышечные судороги при физической нагрузке, мышечноя слабость, отсутствие гипогликемии. Синтез АТФ увеличивается за счет окисления жирных кислот.
Гликогеноз VII типа – дефект только фосфофруктосинтетазы. Переносят только умеренные физические нагрузки. Развивается гемолитическая анемия.
Гликогеноз III типа (болезнь Кори) – дефект или отсутствие гликоген-6-глбконогидролазы. Увеличение содержания гликогена в печени. Гликоген состоит из коротких цепей.
Гликогеноз IV (болезнь Андерсона) – недостаток «ветвящего» фермента. Накопление гликогена с аномально длинными цепями. Развивается цирроз печени.
Агликогеноз – дефект гликогенсинтетазы. Отсутствие гликогена или его очень мало, судороги, гипогликемия.
Гемолитические анемии.
Гликолиз в эритроцитах и транспорт кислорода связаны участием в обеих процессах 2,3-дифосфоглицерата. 2,3-дифосфоглицерат снижает сродство гемоглобина к кислороду и облегчает освобождение О2 в тканях.
1. При дефекте гексокиназы снижается концентрация промежуточных продуктов гликолиза, в том числе снижается концентрация 2,3-дифосфоглицерата. В таких эритроцитах гемоглобин обладает очень высоким сродством с О2. Наступает гемолиз эритроцитов, когда гемоглобин плохо обдает О2.
2. При дефекте пируваткиназы нарушается энергетический обмен и мембрана не получает энергию, необходимую для ионного обмена и наряду с этим образуется избыток 2,3-дифосфоглицерата и связь с О2 становится слабой, сродство гемоглобина к О2 становится низким.
Глю  Глю-6-ф
Глю-6-ф  Фру-6-ф
Фру-6-ф  Фру-1,6-дф
Фру-1,6-дф  3ФГА
3ФГА 

 1,3-ДФГК
1,3-ДФГК  3-ФГК
3-ФГК  2-ФГК
2-ФГК  ФЭП
ФЭП  Пир
Пир  Лак
Лак

2,3-ДФГК
2,3-ДФГК снижает сродство Hb к О2
Недостаточность глюкозо-6-фосфотдегидрогеназы – причина лекарственной гемолитической анемии.
У ряда больных малярией применение противомалярийного препарата памахина сопровождается гемолитической анемией. Через 30 лет после начала применения препарата была выяснена причина анемии. Было установлено, что возникновение анемии связано с недостаточностью глюкозо-6-фосфатдегидрогеназы в эритроцитах. В результате недостаточности фермента нарушается образование НАДФН в пентозофосфатном пути. Главная роль НАДФН в эритроцитах состоит в восстановлении дисульфидной формы глутатиона в сульфгидрильную форму.
Г-S-S-Г + НАДФН + Н+  Г-SH +НАДФ+
Г-SH +НАДФ+
Восстановленная форма глутатиона обеспечивает обезвреживание перекиси и органических перекисей:
2 Г-SH + R-O-OH  Г-S-S-Г + Н2О + ROH
Г-S-S-Г + Н2О + ROH
Клетки со сниженным содержанием восстановленного глутатиона обладают повышенной чувствительностью к гемолизу. Возможно, что в отсутствие восстановленного глутатиона памахин и ряд других лекарственных препаратов, вызывают изменения поверхности мембраны эритроцитов за счет образования токсических перекисей.
Недостаточность глюкозо-6-фосфатдегидрогеназы в эритроцитах, по-видимому, обуславливает устойчивость к тропической малярии, т.к. для роста возбудителя необходим нормально функционирующий пентозный путь и восстановленный глутатион. Дефект фермента распространен в тех странах, где распространена малярия. Такая наследуемая недостаточность фермента может быть относительно безвредной, до тех пор, пока не вводятся определенные лекарства.
Особенности обмена углеводов в различных органах и тканях.
1. Обмен углеводов в печени.
Одной из важнейших функций печени в процессах обмена веществ является ее участие в поддержании постоянного уровня глюкозы в крови (глюкостатическая функция): глюкоза, поступающая в избытке, превращается в резервную форму, которая используется в период, когда пища поступает в ограниченном количестве.
Энергетические потребности самой печени, как и других тканей организма, удовлетворяется за счет внутриклеточного катаболизма поступающей глюкозы. В печени катаболизм глюкозы представлен 2 процессами: 1) гликолитический путь превращения 1 моль глюкозы в 2 моль лактата с образованием 2 моль АТФ и 2) фосфоглюконатный путь превращения 1 моль глюкозы в 6 моль СО2 с образованием 12 моль НАДФ.Н. Оба процесса протекают в анаэробных условиях, обе ферментативные системы содержатся в растворимой части цитоплазмы, оба пути требуют предварительного фосфорилирования глюкозы.
Гликолиз обеспечивает энергией клеточные реакции фосфорилирования, синтез белка; пентозофосфатный путь служит источником энергии восстановления для синтеза жирных кислот, стероидов.
При аэробных условиях происходит сочетание гликолиза, протекающего в цитоплазме и цикла лимонной кислоты с окислительным фосфорилированием в митохондриях достигается максимальноый выход энергии в 38 АТФ на 1 моль глюкозы. Фосфотриозы, образующиеся в процессе гликолиза, могут быть использованы для синтеза  -глицерофосфата, необходимого для синтеза жиров. Пируват, который образуется при гликолизе, может быть использован для синтеза аланина, аспартата и других соединений, через стадию образования оксалоацетата. В печени реакции гликолиза могут протекать в обратном направлении и тогда происходит синтез глюкозы путем глюконеогенеза. В пентозофосфотном пути образуются пентозы, необходимые для синтеза НК. В отличие от гликолиза фосфоглюконатный путь необратим и здесь окисляется 1/3 глюкозы, 2/3 глюкозы окисляются по гликолитическому пути.
-глицерофосфата, необходимого для синтеза жиров. Пируват, который образуется при гликолизе, может быть использован для синтеза аланина, аспартата и других соединений, через стадию образования оксалоацетата. В печени реакции гликолиза могут протекать в обратном направлении и тогда происходит синтез глюкозы путем глюконеогенеза. В пентозофосфотном пути образуются пентозы, необходимые для синтеза НК. В отличие от гликолиза фосфоглюконатный путь необратим и здесь окисляется 1/3 глюкозы, 2/3 глюкозы окисляются по гликолитическому пути.
В печени протекают гликогенез и гликогенолиз. Эти процессы взаимосвязаны и регулируются как внутри – так и внеклеточными соотношениями между поступлением и потреблением глюкозы.
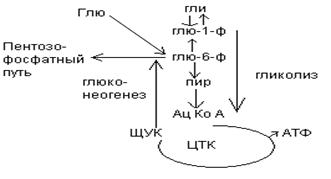

Роль печени в обмене углеводов.
От ЖКТ

Обмен углеводов в мышцах.
Печень учитывает запросы других органов и тканей в отношении углеводного обмена. В мышцах углеводный обмен происходит в соответствии с принципом самообслуживания.
Цель мышечной клетки – наиболее эффективно использовать поступающую глюкозу для образования АТФ, необходимого для осуществления механической работы – сокращения. В состоянии покоя значительные количества глюкозы резервируются в форме гликогена. Цитоплазма мышечных клеток содержит в высоких концентрациях ферменты гликолиза, а изобилие митохондрий обеспечивает эффективный распад продуктов гликолиза через путь лимонной кислоты и цепь переноса электронов. Лишь в условиях крайнего утомления эти аэробные процессы е справляются с накоплением лактата.
В мышцах идет гликогенез, мышца осуществляет лишь немногие синтетические функции. Ключевые ферменты глюконеогенеза в мышцах отсутствуют, и глюконеогенез не идет. Для востановительных синтезов в мышце НАДФ.Н не требуется, и фосфоглюконатный путь почти не функционирует.
Обмен углеводов в мышцах обеспечивает создание тканевых запасов гликогена в состоянии покоя и использование этих запасов, а также поступающей глюкозы при напряженной работе; основные энергетические потребности всех типов мышц удовлетворяются главным образом за счет окисления продуктов обмена жиров. Ни медленно сокращающаяся гладкая мышечная ткань, ни сердечная мышца не потребляют глюкозу в значительной мере. Во время напряженной работы сердце обеспечивает себя лактатом для окисления.
Обмен углеводов в мышце.


Дата добавления: 2015-10-13; просмотров: 586 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Участие в обмене веществ. | | | Доказательства белковой природы ферментов. |