
Читайте также:
|
Часовая производительность стадии алкилирования по 100% этилбензолу, кг/час:

В пересчете на кмоль:

Расход этилена с учетом селективности процесса, кмоль/ч:

Расход этиленовой фракции, кмоль/час:


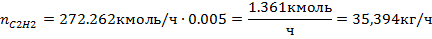






Таблица 1 – Расход этиленовой фракции
| Компонент | Xi, % | ni, кмоль/ч | mi, кг/ч |
| CH4 | 13.8 | 
| 
|
| C2H2 | 0.5 | 
| 
|
| C2H4 | 58.7 | 
| 
|
| C2H6 | 15.8 | 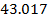
| 
|
| C3H6 | 5.3 | 
| 
|
| H2 | 1.3 | 
| 
|
| N2 | 3.1 | 
| 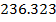
|
| O2 | 0.7 | 
| 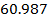
|
| CO | 0.8 | 
| 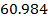
|
| Сумма | 100,00 | 272.26 | ∑ЭФ7373.353 |
Расход бензола, кмоль/час (кг/час):

С бензолом поступает воды:

Расход хлорида алюминия, кг/час (кмоль/час):


AlCl3 + 3H2O = Al(OH)3 + 3HCl
Расход хлорида алюминия, взаимодействующая с водой в растворе, кмоль/ч (кг/ч):



Этилен, переходящий в отходящие газы:

Оксид углерода, переходящий в отходящие газы:

Количество бензола в газовой фазе:
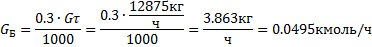
Таблица 2 – Количество и состав отходящих газов
| Компонент | ni, кмоль/ч | Xi, % | mi, кг/ч |
| CH4 | 
| 38,27 | 
|
| C2H4 | 
| 1.63 | 
|
| C2H6 | 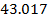
| 43.84 | 
|
| С6H6 | 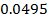
| 0.05 | 
|
| H2 | 
| 3.61 | 
|
| N2 | 
| 8.6 | 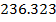
|
| O2 | 
| 1.94 | 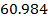
|
| CO | 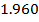
| 2.00 | 
|
| HCl | 
| 0.047 | 1.668 |
| Сумма | ∑ОГ 98.127 | 100,00 | ∑’ОГ 2301.228 |
По реакции переалкилирования:
C6H4- - (C2H5)2 + C6H6 = 2∙ C6H5- - C2H5
Количество, получаемого этилбензола:
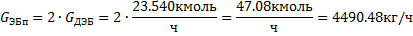
Бензола расходуется:

Алкилированием бензола получают этилбензола, кмоль/час:
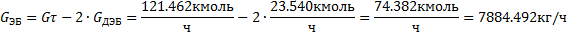
По уравнению целевой реакции (алкилирования бензола):
C6H6 + C2H4 = C6H5 – C2H5
Количество бензола, расходуемого на целевую реакцию:

Количество этилена:
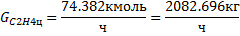
По реакции:
C6H6 +2C2H4 = C6H4 – (C2H5)2
Количество этилена, расходуемого на эту реакцию:

Количество бензола:

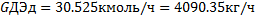
По реакции:
C6H6 + 3C2H4 = C6H3 – (C2H5)3
Количество расходуемого этилена:

Количество бензола:

Количество триэтилбензола:

На реакцию:
C6H6 + 4C2H4 = C6H2 – (C2H5)4


Количество бензола. расходуемого на тетраэтилбензол:

Количество получаемого тетраэтилбензола:

На реакцию:
C6H6 + C3H6 = C6H5 – C3H7
расходуется весь пропилен:
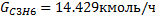
Тогда расход бензола:

Получаемый изопропилбензол:

На реакцию:
2C6H6 + C2H2 = C2H4 – (C6H5)2
расходуется весь ацетилен:


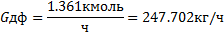
На реакцию:
2C6H6 + CO = (C6H5)– CHOH

бензола расходуется:

количество дифенилэтана:

Оставшийся бензол, переходящий в алкилат:



В алкилат уходит непрореагировавший хлорид алюминия:

Таблица 3 - Количество и состав алкилата
| Компонент | ni, кмоль/ч | xi, % | mi, кг/ч | wi, % |
| C6H6 | 374,153 | 67.99 | 29183.934 | 58.97 |
| C6H6 – C2H5 | 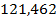
| 22.07 | 
| 26.01 |
| C6H4 – (C2H5)2 | 
| 5.54 | 
| 8.26 |
| C6H3 – (C2H5)3 | 
| 1.05 | 
| 1.92 |
| C6H2 – (C2H5)4 | 
| 0.24 | 
| 0.49 |
| C6H5 – C3H7 | 
| 2.62 | 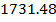
| 3.49 |
| C2H4 – (C6H5)2 | 
| 0.24 | 247.702 | 0.5 |
| (C6H5)2 – CHOH | 
| 0.08 | 
| 0.06 |
| AlCl3 | 
| 0.17 | 
| 0.25 |
| Al(OH)3 | 
| 0.003 | 
| 0.002 |
| Сумма | ∑ЖА 550.434 | ∑’ЖА49486.235 |
Таблица 4 - Упрощенный материальный баланс процесса (без учета циркулирующего бензола)
| Приход | Расход | ||||
| Компонент | Количество, кг/час | Содержание, % масс. | Компонент | Количество, кг/час | Содержание, % масс. |
| Бензол (Gб) | 
| 79.43 | Отходящие газы (ΣОГ) | 2301.228 | 4.44 |
| Этиленовая фракция (Σэф) | 7373,338 | 1.42 | Алкилат (ΣЖА) | 49486.235 | 95.54 |
| Диэтилбензол (GДЭ) | 
| 6.1 | |||
| Хлорид алюминия (GAlCl3) | 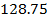
| 0.25 | |||
| Невязка | 6.122 | 0.011 | |||
| Итого | 51793.585 | Итого | 51793.585 | 100,00 |
Расчет основных расходных коэффициентов:



Дата добавления: 2015-08-21; просмотров: 137 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Технологическая схема процесса | | | Технологический расчет алкилатора |