
|
Читайте также: |
ОКСИДОРЕДУКТАЗЫ, класс ферментов, катализирующих обратимые окислит.-восстановит. р-ции, в к-рых происходит перенос восстановит. эквивалентов (двух атомов Н, двух электронов или гидрид-иона Н-) от восстановителя (спе-цифич. субстрат р-ции) к окислителю (относительно не-специфич. субстрат), напр.:
АН 2 - восстановитель, В - окислитель
Подклассы О. (их 17) сформированы по типу окисляемого в-ва (восстановителя), подподклассы - по типу окислителя (акцептора восстановит. эквивалента). О. всех подподклас-сов, для к-рых акцептором служит не О2, а любое др. соед., наз. дегидрогеназами, или редуктазами, если акцептор О2- оксидазами. В тех случаях, когда атом О включается в состав субстрата, ферменты наз. оксигеназами (при включении в молекулу одного атома О монооксиге-назами, двух атомов О-диоксигеназами), если атом О включается в виде группы ОН-гидроксилазами.
К О. относится большая группа ферментов (ок. 20% от общего их числа). Многие О. (ок. 170 ферментов) в качестве акцепторов используют никотинамидные коферменты (см. Ниацин)-никотинамидадениндинуклеотид (НАД) и никотин-амидадениндинуклеотидфосфат (НАДФ). Эти дегидрогена-зы (напр., алъдегиддегидрогеназа, лактатдегидрогеназа)выполняют важные ф-ции, участвуя в гликолизе, дыхании, брожении, а также на начальном этапе окислит, распада аминокислот при деградации белков. Нек-рые дегидрогена-зы аминокислот (напр., глутаматдегидрогеназа)могут катализировать синтез аминокислот, участвуя в ассимиляции NH3 микроорганизмами и растениями. Считается, что восстановит. эквиваленты от восстановленного НАД (т. е. от НАДН) переносятся в клетке на О2 через дыхат. цепь переноса электронов (см. Окислительное фосфорилирование), где своб. энергия этих эквивалентов расходуется для запасания энергии в виде макроэргич. связи АТФ; восстановит. эквиваленты НАДФН расходуются для биосинтетич. целей.
Ряд дегидрогеназ в качестве акцептора содержит химически прочно связанный с ферментом флавинмононуклеотид или флавинадениндинуклеотид (соотв. ФМН и ФАД; см. Рибофлавин). В таких флавопротеидах ФМН или ФАД восстанавливаются в результате окисления НАДН или НАДФН, а затем передают восстановит. эквиваленты др. компонентам цепи переноса электронов при дыхании, напр. цитохромам или непосредственно на О2. Др. продукт р-ций, катализируемых флавопротеидными О.,-Н2О2. Ферменты, использующие Н2О2 в качестве акцепторов восстановит. эквивалентов (напр., каталаза),
2)Анаэробная фаза дыхания (гликолиз).
Гликолиз осуществляется во всех живых клетках организмов. В процессе гликолиза происходит преобразование молекулы гексозы до двух молекул пировиноградной кислоты: С6Н1206 -> 2С3Н402 + 2Н2. Этот окислительный процесс может протекать в анаэробных условиях (в отсутствие кислорода) и идет через ряд этапов. Прежде всего, для того чтобы подвергнуться дыхательному распаду, глюкоза должна быть активирована. Активация глюкозы происходит путем фосфорилирования шестого углеродного атома за счет взаимодействия с АТФ:глюкоза + АТФ -> глюкозо-6-фосфат + АДФ.Реакция идет в присутствии ионов магния и фермента гексокиназа. Затем глюкозо-6-фосфат изомеризуется до фруктозо-6-фосфата. Процесс катализируется ферментом фосфоглюкоизомеразой:глюкозо-6-фосфат —> фруктозо-6-фосфат.Далее происходит еще одно фосфорилирование при участии АТФ. Фосфорная кислота присоединяется к первому углеродному атому молекулы фруктозы, процесс катализируется ферментом фосфофруктокиназой:фруктозо-6-фосфат + АТФ -> фруктозо-1,6-дифосфат + АДФ.Дальнейшие реакции, составляющие процесс гликолиза, складываются следующим образом: фруктозо-1,6-дифосфат расщепляется с образованием двух триоз, реакция катализируется ферментом альдолазой, которая состоит из четырех субъединиц и содержит свободные SH-группы. Реакция протекает по уравнению:
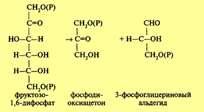 Молекула фосфодиоксиацетона при участии фермента триозофосфатизомеразы превращается также в 3-фосфоглицериновый альдегид (ФГА). Дальнейшим превращениям подвергается именно ФГА, окисляясь до 1,3-дифосфоглицериновой кислоты (ДФГК). Это важнейший этап гликолиза. Процесс идет с участием неорганического фосфата (Н3Р04) и фермента глицеральдегид-3-фосфатдегидро-геназы. Молекула этого фермента состоит из четырех идентичных субъединиц. Каждая субъединица представляет одиночную полипептидную цепь приблизительно из 220 аминокислотных остатков. Фермент содержит SH-группы и кофермент НАД, который взаимосвязан с ферментом на всем протяжении процесса. Сущность процесса заключается в окислении альдегидной группы ФГА в карбоксильную ДФГК. Окисление идет с выделением энергии. За счет энергии окисления при участии неорганического фосфата (Н3Р04) в молекуле ДФГК образуется макроэргическая фосфатная связь. Одновременно происходит восстановление кофермента НАД.
Молекула фосфодиоксиацетона при участии фермента триозофосфатизомеразы превращается также в 3-фосфоглицериновый альдегид (ФГА). Дальнейшим превращениям подвергается именно ФГА, окисляясь до 1,3-дифосфоглицериновой кислоты (ДФГК). Это важнейший этап гликолиза. Процесс идет с участием неорганического фосфата (Н3Р04) и фермента глицеральдегид-3-фосфатдегидро-геназы. Молекула этого фермента состоит из четырех идентичных субъединиц. Каждая субъединица представляет одиночную полипептидную цепь приблизительно из 220 аминокислотных остатков. Фермент содержит SH-группы и кофермент НАД, который взаимосвязан с ферментом на всем протяжении процесса. Сущность процесса заключается в окислении альдегидной группы ФГА в карбоксильную ДФГК. Окисление идет с выделением энергии. За счет энергии окисления при участии неорганического фосфата (Н3Р04) в молекуле ДФГК образуется макроэргическая фосфатная связь. Одновременно происходит восстановление кофермента НАД.
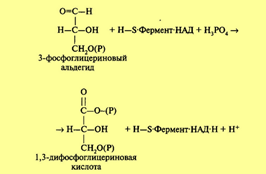
В целом реакция выглядит следующим образом:
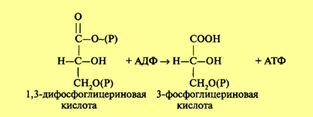
На следующем этапе за счет имеющейся макроэргической связи в 1,3-дифосфоглицериновой кислоте образуется АТФ. Процесс катализируется ферментом фосфоглицераткиназой:

Таким образом, на этом этапе энергия окисления аккумулируется в форме энергии фосфатной связи АТФ. Затем 3-ФГК превращается в 2-ФГК, иначе говоря, фосфатная группа переносится из положения 3 в положение 2. Реакция 1 катализируется ферментом фосфоглицеромутазой и идет в присутствии магния:

Далее происходит дегидратация ФГК. Реакция идет при участии фермента енолазы в присутствии ионов Mg2+ или Мп2+. Дегидратация сопровождается перераспределением энергии внутри молекулы, в результате чего возникает макроэргическая связь. Образуется фосфоенолпировиноградная кислота (ФЕП):
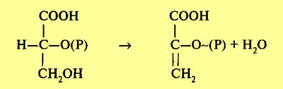
Затем фермент пируваткиназа переносит богатую энергией фосфатную группу на АДФ с образованием АТФ и пировиноградной кислоты. Для протекания реакции необходимо присутствие ионов Mg2+ или Мn2+:
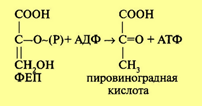
Поскольку при распаде одной молекулы глюкозы образуются две молекулы ФГА, то все реакции повторяются дважды. Таким образом, суммарное уравнение гликолиза. В результате процесса гликолиза образуются четыре молекулы АТФ, однако две из них покрывают расход на первоначальное активирование субстрата. Следовательно, накапливаются две молекулы АТФ. Образование АТФ в процессе следующее:
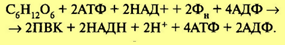
Реакция гликолиза носит название субстратного фосфорилирования, поскольку макроэргические связи возникают на молекуле окисляемого субстрата. Если считать, что при распаде АТФ из АДФ и Фн выделяется 30,6 кДж, то за период гликолиза накапливается в макроэргических фосфатных связях всего 61,2 кДж. Прямые определения показывают, что распад молекулы глюкозы до пировиноградной кислоты сопровождается выделением 586,6 кДж. Следовательно, энергетическая эффективность гликолиза невелика. Кроме того, образуются 2 молекулы НАДН, которые вступают в дыхательную цепь, что приводит к дополнительному образованию АТФ. Образовавшиеся две молекулы пировиноградной кислоты участвуют в аэробной фазе дыхания.
Дата добавления: 2015-10-30; просмотров: 408 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Транспорт у растений | | | Аэробная фаза дыхания. |