
|
Читайте также: |
Матеріальне технічне забезпечення выдбувається згідно табелю оснащення обладнанням (Наказ №951 від 04.11.2010).
Кадрові ресурси: обов’язкова підготовка лікарів та середнього медичного персоналу по технологіям УКПМД.
Наявність цілодобового лабораторного обстеження.
А.5 Індикатори якості надання допомоги новонародженій дитині з неонатальною інфекцією
| Індикатор | Порогове значення | Методика вимірювання (обчислення) | Фактори впливу | |
| 1. | Наявність УКПМД та ЛПМД надання допомоги новонародженій дитині з неонатальною інфекцією | Наявність у закладі УКПМДМ та ЛПМД надання допомоги новонародженій дитині з неонатальною інфекцією на електронних та /або паперових носіях | Наявність бази Інтернет | |
| Забезпечення навчання медичного персоналу медико-організаційним технологіям УКПМД та ЛПМД | 90% і більше | Кількість медичних працівників, які залучені до надання медичної допомоги новонародженим і пройшли навчання з практичного використання УКПМДМ та ЛПМД х100/ загальну кількість медичних працівників (фізичних осіб) | Наявність наказу по закладу про впровадження УКПМД та ЛПМД, забезпечення мотивації медичного персоналу до впровадження технологій ЛПМД | |
| Наявність можливостей для діагностичного обстеження згідно технологій | 95% і більше | Кількість обов’язкових згідно УКПМДМ та ЛПМД діагностичних досліджень, умови для виконання яких створені в закладі х 100/ кількість обов’язкових згідно УКПМДМ та ЛПМД діагностичних досліджень | Забезпечення діагностичним обладнанням згідно з табелем оснащення. Розробка функціонально-організаційних алгоритмів виконання УКПМДМ та ЛПМД | |
| Наявність сучасного медичного обладнання для проведення лікування новонароджених з неонатальними інфекціями | 95% і більше | Кількість наявного передбаченого табелем оснащення сучасного медичного обладнання х100/ кількість передбаченого табелем оснащення сучасного медичного обладнання | Залучення позабюджетних джерел для придбання необхідного медичного обладнання, участь у у міжнародних проектах, державних і регіональних програм | |
| Повний загальний аналіз крові | 99% і більше | Кількість дітей з факторами ризику або імовірним діагнозом неонатальних інфекцій, яким в перші 4 години зроблено загальний аналіз крові х 100/ загальну кількість дітей з факторами ризику або імовірним діагнозом неонатальних інфекцій | Цілодобове лабораторне забезпечення | |
| Лейкоцитарний Індекс (І:Т) | 99% і більше | Кількість дітей з факторами ризику або імовірним діагнозом неонатальних інфекцій, яким в першу добу розраховано індекс І:Т х 100/ загальну кількість дітей з факторами ризику або імовірним діагнозом неонатальних інфекцій | Навчання медичного персоналу розрахункам індексу І:Т та його оцінки | |
| Бактеріалогічне дослідження крові | 85% і більше | Кількість дітей з факторами ризику або імовірним діагнозом неонатальних інфекцій, яким в до призначення а/б зрблено бактеріальний посів крові х 100/ загальну кількість дітей з факторами ризику або імовірним діагнозом неонатальних інфекцій | Наявність можливостей для бактеріологічного дослідження | |
| Аналіз крові на С-реактивний білок (кількісний) | 90% і більше | Кількість дітей з факторами ризику або імовірним діагнозом неонатальних інфекцій, яким в перші 2 доби життя зроблено аналіз крові на С-реактивний білок х 100/ загальну кількість дітей з факторами ризику або імовірним діагнозом неонатальних інфекцій | Наявність можливостей для біохімічного дослідження | |
| Бактеріологічний аналіз матеріалу з пуповинного залишку та елементів бактеріальної інфекції шкіри | 95% і більше | Кількість дітей з імовірним діагнозом омфаліту, везикулопустульозу, пузирчатки та некротичної флегмони новонароджених, яким в першу добу після установлення імовірного діагнозу зроблено бактеріологічний аналіз матеріалу з пуповини х 100/ загальну кількість дітей з імовірним діагнозом омфаліту, везикулопустульозу, пузирчатки та некротичної флегмони новонароджених | Наявність можливостей для бактеріологічного дослідження | |
| Лабораторне та мікробіологічне дослідження виділень з ока | 95% і більше | Кількість дітей з імовірним діагнозом кон’юнктивіту, яким в першу добу після установлення імовірного діагнозу зроблено лабораторне та мікробіологічне дослідження виділень з ока х 100/загальну кількість дітей з імовірним діагнозом кон’юнктивіту | Наявність можливостей для бактеріологічного дослідження | |
| Люмбальна пункція | 85% і більше | Кількість дітей з імовірним діагнозом менінгіту, яким в першу добу після установлення імовірного діагнозу зроблена люмбальна пункція х 100/загальну кількість дітей з імовірним діагнозом менінгіту | Оволодіння лікарями навичками люмбальної пункції | |
| Дослідження функції слуху | 80% і більше | Кількість дітей з установленим діагнозом менінгіту, яким перед випискою проведено дослідження функції слуху х 100/ загальну кількість дітей з установленим діагнозом менінгіту | Наявність можливостей забезпечення новонароджених ехоскринінгом | |
| Рентгенографія органів черевної порожнини | 90% і більше | Кількість дітей з імовірним діагнозом некротичного ентероколіту, яким в першу добу після установлення імовірного діагнозу зроблено рентгенографію органів черевної порожнини х 100/ загальну кількість дітей з імовірним діагнозом некротичного ентероколіту | Наявність можливостей для рентгенологічного дослідження | |
| Аналіз калу на приховану кров | 95% і більше | Кількість дітей з імовірним діагнозом некротичного ентероколіту, яким в першу добу після установлення імовірного діагнозу зроблено аналіз калу на приховану кров х 100/ загальну кількість дітей з імовірним діагнозом некротичного ентероколіту | Повне виконання медичним персоналом технологій УКПМДМ та ЛПМД, проведення клінічного аудиту | |
| Рентгенографія органів грудної клітки | 95% і більше | Кількість дітей з імовірним діагнозом пневмонії, яким в першу добу після установлення імовірного діагнозу зроблено рентгенографію органів грудної клітини х100/ загальну кількість дітей з імовірним діагнозом пневмонії | Наявність можливостей для рентгенологічного дослідження | |
| Лабораторне та мікробіологічне дослідження пунктату уражених кісток та суглобів | 80% і більше | Кількість дітей з імовірним діагнозом остеомієліту, яким в першу добу після установлення імовірного діагнозу зроблено лабораторне та мікробіологічне дослідження пунктату уражених кісток та суглобів х100/ загальну кількість дітей з імовірним діагнозом остеомієліту | Навчання лікарів технології забору матеріалу уражених кісток та суглобів для проведення дослідження, проведення клінічного аудиту | |
| Антибіотикотерапія | 99% і більше | Кількість дітей з установленим діагнозом системної і генералізованої інфекції, яким проведено лікування антибіотиками згідно технологіям УКПМДМ та ЛПМД х100/загальну кількість дітей з установленим діагнозом системної і генералізованої інфекції | Навчання медичного персоналу технологіям УКПМДМ та ЛПМД, проведення клінічного аудиту | |
| Нейросонографія | 95% і більше | Кількість дітей з установленим діагнозом менінгіту, яким перед випискою проведено нейросонографію х 100/ загальну кількість дітей з установленим діагнозом менінгіту | Наявність можливостей для ультразвукового дослідження, проведення клінічного аудиту | |
| Консультація хірурга | 99% і більше | Кількість дітей з імовірним діагнозом остеомієліту та некротичного ентероколіту (ІІ,ІІІ), яким в першу добу після установлення імовірного діагнозу проведено консультацію хірурга х 100/ загальну кількість дітей з імовірним діагнозом остеомієліту та некротичного ентероколіту | Наявність можливостей для забезпечення консультацій «вузьких» спеціалістів, проведення клінічного аудиту | |
| Профілактика кандидозу | 95% і більше | Кількість новонароджених які отримували 10 днів і більше антибіотики, 7 днів і більше парентеральне харчування, ШВЛ, катетеризацію центральних судин та отримували противогрибкову терапію х100/ кількість новонароджених які отримували 10 днів і більше антибіотики, 7 днів і більше парентеральне харчування, ШВЛ, катетеризацію центральних судин | Забезпечення виконання технологій УКПМДМ та ЛПМД, проведення клінічного аудиту | |
| Ускладнення локальних інфекцій генералізацією інфекційного процесу | 20% і менше | Кількість дітей з установленим діагнозом локальних інфекцій, перебіг яких ускладнився генералізацією інфекційного процесу х100/ кількість дітей з установленим діагнозом локальних інфекцій | Забезпечення виконання технологій УКПМДМ та ЛПМД, проведення клінічного аудиту | |
| Ускладнення перебігу некротичного ентероколіту перфорацією кишківника | 20% і менше | Кількість дітей з установленим діагнозом некротичного ентероколіту, перебіг якого ускладнився перфорацією кишківника х100/ кількість дітей з установленим діагнозом некротичного ентероколіту | Забезпечення виконання технологій УКПМДМ та ЛПМД, проведення клінічного аудиту | |
| Лікарняна летальність при некротичному етероколиті | 10% і менше | Загальна кількість померлих новонароджених з некротичним ентероколітом х 100 /загальна кількість з установленим діагнозом некротичного ентероколіту | Забезпечення виконання технологій УКПМДМ та ЛПМД, проведення клінічного аудиту | |
| Лікарняна летальність при сепсисі | 20% і менше | Загальна кількість померлих новонароджених з сепсисом 100 /загальна кількість з установленим діагнозом сепсису | Забезпечення виконання технологій УКПМДМ та ЛПМД, проведення клінічного аудиту | |
| Лікарняна летальність при менінгіті | 20% і менше | Загальна кількість померлих новонароджених з менінгітом 100 /загальна кількість з установленим діагнозом менінгіту | Забезпечення виконання технологій УКПМДМ та ЛПМД, проведення клінічного аудиту |
Б. Бібліографія
1. Arch Dis Child Fetal Neonatal Ed 2005; 90: F220-F224; Curr Opin Infect Dis 2004; 17: 217-224
2. Manroe BL, Weinberg AG, Rosenfeld CR, et al. the neonatal blood count in health and disease. I. Reference values for neutrophilic cells. J Pediatr 1979; 95:89-98.
3. Manroe et al., Herman A. Hein, MD Peer Review Status: Internally Peer Reviewed
4. Managing Newborn Problems: A guide for doctors, nurses, and midwives. World Health Organization, Geneva. 2003 F42
5. Mouzinho A, Rosenfeld CR, Sanchez PJ, Risser R. Revised reference ranges for circulating neutrophils in very-low-birth-weight infants. Pediatrics 1994; 94:76-82.
6. Tomas E. Young, Barry Magnum. Neofax. 17 Ed., 2007
7. Практичний посібник з неонатології. 6-те видання. За ред. Судакара Г.Єзутачана, Дмитра Д. Добрянського. Львів-Детройт. 2002.
8. Red Book: Report of the Committee on Infectious Diseases, Pickering LK (Ed). American Academy of Pediatrics, Elk Grove Village, IL, 2006, p. 620.
9. American Academy of Pediatrics. Group B Streptococcal Infections. In: Red Book: 2006 Report of the Committee on Infectious Diseases, 27th ed, Pickering, LK (Ed), American Academy of Pediatrics, Elk Grove Village, IL 2006. p. 620.
10. Watterberg KL, Demers LM, Scott SM. Chorioamnionitis and early lung inflammation in infants in whom bronchopulmonary dysplasia develops. Pediatriks 1996;97: 210-15.
11. Makhoul I.R., Sujov P.; Israel Neonatal Network. Pathogen-specific mortality in very low birth weight infants with late-onset sepsis:a national survey. Clin Infect Dis.2005;40(2):218-24.
12. Hoffman R., Lohner M., Bohm N. Staphylococcal scalded skin syndrome and consetive septicemia in a preterm infant. Pathol. Res. Pract. 1994; 190:77-81.
13. John P. Cloherty, Ann R. Stark. Manual of Neonatal Care. Children of Chornobylб Relief Fund, 2002. p.-279.
14. Fanaroff et al. Pediatric Infectious Diseases J 1998; 17:539.
15. Philip, A. G. S. Early diagnosis of neonatal sepsis. Pediatrics 65: 1036,1980.
16. Stoll, B.J., Weisman, L. E. Infections in perinatology. Clin. Perinatol. 24:1,1997.
17. Hans Versmold. Richtlinien neanotologie. Berlin, 1997. p.182.
18. Goldman,R.Ellis, V. Dhar, M. S. Cairo. Rational and potential use of cytokines
19. In the prevention and treatment of neonatal sepsis. J. Clinics in perinatology. 1998, V25, 3.- p.699-709.
20. W. Benitz tn al Ptdiatrics. 1988. 102(4).
21. J. Garcia-Prats et. Al., Semin. Pediatr Infect. Dis., 2000; 11:4.
22. S.Vernano et. Al., ADCFNE, 2005; 90: F 220.
23. Pong and Bredley, Infect. Dis. Clin. North Am., 1999; 13:711.
24. Johnson C.E. et. al. Pediatrics, 1997; 99:E10.
25. Gonzalez IA, Hiil HR. The current status of intravenous gammaglobulin use in neonates. Pediatr Infect Dis J 1989;8:315-22.
26. Hill HR Intravenous immunoglobulin use in neonate: role in profylaxis and therapy of infection. Pediatr Infect Dis J1993;12:549-59.
27. Lacy JB, Ohlsson A. Administration of intravenous immunoglobulins for profylaxis or treatment of infection in preterm infants: meta-analysis. Arch Dis Child Fetal Neonatal Ed 1995;72:F151-5.
28. Reviewed by Carl Kushel. Antibiotics for Neonatal Sepsis. Newborn Services Clinical Guideline. 2003.
29. Minesh Khashu et al. Persistent Bacteriemia and Severe Thrombocytopenia Caused by Coagulased-Negative Staphylococcus in a Neonatal Intensive Care Unit. Pediatrics.February 2006; 117:340-348.
30. Reese H. Clark et al. Empiric Use of Ampicillin and Cefotaxime, Compared With Ampicillin and Gentamicin, for Neonates at Risk for Sepsis is Associated With an Increased Risk of Neonatal Death, Pediatrics. January 2006; 117:67-74.
31. Massror Pourcyrous et al. C-Reactive Protein in the Diagnosis, and Prognosis of
32. Neonatal Necrotizing Enterocolitis. Pediatrics. November 2005; 116: 1064-69.
33. A.R. Franz et. al.Measurement jf C-reactive protein reduced unnecessary antibiotic therapy in newborn infants: a multicenter, randomized, controlled trail.Pediatrics 2004;114:1-8.
34. Anhmad A., Laborada G., Nesin M. Comparison of recombinant granulosyte colony-stimylating factor and placebo for treatment of septic preterm infants. Pediatrics Infections Disease Journal, 2002:21; 1061-5.
35. Kaufman D. et al. Twice Weekly Fluconazole Profilaxis For Prevention Of Invasive Candida Infection In High-Risk Infants Of<1000 Grams Birth Weight. J of Pediatr. August 2005; 147:172-179.
36. Paolo Manzoni et al.Profilactic Fluconazole is Effective in Preventing Fundal Systemic Infections in Preterm Neonates:A Single-Center,6-Year, Retrospective Cohort Study, Pediatrics. January 2006;117:22-32.
37. Giovanna Bertini et al. Fluconazole Profilaxis Prevents Invasive Fungal Infection In High-Risc, Very Low Birth Weight Infants. J of Pediatr. August 2005;147:162-165.
38. NEUROPÄDIATRIE. Joppich, Schulte (ed) Georg Thime Verlag, 1973.
39. J.J. Volpe. Neurology of the Newborn. W.B.Saunders Company, 1987. P.609-610.
40. Textbook of Neonatology. N.R.C.Roberton, ed. Churchill Livingstone, 1992, P. 950.
41. Shattuck K.E., Chonmaitree T. The changing spectrum of neonatal meningitis over a fifteen-year period. Clin Pediatr(Phila), 1992,31(3)^P.130-136.
42. K. Malbon, R.Mohan, R.Nichol. Should a neonate with possible late onset infection always have a lumbar puncture? Archives of disease in childhood, 2006, 91: P.75-76.
43. Fluegge K, Siedler A, Heinrich B, Schulte-Moentig J. et al. Incidence and clinical presentation of invasive neonatal group B streptococcal infections in Germany. Pediatrics 2000, Vol 117, No 6 pp e1139-e1145.
44. Myiairi I, Causei KT, DeVincenzo JP, Buckingham SC. Group B streptococcal ventriculitis: a report of three cases and literature review. Pediatric Neurology, 2006,34,5: 395-399.
45. Harvey D, Holt DE, Bedford H. Bacterial meningitis in the newborn: a prospective study of mortality and morbidity. Semin Perinatol, 1999, 23,3, 218-225.
46. Kim HJ, Kim SJ, Seo WH et al. Outbreak of late-onset gbroup B streptococcal infection in healthy newborn infants after discharge from a maternity hospital: a case report. J Korean Med Sci, 2006, 21, 2, 347-350.
47. Garges HP, Moody MA, Cotton C.M. et al. Neonatal meningitis: What is the correlation among cerebrospinal fluid cultures, blood cultures and cerebrospinal fluid parameters? Pediatrics, 2006, 117,4, pp1094-1100.
48. Manual of Neonatral Care. JP Cloherty, AQR Stark (ed). Lippincott-Raven, 1997
49. A.K. Shetty, B.C.Desselle, R.D.Craver et al. Fatal cerebral herniation after lumbar puncture in a patient with a normal computed tomography scan. Pediatrics, 1999, 103, 6, pp 1284-1286.
50. Riordan FAI, Cant AJ. When to do a lumbar puncture. Archives of Disease in Childhood, 2002, 87: pp 235-237.
51. Линчевский Г.Л. Перспективи использования гематологических индексов в неонатологии / Г. Л. Линчевский, О. В. Воробьева, В. В. Татарченко // Современная педиатрия. - 2006. - № 4. - С. 151-154. (Відбір пацієнтів для обстеження, обробка отриманих даних, формулювання висновків).
52. Татарченко В.В. Особенности спонтанного НСТ-теста у новорожденньїх/ В. В. Татарченко, Д. Ю. Игнатов, О. В. Воробьева, В.А. Беленко, И. Г.Герасимов // Лабораторная диагностика. - 2007. - № 2. - С. 57-60. (Участь у плануванні експерименту, проведення НСТ-тесту, статистична обробка отриманих результатів).
53. Татарченко В. В. Тест восстановления нейтрофилами нитросинеготетразолия в диагностике бактериальнои инфекции новорожденньїх / В.
54. Протоколы диагностики, лечения и профилактики внутриутробных инфекций у новорожденных детей.- М.:ГОУ ВУНМЦ МЗ РФ, 2001.53-61.
В, Додатки
Додаток 1
ЗДІЙСНЕННЯ СПИННОМОЗКОВОЇ ПУНКЦІЇ
Здійснюється лікарем, який пройшов відповідне навчання і володіє даними навиком. Виконується тільки з інформованої згоди одного з батьків (опікуна). Люмбальна пункція використовується для підтвердження діагнозу, коли дитина має ознаки, що дають привід запідозрити менінгіт. Люмбальна пункція не виконується, якщо у дитини є spina bifida або менінгоміелоцеле.
ЗАСОБИ
· Чисті та стерильні рукавички
· Стерильні серветки
· Тампони або ватні кульки з антисептичним розчином
· Голка для спинномозкової пункції з стилетом
· Пробірки (2 шт.)
· Сухі ватяні кульки
· Лейкопластир
· Лідокаін (спрій) для місцевої анестезії
Методика
· Приготувати обладнання для первинної реанімації новонародженого (мішок Амбу та маску) (на той випадок, якщо виникне необхідність)
· Приготувати необхідні засоби
· Вкласти дитину під джерело променевого тепла і роздягнути її.
· Дотримуватися принципів профілактики інфекцій та методів асептики.
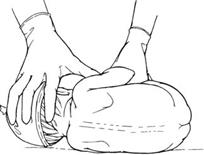
· Вибрати полодження дитини на боці
– Переконатися в тому, що голова дитини не притиснута до грудей, так як це може порушити провідність дихальних шляхів дитини.
МАЛЮНОК 1 Положення дитини лежічи
· Вимити руки та одягнути чисті рукавички
· Обробити шкіру в проекції поперекового відділу хребта, змащуючи спіральними рухами від центру до периферії тампоном або ватною кулькою, змоченою в антисептичному розчині. Повторіть процедуру ще два рази, кожного разу використовуючи новий тампон або ватяну кульку; після обробки дати поверхні просохнути.
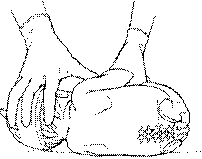
· Визначити ділянку пункції між третім та четвертим участок пункции между третьим и четвертым поперековими хребцями (на лінії, що проведена між гребенями клубових кісток)
Малюнок 2 Місце спинномозкової пункції
· Зняти рукавички та одягнути стерильні рукавички.
· Накрити тіло дітини стерильними пелюшками, залишивши неприкритим лише місце для пункції.
· Ввести голку по середній лінії хребта у напрямку до пупкового кільця дитини.
· Повільно просувати голку вперед на глибину приблизно 1 см або менше, якщо мало вагова дитина (менше 2.5 кг при народженні або народився до 37 тижня вагітності). У зв'язку з тим, що голка увійде в субарахноїдальний простір, можливо, відчуття "провалу".
· Видалити стилет
· Якщо голка впирається в кістку, її напрямок змінити не вдістся. В такому разі необхідно витягнути голку до шкіри і ще раз зробити укол, направляючи голку трошки вгору у напрямку пупка дитини.
· Зібрати цереброспінальну рідину (ЦСР):
– Взяти приблизно 0,5 мл (6 крапель) ликвору в кожну пробірку. Щоб уникнути синдрому вклинення, зібрати не більше 1 мл.
– Якщо не вдіється отримати ЦСР, необхідно трішки повернути голку.
– Якщо ЦСР як і раніше не капає, необхідно витягнути голку та повторити пункцію, вводячи її між четвертим та п’ятим поперековими хребцями.
– Якщо ЦСР з домішками крові, можливо, голка пройшла крізь спинний канал та викликала кровотечу. Якщо ЦСР кров’яниста, необхідно зібрати її для посіву та визначення чутливості збудника до антибіотиків. Якщо кров згорнулася, можливо ця кров з судини.
– Після збору ЦСР витягнути голку.
· Обережно прижати ватною кулькою місце пункції поки не припинеться кровотеча або лікворея.
· Закрити місце пункції пов’язкою та лецкопластирем.
· Забезпечити дитині спокій та горизонтальне положення протягом 2 годин.
· Спостерігати за станом дитини протягом 2 годин (увага – апное).
Додаток 2
Нормальні показники аналізу ліквору у новонароджених
Тиск 80-110 мм вод ст.
Глюкоза
Недоношені новонароджені 1,3-3,47 ммоль/л (коефіцієнт ліквор:кров 55-105%)
Доношені новонароджені 2,42-7,04 ммоль/л (коефіцієнт ліквор:кров 44-128%)
Білок
Недоношені новонароджені 0,65-1,5 г/л
Доношені новонароджені 0,2-1,7 г/л
Лейкоцити
Недоношені новонароджені 0-25/мм3 (57% нейтрофіли)
Доношені новонароджені 0-22/ мм3 (61% нейтрофіли)
Додаток 3
Нейтрофільні індекси (норма, в мм³)
| Показник | Після народження | 12 год. | 24 год. | 48 год. | 72 год. | >120 год. |
| Абсолютне число нейтрофілів | 1800-5400 | 7800-14400 | 7200-12600 | 4200-9000 | 1800-7000 | 1800-5400 |
| I:Т індекс | <0,16 | <0,16 | <0,13 | <0,13 | <0,13 | <0,12 |
Дата добавления: 2015-10-29; просмотров: 191 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Сепсис новонародженого, викликаний стрептококом, група В | | | БЕСПЛАТНОЕ ТАКСИ |