
Читайте также:
|
18. Искомое устройство может представлять собой включенные в разрыв электрической цепи подпружиненные контакты, соединению которых мешает кусочек сахара. После приводнения буя сахар растворяется, контакты соединяются и буй начинает функционировать.
19. При работе аккумуляторов выделяется водород, его улавливают и соединяют с кислородом воздуха - образуется вода, которая стекает в аккумулятор. В аккумулятор, разработанный в Японии, можно 5 лет не доливать дистиллированную воду (“Красноярский рабочий”, 23. 12. 83, с. 3).
20. Использовать бумажный или пленочный актинометр в виде плоскости, приклеенной к дужке очков или браслету часов.
21. Нет ответа.
22. Поскольку удаление частиц сажи из бумажной массы затруднительно, следует заменить красящее вещество типографской краски на такое, которое удалить легко. Например, использовать в качестве красителей вещества легко смываемые органическими растворителями или специальными водными растворами. Наконец, печатать изображения органическими красителями, многие из которых легко разрушаются хлором.
Возможно применение и статического эффекта - использовать наборы букв и символов на электретной полимерной пленке (заявка № 3686946/12 (000031) от 2. 01. 84).
23. Кислород необходимый для горения можно подвести к корням в химически связанном виде. Согласно старинному рецепту, опубликованному в приложении к журналу “Живописное обозрение” (1895 г.) в центральной части пня сверлят отверстие диаметром 1-1,5 вершка (вершок 44,5 мм) и глубиной 10-12 вершков. В это отверстие набивают 10 - 15 злотников (злотник равен 4,3 г.) мелко истолчённой селитры (вероятно, нитрата калия) и доливают водой, после чего плотно заколачивают деревянной пробкой. В таком виде всё оставляют до весны. За это время нитрат калия распространяется по корневой системе. Весной втулку выколачивают, наполняют отверстие керосином и поджигают. Пропитанные нитратом калия ствол и корень сгорают до тла, не оставив ничего, кроме золы [Наука и жизнь, 1978, №9. -С.137]. Кстати, американская фирма “Спенсер Гифтс” предлагает химический препарат для корчевания пней имеющий сходные правила применения. Правда время ожидания гораздо меньше, чем в старинном способе, поэтому и состав препарата, по видимому, иной (фирма держит его в секрете) [Препарат для корчевки пней. Наука и жизнь, 1978, №5. -С.137]. Однако, скорее всего, он реализует тот же принцип и отличается лишь использованием другого кислородсодержащего вещества.
24. Перемещать уровень травящего раствора относительно алюминиевой заготовки можно с помощью водорода, выделяющегося в ходе химической реакции:
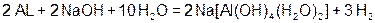
Для этого лист помещают в газовый колокол, заполненный травильным раствором и погружённый в него открытым концом. По мере прохож-дения процесса раствор вытесняется выделяющимся водородом и его уровень движется относительно листа, движется тем быстрее, интенсивнее идёт травление. Таким образом автоматически учитывается изменяющаяся концентрация щелочи. Устройство для травления с газовым колоколом признано изобретением: А. Калабин, а. с. СССР №1216251 [А. Калабин. Технология в расчёте на хозяина. Изобретатель и рационализатор, 1990, №11. -С.9-11 ].
25. Химический эффект, который не учёл Мамед, состоит в уменьшении объёма водно-спиртового раствора по сравнению с суммой объёмов исходных воды и спирта.Рассчитаем объём раствора, который должен был получиться в результате смешения.

Начнем с вычисления массы смеси. Очевидно она равна сумме масс спирта и воды. Поскольку в продажу обычно поступает 96%-ный спирт, имеющий при 200С плотность 0,801 г/см3, а плотность воды при этой температуре равна 0, 998 г/см3, масса смеси составит:
v(см.) = 1000 л × 0,801 кг/л + 1500 л × 0,998 кг/л = 2298 кг
Для нахождения по справочным таблицам плотности водно-спиртовой смеси, необходимо предварительно рассчитать массовую долю в ней этанола:

Согласно справочным данным плотность такой смеси 0,947 г /см3. Вычислим теперь объём этой смеси:
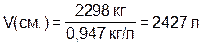
Подсчитаем разницу между суммой объёмов спирта и воды и объёмом полученной водно-спиртовой смеси:
(1000 л + 1500 л) - 2427 л = 73 л или, соответственно, 146 полулитровых бутылок! Да, очень полезно иметь элементарные химические знания и уметь их применять, впрочем как и соблюдать юридические законы.
26. Налить в фарфоровую чашку немного масла и осторожно нагревать его до температуры 70-800С. Над его поверхностью поместить ватный тампон, припудренный веществом, способным изменять окраску при взаимодействии с водяными парами. Изменение окраски сигнализирует о наличии в масле воды.
В качестве индикатора водяных паров можно использовать безводные сульфат меди или хлорид кобальта. Простое решение этой задачи предложено российским изобретателем Ю. Т. Судаковым (а. с. №139866, он предложил использовать ватный тампон, припудренный перманганатом калия. Пары воды, частично конденсируются на тампоне, образующаяся вода растворяет перманганат калия и он окрашивает тампон в малиновый цвет [Г.В. Лисичкин, В.И. Бетанели Химики изобретают. М.: Просвещение, 1990. С.104].
27. Американские специалисты использовали в качестве индикатора бытовых отходов кофеин. Действительно, это вещество является обязательным ингридиентом большинства любимых человеком напитков, будь то кока-кола, чай или кофе... Выяснилось, что кофеин очень устойчив в природных условиях и легко минует очистные сооружения.
Сравнивая содержание кофеина с содержанием других соединений, встречающихся как в бытовых, так и в промышленных отходах оказалось возможным определить какая часть загрязнений в конкретном районе образуется за счёт бытовых отходов, а какая за счёт стоков с заводов и ферм [На хвосте у кофеина. Поиск, 1994, №33-34. -С.15].
28. То, что медь и алюминий не горят в атмосфере кислородасвязано с образованием на их поверхностях плотных нелетучих плёнок оксидов, препятствующих дальнейшему проникновению кислорода к металлу. В то же время, хлориды меди и алюминия легко летучи, поэтому они не защищают поверхность этих металлов. В результате медь и алюминий легко загораются в атмосфере хлора.
Поэтому, чтобы разрезать медную или алюминиевую пластину достаточно нагреть ее традиционным способом (кислородно-ацетиленовым пламенем), после чего на место разогрева направить тонкую струю хлора. В месте контакта струи хлора с металлом образуется разрез.
29. Установку заполняют хлороводородом. После окончания заполнения зажимами пережимают резиновые трубки на входе и выходе из установки. На место источника хлороводородаподсоединяют грушу от пульвериза-тора, а к выходной трубке - кусочек стеклянной трубки, который опускают в сосуд с водой. Убирают зажимы и воздухом вытесняют хлороводород в воду.
Оттитровывают полученный раствор раствором едкого натра известной концентрации:
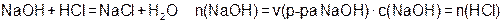
где n(NaOH) и n(HCl), соответственно, количества вещества едкого натра и хлороводорода,
v(ра-ра NaOH) - объём раствора едкого натра и c(NaOH) - концентрация едкого натра в растворе.
При нормальных условиях объём хлороводородасоставит:
 Для приведения этого объёма к комнатным условиям можно воспользоваться объединённым законом газового состояния:
Для приведения этого объёма к комнатным условиям можно воспользоваться объединённым законом газового состояния:

где p0 - нормальное атмосферное давление, 1, 013 × 105 Па,
v0 - вычисленный выше объём газа при нормальных условиях, м3,
Т0 - нормальная температура, 273,14 К,
p1 - давление в условиях опыта, Па,
Т1 - температура в условиях опыта, К.
* Молярные объёмы газов при нормальных условиях близки к величине 22,4×10-3 м3/моль, но несколько отличаются для разных газов, для хлороводорода22,253×10-3 м3/моль[ Общая химия: Учебник / Под ред. Е.М. Соколовской и Л.С. Гузея. -М.: Изд-во Моск. Ун-та, 1989. С.42].
30. Для количественного определения воды в нефтепродуктах можно
использовать химический реагент, не взаимодействующий с нефтепродуктами, но образующий газ при взаимодействии с водой. Объём выделившегося газа можно измерить с большой точностью, а по нему рассчитать концентрацию в нефтепродуктах воды (техника расчёта аналогична предложенной в решении предыдущей задачи).
Группа российских изобретателей предложила использовать для этой цели гидрид кальция:

[ Г.В.Лисичкин, В.И.Бетанели Химики изобретают. -М. "Просвещение", 1990 г. С. 14;64, Лидерман И.С. и др. А. с. №197268].
Однако определение, хотя и менее точное (почему?), можно провести и с металлическим кальцием:
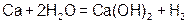
31. Говоря о взрывной штамповке не обязательно предполагать использование энергии обычных твердых взрывчатых веществ, широко применяемых в военном или горном деле. Но ведь взрывчатыми свойствами обладают и газовые смеси, например гремучий газ (смесь водородаи кислорода). Получают гремучий газ прямо в штампе в полиэтиленовом пакете электролизом слабого раствора фосфорной кислоты. После того, как накопится расчётное количество смеси, её подрывают электрической искрой. Авторы изобретения - немецкие инженеры утверждают, что поверхность отштампованных таким образом деталей получается исключительно гладкой и чистой, немаловажно и то, что единственным продуктом взрыва являются водяные пары [ И.И. Эльшанский. Законы природы служат людям. -М.: Просвещение, 1978. -С.141-142].
32. Для проведения откачивания воды без использования насосов можно использовать хорошую растворимость в неё некоторых газов. Например, при 20оС один объём воды растворяет около семисот объёмов аммиака. Поэтому, если наполнить аммиаком бочку и соединить её шлангом с содержащей воду ёмкостью, вода перетечёт в бочку быстро растворив наполнявший её газ. На этом принципе основан широко известный химический демонстрационный эксперимент “Аммиачный фонтан” [Ф.П. Платонов. Лекционные опыты и демонстрации по общей и неорганической химии. -М.: Высш. школа, 1976. -С.81].
Дата добавления: 2015-10-29; просмотров: 116 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Химические эффекты | | | Химические эффекты в электрохимических системах |