
Читайте также:
|
Вступ
Молекулярна фізика¾ наука, що вивчає фізичні властивості та агрегатні стани речовини в залежності від її молекулярної будови, сил взаємодії між структурними частинками - атомами чи молекулами та характеру теплового руху цих частинок. Молекули складаються з атомів. У складі атомів є однакове число електронів і протонів, та нейтрони. Протони та нейтрони утворюють ядро атома. Іонявляє собою заряджений атом.
На малих відстанях між частинками речовини (r~10-9 м) виникає сила притягання  , апри ще менших відстанях виникає сила відштовхування
, апри ще менших відстанях виникає сила відштовхування 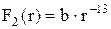 . Ці сили прикладені до частинки, лежать на одній прямій і протилежно направлені. На відстані
. Ці сили прикладені до частинки, лежать на одній прямій і протилежно направлені. На відстані  рівнодійна сил
рівнодійна сил 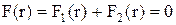 і точка з координатою
і точка з координатою  є точкою рівноваги. При малих відхиленнях від положення рівноваги, рівнодійна сила лінійно залежить від г і може створювати коливальний рух. На Mал.49 наведена залежність рівнодійної сили в залежності від відстані між частинками.
є точкою рівноваги. При малих відхиленнях від положення рівноваги, рівнодійна сила лінійно залежить від г і може створювати коливальний рух. На Mал.49 наведена залежність рівнодійної сили в залежності від відстані між частинками.
 Велике число частинок речовини досліджується статистичним методом. Статистичний метод - метод, що вивчає властивості макроскопічних систем на підставі ймовірнісного та статистичного аналізу закономірностей теплового руху великого числа мікрочастинок, що складають ці системи. За допомогою молекулярно-кінетичної теорії визначаються такі властивості термодинамічних систем
Велике число частинок речовини досліджується статистичним методом. Статистичний метод - метод, що вивчає властивості макроскопічних систем на підставі ймовірнісного та статистичного аналізу закономірностей теплового руху великого числа мікрочастинок, що складають ці системи. За допомогою молекулярно-кінетичної теорії визначаються такі властивості термодинамічних систем
· тиск,
· температура,
· енергія,
· теплоємність,
· явища переносу та інше.
В основі молекулярно-кінетичної теоріїлежать три положення:
* усі фізичні тіла складаються з великого числа частинок ¾ молекул, атомів або іонів, розміри яких складають  ,
,
* частинки речовини постійно знаходяться в тепловому хаотичному русі, а їх середня кінетична енергія визначає температуру тіла,
* між частинками речовини діють сили взаємодії, які, в залежності від відстані між частинками, будуть силами тяжіння або силами відштовхування.
6.2. Імовірністьта флуктуації
Наведемо деякі визначення поняття ймовірності.
1. Імовірність wі деякого і-го стану системи визначається границею відношення часу tі, на протязі якого система знаходиться в даному стані, до повного часу Т спостереження за системою при необмеженому збільшенні Т
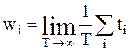 . (1)
. (1)
2. Якщо фізична величина А при N вимірюваннях мала Ni число значень Аі, то ймовірність wi того, що величина А має значення Аі дорівнює границі відношення Ni/N при необмеженому зростанні N і вона співпадає з імовірністю wі і - го стану системи
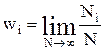 . (2)
. (2)
3. Імовірність dw(A) того, що фізична величина має значення в інтервалі (A; A + dA) пропорційна dA
dw(A) = f(A)dA, (3)
де f(A) - називається густиною ймовірності або функцією розподілу ймовірності.
Умова нормування ймовірностідля дискретних станів
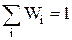 (4)
(4)
¾ сума ймовірності по всім можливим станам є ймовірність достовірної величини і вона дорівнює 1, а для неперервної зміни стану сума замінюється інтегралом
 (5)
(5)
¾ сума ймовірностей для всіх елементарних значень параметра стану А є ймовірність достовірної величини і дорівнює 1.
Середнє статистичне значеннявеличини А позначається  і визначається для дискретних станів так
і визначається для дискретних станів так
 , (6)
, (6)
а для неперервної зміни величини А як
 ,
,
де сума й інтеграл беруться по всім можливим станам системи.
Флуктуації ¾ це випадкові відхилення термодинамічних параметрів від рівноважних значень. Якщо термодинамічна система складається з невеликого числа частинок, то розподіл частинок, випадково відхиляючись від рівноважного, може суттєво змінювати величини термодинамічних параметрів. Для кількісної оцінки флуктуації деякої величини А використовують квадратичну флуктуацію, яку ще називають дисперсією s  . Дисперсія є середнє значення квадрата відхилення А від її середнього значення:
. Дисперсія є середнє значення квадрата відхилення А від її середнього значення:
 .
.
Величина  називається абсолютною флуктуацією, а
називається абсолютною флуктуацією, а 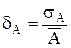 ¾ відносною.
¾ відносною.
Природа флуктуацій термодинамічних величин визначається хаотичним тепловим рухом структурних частинок середовища. Чим більше число N цих частинок, тим менший вплив їх флуктуацій на значення термодинамічних величин. Доведено, що для хімічно однорідного ідеального газу, при сталому об'ємі, флуктуації густини r, тиску Р та температури Т обернено пропорційні кореню з числа частинок газу
 .
.
Звідси видно, що для середовища з великим числом частинок флуктуаціями термодинамічних величин можна нехтувати.
Ідеальний газта його характеристики
Фізична модель ідеального газу передбачає, що
· в ньому відсутні сили притягання між частинками на відстані,
· власним об'ємом частинок газу, порівняно з наданим йому об'ємом, можна знехтувати,
· співударяння між частинками центральні й пружні.
· частинки здійснюють хаотичний тепловий рух, який відповідає рівно ймовірному напрямкові руху частинок по всім виділеним напрямкам. Наприклад, в системі координат XYZ є 6 напрямків руху і тому в напрямкові + ОХ, як і в інших напрямках, із N частинок буде рухатися 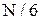 частинок.
частинок.
Молекула¾ найменша стійка частинка речовини, яка ще несе в собі її хімічні властивості.
Молекула складається з атомів хімічних елементів, наприклад, молекула кисню ¾  , води ¾
, води ¾  , азоту ¾
, азоту ¾  .
.
Атом- найменша частинка хімічного елемента, яка є носієм його хімічних властивостей, наприклад, кисень ¾ О, водень ¾ Н, азот ¾ N.
Атомна одиниця маси (аом) ¾  частка маси атома стійкого ізотопу вуглецю
частка маси атома стійкого ізотопу вуглецю  і
і
 ,
,
яка є мірою мас атомів та молекул.
Атомна (молекулярна) маса А(М) ¾ масаатома (молекули) m виражена в атомних одиницях маси. Їх маса в системі СІ
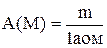
Наприклад, атомна маса водню ¾ А(Н)=1, молекулярна маса молекули водню ¾ М(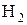 )=2, А(N)=14, M(CO)=20, М(
)=2, А(N)=14, M(CO)=20, М(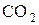 )=28, а масу молекули
)=28, а масу молекули 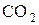 можна обчислити через молярну масу у такий спосіб
можна обчислити через молярну масу у такий спосіб
 .
.
Моль ¾ кількість речовини, що містить у собі число Авогадро  структурних одиниць: атомів (простий хімічний елемент) або молекул (складний хімічний елемент).
структурних одиниць: атомів (простий хімічний елемент) або молекул (складний хімічний елемент).
Маса моляречовини m вимірюється в кг і її можна обчислити через атомну А чи молекулярну М маси так
 .
.
Кількість моліву речовині позначається літерою n і вона дорівнює n=m/m.
Універсальна (молярна) газова стала  .
.
Стала Больцмана  . Величини k, NA, та R зв'язані співвідношенням
. Величини k, NA, та R зв'язані співвідношенням  .
.
Температура
Температура характеризує ступінь нагрітості тіла і є мірою хаотичного руху структурних частинок речовини. Шкали температури визначають температурою кипіння tk води та температурою плавлення t0 льоду при нормальному атмосферному тиску, який можна визначити через тиск стовпа ртуті висотою 760 мм

1).Шкала Цельсія:
 .
.
Дата добавления: 2015-10-28; просмотров: 117 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Выбор производственной технологии. Техническая и экономическая эффективность | | | Шкала Фаренгейта |