
Реакции гидрогенолиза, как и реакции гидрокрекинга, приводят к превращению парафинов в подобные же, но более низкомолекулярные углеводороды. Однако, если реакцию гидрогенолиза катализируют металлические центры катализатора ряформинга, то расщепление углеводородов при гидрокрекинге происходит на кислотных центрах.
При гидрогенолизе может происходить разрыв любых С-С связей в молекулах гексанов. Содержание метана в продуктах реакции значительно возрастает с увеличением степени разветвления изомеров гексана, а следовательно с увеличением числа метальных групп. Очевидно, в этой реакции значительную роль играет разрыв связей С-С, расположенных на концах углеродных цепей гексанов.
Схема гидрогенолиза этана может быть представлена следующим образом:
С2Н5 С2Н5адс + Надс С2НХадс + аН2
C2HХ С фрагменты (под воздействием водорода) СН4
Адсорбция атомов углерода на соседних металлических центрах сопровождается разрывом связей С-Н. Дальнейшая дегидрогенизация атомов углерода приводит к образованию кратных связей С-С и в конечном счете их разрыв. Образующиеся фрагменты подвергаются гидрированию в метан. Возможно, при гидрогенолизе более высокомолекулярных парафинов образуются несколько иные промежуточные соединения, например типа 1,1,3-диадсорбированных соединений:
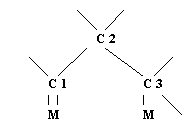
В этом промежуточном соединении может происходить разрыв связей С2-С3, но значительно более предпочтителен разрыв связи C1-С3
При справедливости такого механизма может происходить зауглероживание металлических центров платиновых катализаторов риформинга, что и подтверждается практикой.
При реакциях гидрокрекинга изомерных гексанов метан образуется в весьма малых количествах, и, следовательно, периферийные связи С-С молекул почти не расщепляются. Например, в случае 2,3-диметилбутана - гидрокрекинг этого углеводорода приводит в основном к получению пропана, при гидрогенолизе же образуется главным образом метан Хотя реакции гидрогенолиза играют весьма ограниченную роль в кат.риформинге, все же они идут, особенно в жестких условиях процесса.
Гидрокрекинг протекает в данном случае по бифункциональному механизму:
1) дегидрирование н-парафина в н-олефин на металлическом центре катализатора;
2) адсорбция н-олефина на кислотных центрах катализатора с образованием вторичного карбкатаона;
3) превращение вторичного в более стабильный третичный, либо крекинг с образованием меньшего иона карбония и олефина;
4) изомеризация н-олефина в изоолефин;
5) гидрирование образовавшихся олефинов (С3, С4) на металлических центрах катализатора в соответствующие парафины.
Подтверждением того, что процесс гидрокрекинга на катализаторах риформинга представляет собой бифункциональный катализ, является увеличение его скорости с повышением кислотности катализатора за счет галогенов. Поскольку продукты гидрокрекинга - предельные углеводороды, дезактивация катализаторов происходит значительно медленнее, чем при кат.крекинге. В соответствии с механизмом, метан и этан могут образовываться лишь в небольших количествах.
ОТНОСИТЕЛЬНЫЕ СКОРОСТИ РЕАКЦИЙ КАТАЛИТИЧЕСКОГО РИФОРМИНГА
И ИХ РОЛЬ В ПРОЦЕССЕ
Химия каталитического риформинга предопределяется свойствами применяемых катализаторов:
1) наличием у катализаторов двух функций - металлической и кислотной,
2) независимостью действия этих функций.
Ряд важнейших реакций каталитического риформинга протекает по бифункциональному механизму, в соответствии с которым отдельные стадии одной и той же реакции идут на металлических или кислотные центрах. Металл катализирует реакции дегидрирования парафинов а олефины, циклопарафинов в циклоолефины и шестичленных нафтенов в ароматические углеводороды. Непредельные углеводороды (продукты изомеризации и гидрокрекинга), мигрирующие с кислотных центров на металлические, подвергаются на них гидрированию.
На кислотной функции, осуществляемой носителем, происходит изомеризации олефинов, их циклизация и гидрокрекинг, а также превращение пятичленных циклоолефинов в шестичленные. Все эти реакции протекают по карбкатионному механизму. Таким образом олефины и циклоолефины являются важнейшими промежуточными продуктами реакции.
Согласно схеме реакций риформинга, реакции, представленные параллельно оси абсцисс, протекают на кислотных центрах, а изображенные параллельно оси ординат - на металлических центрах.
Рис. 6. Схема реакций каталитического риформинга
Схема достаточно хорошо выражает ход бифункциональных реакций риформинга, однако она не учитывает в полной мере независимость действия металлической и кислотной функций катализатора и, следовательно возможность протекания всех стадий одной и той же реакции на металлических или кислотных центрах. Такое исключение делается только для реакции дегидрирования шестичленных нафтенов, которая полностью протекает на металлических центрах. Однако реакциям дегидродроциклизации парафинов проходит не только по бифункциональному механизму, но и монофункционально - на металле. Гидрогенолиз парафинов также протекает на металлических центрах. С другой стороны, кислотная функция катализирует размыкание кольца пятичленных нафтенов. Должны быть приняты во внимание также реакции изомеризации и гидродеалкилирования ароматических углеводородов, имеющих немаловажное значение.
С наибольшей скоростью протекают реакции, дегидрирования шестичленных нафтенов в ароматические углеводороды, что приводит к быстрому установлению равновесия. Реакции изомеризации пятичленных нафтенов в шестичленные, а также парафинов проходят тоже с достаточно большими скоростями. К числу наиболее медленно протекающих реакций относятся реакции дегидроциклизации парафинов. Основной путь повышения как скорости, так и селективности реакций дегидроциклизации заключается в снижении давления.
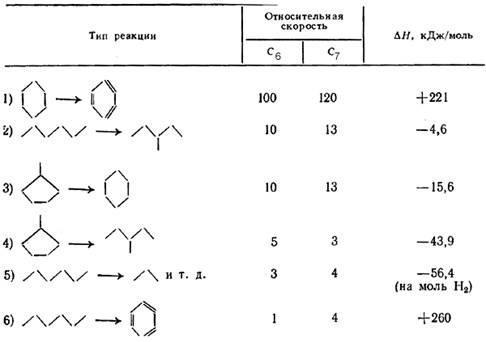
Данные об относительных скоростях и тепловых эффектах реакций риформинга приведены в таблице.
Таблица 3. Относительные скорости и тепловые эффекты реакций каталитического риформинга
КАТАЛИЗАТОРЫ РИФОРМИНГА
Алюмомолибденовый катализатор (МоО3/Al2O3) был первым катализатором риформинга, нашедшим промышленное применение. Попытки использования других оксидных катализаторов (Cr2O3/Al2O3, CoO-MoO3/Al2O3) к успеху не привели.
Алюмомолибденовый катализатор, как и современные катализаторы риформинга, катализирует реакции-ароматизации, изомеризации и гидрокрекинга углеводородов. Однако селективность его в реакциях ароматизации, особенно парафинов, значительно ниже, а скорость закоксовывания намного больше. Тем не менее эти не явилось препятствием для промышленного использования во время второй мировой войны риформинга на алюмомолибденовом катализаторе, так как процесс служил для производства толуола и компонентов авиационных бензинов.
Были проведены обширные исследования, в которых было не только изучено каталитическое действие платины на разные углеводороды, но и показана практическая ее ценность как ароматизующего катализатора. Однако только в конце 40-х годов, когда возникла потребность в экономичном процессе каталитического риформинга для улучшения качества автомобильных бензинов, стали впервые применять более эффективный катализатор - платиновый. На протяжении последующих десяти лет платиновые катализаторы вытеснили оксидные, а широкие исследования привели к созданию разных их модификаций для процесса каталитического риформинга.
Дороговизна платины предопределила малое ее содержание в промышленных катализаторах риформинга, а следовательно, необходимость весьма эффективного ее использования. Этому способствовало также применение в качестве носителя оксида алюминия, который давно был известен как лучший носитель для катализаторов ароматизации. Важно было превратить алюмоплатиновый катализатор ароматизации в бифункциональный катализатор риформинга, на котором протекал бы весь комплекс реакций, рассмотренных в предыдущей главе. Для этого следовало придать носителю необходимые кислотные свойства, что было достигнуто путем промотирования оксида алюминия галогенами (фтором, хлором).
На первом этапе промышленного осуществления процесса предпочитали работать на фторированном алюмоплатиновом катализаторе.
При применявшейся технологии концентрация водяных паров в зоне катализа была велика, а потому для снижения потерь галогена (в результате отщепления от катализатора) целесообразнее было применять фторированный катализатор поскольку фтор прочно связан с катализатором.
Дальнейшее совершенствование технологии каталитического риформинга, в частности удаление из сырья каталитических ядов и его обезвоживание, позволили перейти к использованию более эффективных алюмоплатиновых катализаторов, промотированных хлором. Преимущество хлорированных катализаторов - возможность регулирования содержания хлора в катализаторах, а следовательно, и уровня их кислотности, непосредственно в условиях эксплуатации
Последнее поколение катализаторов риформинга отличается тем, что наряду с платиной, содержат один или несколько других металлов. Для таких катализаторов характерна высокая стабильность в условиях реакционного периода, что в конечном счете обеспечивает возможность получения более высоких выходов как высокооктановых бензинов риформинга, так и ароматических углеводородов.
Дата добавления: 2015-10-26; просмотров: 256 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Реакции дегидроциклизации | | | Working Backwards to Fill the Drug Pipeline |