
Читайте также:
|
Рассмотрим, какие ещё упорядоченные системы спонтанно формируются в мезомире – мире большого скопления молекул при достаточном плотном их расположении (конденсированном состоянии вещества).
Это состояние соответствует расстоянию между молекулами, при котором существенны электромагнитные силы, т.е. не более, чем 10-6 м.
Как правило, главной причиной, вынуждающей молекулы сблизится на такое расстояние, является гравитационное взаимодействие. В частности, на Земле конденсированное состояние вещества обусловлено силой тяжести – силой гравитационного притяжения Земли.
Сблизившись на такое расстояние, молекулы начинают взаимодействовать электромагнитными силами друг с другом. Это взаимодействие носит сложный характер [16,45 ], так как обусловлено подвижностью электронных оболочек молекул. Это приводит к формированию более упорядоченных, чем газ, агрегатных состояний – жидкому и твердому.
Переход от хаотического (газообразного) состояния к жидкому сопровождается уменьшением энтропии на величину
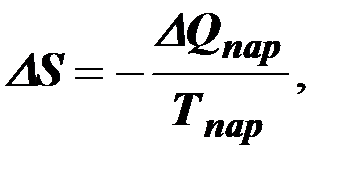
где ΔQпар и Тпар – теплота и температура парообразования (конденсации). Внешне бόльший порядок жидкости по сравнению с газом выражается в четко обозначенной границе, отделяющей объём этой жидкости от других объектов. Сама граница может изменять свою конфигурацию, но величина объема при этом не меняется.
Переход от жидкого состояния к твердому приводит к ещё большей упорядоченности, так как граница отвердевшего объекта не меняется. При этом энтропия уменьшается на величину
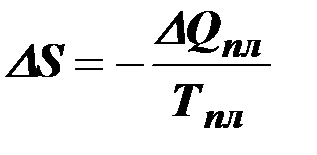
где ΔQпл и Тпл – теплота и температура плавления (кристаллизации).
Порядок твердого тела характеризуется двумя факторами: 1) неизменностью геометрической конфигурации границы (естественно, при отсутствии внешнего воздействия), 2) неизменностью расстояний между молекулами (кристаллическая структура).
Очень важным фактором увеличения упорядоченности, связанным с фазовыми переходами от газа к жидкости, и от жидкости к твердому телу, является уменьшение объема вещества – увеличение его плотности. Как было указано выше (§2.2), увеличение плотности вещества (количества молекул в единице объема) свидетельствует о количественном увеличении порядка, так как уровень неопределённости расположения частицы в меньшем объеме ниже, чем в большем.
Тепловая энергия, выделяемая при конденсации газа и кристаллизации жидкости, приводит к нагреву окружающих объектов, т.е. к повышению их энтропии. Сама по себе эта энергия берется за счет уменьшения потенциальной энергии электромагнитного взаимодействия молекул преобразуемого вещества. Следовательно, формирование упорядоченных агрегатных состояний вещества является следствием двух перечисленных в §2.1 тенденций – повышения энтропии и понижения потенциальной энергии.
Кроме перечисленных трех агрегатных состояний, конденсированное вещество может находится еще в нескольких видах. Перечислим некоторые из них.
Жидкие кристаллы: Жидкости, образованные веществом с длинными молекулами, содержащими несколько десятков атомов. Хотя поверхность объектов, образованных жидкими кристаллами, легко видоизменяется под действием внешних факторов, сами молекулы расположены и двигаются друг относительно друга не хаотически, а по ограниченному числу траектории. Это обстоятельство, во-первых, создает анизотропные свойства вещества. (Например, неодинаковый коэффициент преломления при прохождении электромагнитной волны под разными углами). Во-вторых, эта анизотропность может видоизменяться внешними полями.
Гели: псевдорастворы некоторых твердых веществ также с длинными молекулами, в которых эти молекулы притягивают к себе молекулы растворителя. Внешне такие гели образуют полужидкость, полутвердое тело (например, желе). Чаще всего из вещества в таком состоянии состоят живые организмы. Протоплазма клеток состоит, как правило, из 70÷90% воды и 30-10% белка (полимеров аминокислот). Молекулы белка представляют собой длинную нить, свёрнутую в клубок (глобулу), окружённый оболочкой, состоящей из молекул воды, притянутых к наружным мономолекулам клубка (см. §6.3).
Плазмы: полужидкое, полугазообразное состояние, состоящее из “обломков” молекул – ионов. Например: пламя, электрическая дуга, молния, искры, Солнце, звезды.
Аморфные вещества: вещества, внешне имеющие главный признак твердого – неизменную границу, но при этом хаотическое (некристаллическое) расположение молекул. Примеры: стекло, бумага, картон, некоторые полимерные материалы.
Особыми формами конденсированного состояния вещества являются растворы, сплавы, взвеси, коллоиды, химические соединения. Наружная часть атмосферы Земли окружена магнитосферой [17,26,45 ] – еще одной разновидностью конденсированного состояния.
В космическом пространстве обнаружены объекты с весьма своеобразной формой конденсации – нейтронные звезды, черные дыры.
Несмотря на всё разнообразие конденсированных состояний вещества, каждое из них является более упорядоченным, чем состояние идеального газа. Причем механизм его формирования также определяется сформулированными в предыдущей главе необратимыми тенденциями.
Дата добавления: 2015-08-27; просмотров: 315 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Спонтанное возникновение порядка на молекулярном уровне | | | Неравновесные системы |