
Читайте также:
|
Прикладом двокомпонентних систем є ненасичені розчини, що скла-даються з розчинника і однієї розчиненої речовини, розплаву двох солей, сплаву з двох металів.
Розрахуємо можливе число ступенів вільності для двокомпонентних систем (Κ = 2):
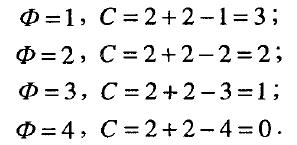
Звідси можна зробити висновок, що найбільше число ступенів вільно-сті для двокомпонентних систем рівне трьом при Ф = 1 (температура, тиск і концентрація одного з компонентів), а найбільше число фаз, що знаходяться в рівновазі - 4 (дві тверді фази одного і другого компонентів, рідка фаза і па-ра). Для побудови діаграми стану двокомпонентної системи потрібно корис-туватись трьома осями координат: температура, тиск, концентрація одного з компонентів.
При дослідженні конденсованих систем, що складаються лише з рід-ких і твердих фаз, тиск практично не впливає на стан рівноваги між фазами. Фазова діаграма спрощується. її будують у координатах "температура – кон-центрація" одного з компонентів. Концентрація другого компоненту є залеж-ною величиною і рівна: С2 = 100% – С1.
Прикладами конденсованих двокомпонентних систем можуть бути сплави двох металів.
Одним із методів вивчення сплавів є термічний аналіз, що ґрунтуєть-ся на визначенні температур фазових перетворень. Наведемо приклади трьох діаграм, побудованих за даними термічного аналізу.
Діаграма стану двокомпонентної системи Ві - Cd
Точка А відповідає температурі плавлення чистого вісмуту, точка В -температурі плавлення чистого кадмію (рис. 4). Крива АЕ характеризує тем-пературу кристалізації вісмуту залежно від вмісту в системі кадмію. Крива
BE характеризує температуру кристалізації кадмію від вмісту в системі віс-муту. У точці Ε кристалізуються обидва метали. Ця точка називається точкою евтектики. Лінія АЕВ - лінія ліквідуса. Лінія DC - лінія солідуса. Розглянутий вид діаграми Ві - Cd утворюють метали, що необмежено розчинні

Дата добавления: 2015-08-17; просмотров: 194 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Однокомпонентні системи | | | Правило фаз Гіббса |