
Читайте также:
|
Кроме оксигенации и выделения СО2, легкие выполняют важную функцию поддержания кислотно-основного гомеостаза. Так называемые ''связанные кислоты" образуются в процессе метаболизма в тканях и непрерывно выводятся почками. ГЗ норме от 40 до 80 ммоль связанных кислот ежедневно выводятся из организма. При метаболических расстройствах различного генеза, таких как повышенное образова-
Рис. 10-6. Кривые диссоциации С()2 для оксигенированной и де-оксикопированной крови. По мере того, как артериальная кровь с Рсоа в 40 мм рт. ст. (точка Л) деоксигенируется, ее связывание с С()2 увеличивается. Смешанная венозная кровь с PcOj, в 47 мм рт. ст. (точка В) песет примерно на 60 мл/л СО2 больше, чем артериальная кровь

гликолем), а также при болезнях почек их способность выводить связанные кислоты может не соответствовать скорости их образования. В этих условиях легкие либо на короткое время, либо длительно компенсируют почечную недостаточность относительно выделения связанных кислот. Такая компенсация сохраняет рН в физиологически приемлемом диапазоне.
Через легкие выводится ежедневно приблизительно 13 000 ммоль угольной кислоты, которая могла бы стать значительной кислотной нагрузкой. Поэтому изменения минутной вентиляции и, особенно, альвеолярной вентиляции (гл. 3) оказывают глубокое воздействие на кислотно-основное равновесие у здоровых и больных людей.
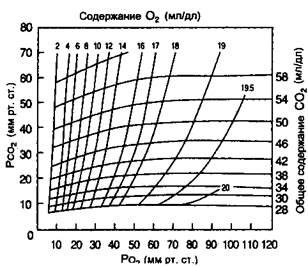
Рис. 10-7. Диаграмма кислород-двуокись углерода. Содержание ()2 и СО2 не зависит прямо пропорционально от их парциального давления в крови
Физиологические буферные системы-система СО2—бикарбонат
Буферные системы организма играют первостепенную роль в поддержании от носительно узкого диапазона рН, в котором протекают ф™ОЛогн™сш?™™ные
1Го"аетТ°кГе ПРОЦ-еССЫ' ГЛаВН°Й 6УФСРНОЙ ^^^^^:МТСО^- карбонат, которая действует во внеклеточной и внутриклеточной жидкостях оога низма. Кроме того, внутриклеточные белки, гемоглобин, белки Га™и составные
Си^^
Система С02-бикарбонат заслуживает особого внимания
сга^^^Т1ПРИС^СПуеТ В большинс™ жидкостей организма и со-ниГя КИ ТР бУФеРныи Резервуар, называемый щелочным резервом орга-
5££S?SKK%^
Н4нсо3-^нгс0з«+сог + н2о. [10.14]
Как отмечалось, превращение Н2СО:, в Н2О и СО2 катализируется сЬеоментпм карбоангидразой. По мере того, как водородные ионы ыраб™^™^™™ болизма, бикарбонатный буфер превращает их в Н.ш'и, наконец в СО*воду HZCO:, является «летучей кислотой", поскольку она образует СО, - газ вьшолимый через легкие. И, наоборот, когда СО2 образуется в пропсе ^очноГмГболи ма, угольная кислота диссоциирует на Н+ и НСО,
рН системы, в которой протекают эти реакции! рассчитывается на основе woe-
=„^-±т^^
Кд=ЩнсОз]
[Н2С03] ' [Ю-15]
Логарифмическая форма уравнения [10-15] может быть записана как:
г, [НС051
logKA=logH+ UlogJ.------Ц
1 J [H2C03] [Ю-16]
Поскольку рН определяется как отрицательный логарифм концентрации иона водорода [Н ], уравнение[10-16] может быть записано как: центРаЧии ™на
[нСОз!
pH = pKA+log7i-------1
Н2С03 [10-17]
Известно, что равновесие между СО2 и Н2СО:) в плазме сдвинуто в сторону СО, на величину фактора, равного 1000 к 1, а количество СО2 пропорционально ГДфи
>«7и"г1ВоТ71ОСТИ (Г °'3 MVVMM рт- СТ' = °-°3 M^M ^ стО «у > равнение [10-17] может быть представлено в виде:
pH = PKA+log 1НС°^1
УО.ОЗхРсо2' [Ю-18]
Величина рКА для буферной системы СО?-бикарбонат равна 6 1 Ноомачыпя концентрация бикарбоната в плазме артериальной крот, 24,nEq" (или
24 ммоль/л), а нормальное РаСО2 — 40 мм рт. ст. Следовательно, нормальное артериальное рН = 6.1 + log[24]: 0.03 х40 или 7.4.
Если концентрация бикарбоната снижается, а РаСО2 остается постоянным, то снижается и рН. Напротив, если концентрация бикарбоната растет, а РаСО2 остается без изменения, то рН повышается. Если же РаСО2 изменяется так, что отношение бикарбоната к (а х РаСО2) остается на уровне 20, то рН сохранит значение 7.4. Подобный анализ уместен при первичных изменениях РаСО2, когда его рост или падение (без сопутствующих изменений концентрации бикарбоната) вызывает соответствующее снижение или повышение рН.
Дата добавления: 2015-08-02; просмотров: 54 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Карбаминовые соединения | | | Диаграмма Давенпорта |