
Читайте также:
|
Цель работы: изучение кинетики гомогенной каталитической реакции на примере разложения пероксида водорода в присутствии 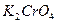 волюмометрическим методом и определение константы скорости и порядка реакции.
волюмометрическим методом и определение константы скорости и порядка реакции.
Разложение водного раствора пероксида водорода по реакции 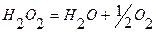 обычных условиях характеризуется невысокой скоростью. Присутствие катализатора ускоряет процесс. Если в качестве катализатора использовать хромат калия, то взаимодействие проходит по реакции
обычных условиях характеризуется невысокой скоростью. Присутствие катализатора ускоряет процесс. Если в качестве катализатора использовать хромат калия, то взаимодействие проходит по реакции
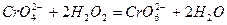 .
.
Каталитическое разложение пероксида водорода является процессом внутримолекулярной рекомбинации атомов кислорода, передаваемых от молекул пероксида водорода катализатору. Общая схема катализа выглядит следующим образом (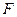 - катализатор):
- катализатор):
I. Передача активных атомов кислорода катализатору
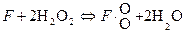 ;
;
II. Рекомбинация атомов кислорода в промежуточном продукте
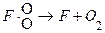 .
.
При этом скорость каталитической реакции выражается уравнением
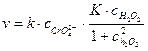 ,
,
где 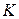 − константа равновесия образования промежуточного продукта
− константа равновесия образования промежуточного продукта 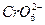 , а
, а 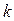 − константа скорости его необратимого разложения.
− константа скорости его необратимого разложения.
Порядок данной реакции зависит от температуры: при 0ºС порядок ниже первого; при 25ºС процесс довольно точно следует первому, а при 50 ºС приближается ко второму порядку.
Приборы и материалы: термостат, установка для изучения каталитической реакции, стеклянная палочка, водяная баня, цилиндр, пипетка на 1 см3 с делениями. Растворы: 0,5 М 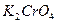 , 30%
, 30% 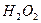 .
.
Дата добавления: 2015-08-10; просмотров: 135 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Экспериментальные и расчетные данные | | | Порядок выполнения работы |