
|
Читайте также: |
Химические процессы всегда сопровождаются выделением или поглощением теплоты. В первом случае реакции называют экзотермическими, во втором – эндотермическими. Количество теплоты, которая выделяется или поглощается в необратимом процессе, называют тепловым эффектом химической реакции (энтальпией), или иначе изохорическим или изобарическим тепловым эффектом химической реакции. Между ними существует такое взаимоотношение:
QР = QV + ∆ ν RT
При условии, что в результате химического процесса число молей газообразных компонентов реакции не изменяется (QР = QV). Если химическая реакция происходит в конденсируемой системе и изменением объема системы можно пренебречь, то величины изохорического или изобарического теплового эффекта также считают одинаковыми.
Уравнения химических реакций, в которых приведены значение их энтальпии и указанное агрегатное состояние реагентов и продуктов реакции, называют термохимическими. Стехиометрические коэффициенты термохимических уравнений могут быть дробными, поскольку они обозначают молярные количества реагирующих веществ.
Таким образом, при обозначении теплового эффекта реакции Q в правой части уравнения его значение для экзотермической реакции положительное, а для эндотермической - отрицательное. То есть, в отличие от общей термодинамики, в термохимии тепловой эффект считают положительным, если теплота поглощается и реакция будет эндотермическая. Если теплота выделяется, - реакция экзотермическая.
Следовательно, изменение энтальпии касается энергетических изменений в системе, а величина теплового эффекта Q - соответствующих изменений в окружающей среде при условии, что Р = const. Чтобы сравнивать между собой тепловые эффекты разных реакций и проводить термохимические расчеты, было введено понятие теплового эффекта при стандартных условиях.
Тепловым эффектом реакции при стандартных условиях (∆Нf0) называют тепловой эффект, измеренный при температуре 298,15 К и давления 101,3 кПа. Его вычисляют по стандартным энтальпиям образования или сгорания компонентов реакции.
Стандартной энтальпией образования (∆Нf0) называют тепловой эффект реакции образования одного моля вещества из элементов или простых веществ при стандартных условиях. Для элементов и простых веществ в стойком агрегатном состоянии ∆Нf0 равняется нулю.
Стандартной энтальпией сгорания ∆Нс0 называют теплоту сгорания в атмосфере кислорода одного моля вещества до самых простых оксидов.
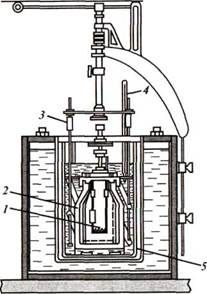
Стандартные энтальпии сгорания веществ определяют в специальных приборах – калориметрах.
Дата добавления: 2015-08-10; просмотров: 45 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ. | | | Законы термохимии |