
Читайте также:
|
ОПЫТЫ
1. Лаборат. способы получения хлора. В четыре пробирки поместить по 1 ст. ложечке крист. KMnO4. K2Cr2O7, MnO2. Во все пробирки долить по 1-2 мл конц. р-ра HCl. Составить уравнения соответствующих реакций. Свойство Cl–, роль Н+в этих опытах.
Получение хлора в больших количествах и свойства хлора в газовой фазе.
|
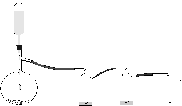
a) Собрать установку для получения газообразного хлора. Наполнить хлором (вытесняя воздух) три глубокие и одну маленькую пробирки.
b) В глубоких пробирках выполнить опыты:
· с сурьмой (всыпать порошок свежеперетертой сурьмы);
· с красным фосфором (внести до дна небольшое количество красного фосфора в ложечке для сжигания) – после ~5сек горения вынуть ложечку из пробирки, пробирку закрыть пробкой, пронаблюдать и сравнить интенсивность горения фосфора в хлоре и на воздухе;
· с парафиновой свечой - усредненный состав С30Н62 (поджечь на воздухе и внести в атмосферу хлора).
В пробирку, оставшуюся после горения фосфора, долить 1-2мл воды. Как ведут себя в контакте с водой разные хлориды фосфора? Встряхнуть пробирку с полученным раствором и по каплям добавить ~1мл раствора AgNO3. В первый момент наблюдать признаки окисления/окрашивания/осаждения (???) ионов Cl-ионами Ag+. Со временем может наблюдаться потемнение осадка, как результат появления мелкодисперсного серебра: 2Ag+ + Н3РО3 + Н2О → 2Ag ↓ + Н3РО4 + 2Н+. Сделайте вывод о количественном соотношении PCl3 и PCl5 в условиях выполненного ранее опыта сгорания фосфора в атмосфере хлора.
c) Маленькую пробирку использовать для опыта с водородом: наполнить точно такую же пробирку водородом из аппарата Киппа, совместить их отверстиями (пробирка с водородом сверху), на несколько секунд перевернуть пробирки, а затем поднести их отверстиями к пламени спиртовки.
Составьте уравнения реакций (в том числе и с кислородом воздуха), сравните их тепловые эффекты (см. признаки взаимодействия), прокомментируйте состав продуктов. Прокомментируйте механизм реакции с водородом. Сделайте обобщающий вывод о физико-химических и химических свойствах хлора, выявленных в этой серии опытов.
Сделайте вывод о свойствах (физико - химических и химических) хлороводорода в газовой фазе (оп. 2с)) и в водном растворе (оп. 1 и 2а)).
Дата добавления: 2015-07-21; просмотров: 36 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| b) Пролог к ликвидации патриаршества. | | | МОРСКАЯ ГОСУДАРСТВЕНАЯ АКАДЕМИЯ |