
Читайте также:
|
С ковалентной связью металлическая сходна тем, что при возникновении этих видов связи валентные электроны переходят в общее пользование атомов. Однако, в случае металлической связи эти электроны связывают все атомы данного куска металла, а в случае с ковалентной – два объединившихся атома.
 С ионной связью металлическая связь сходна наличием ионов. Однако в металлах положительно заряженные ионы удерживаются свободно перемещающимися электронами, а не отрицательно заряженными ионами, как в веществах с ионной связью.
С ионной связью металлическая связь сходна наличием ионов. Однако в металлах положительно заряженные ионы удерживаются свободно перемещающимися электронами, а не отрицательно заряженными ионами, как в веществах с ионной связью.
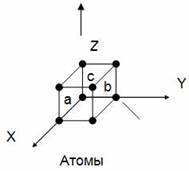
Металлическая связь имеется в металлах, находящихся в жидком и твёрдом состоянии. Твёрдые металлы – вещества кристаллические. Их кристаллические решётки сходны с атомными решётками алмаза, кремния, но в узлах металлических решёток расположены положительно заряженные ионы.
Вследствие притяжения всех свободных электронов всеми положительно заряженными ионами металлическая связь очень прочна. Поэтому для металлов характерны кристаллические решётки с плотной упаковкой ионов, которая 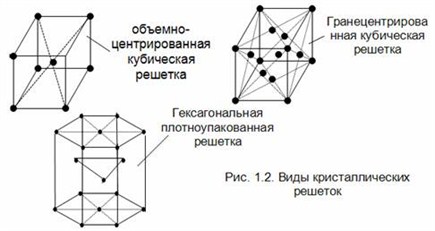 достигается в металлах с решёткой гексагонального типа (цинк, магний и др.) или кубического гранецентрированного (медь, серебро, алюминий и др.). Менее плотной является решётка кубическая объемно-центрированная. Такую решётку при кристаллизации образуют железо, натрий, барий и др.
достигается в металлах с решёткой гексагонального типа (цинк, магний и др.) или кубического гранецентрированного (медь, серебро, алюминий и др.). Менее плотной является решётка кубическая объемно-центрированная. Такую решётку при кристаллизации образуют железо, натрий, барий и др.
Некоторые металлы (например, олово) могут кристаллизоваться в зависимости от температуры с образование решёток то одного, то другого типа.
Если появились вопросы, и Вы хотите более детально остановиться на данном материале, онлайн репетиторывсегда готовы помочь. Для каждого, прошедшего регистрацию на сайте, бесплатное пробное 25-минутное занятие. Занимайтесь бесплатно, выбирайте подходящий тарифный план и получайте квалифицированную помощь по любому предмету школьной программы!
Дата добавления: 2015-07-11; просмотров: 216 | Нарушение авторских прав