
Читайте также:
|
При горении топлива выделяется большое количество теплоты. Количество теплоты, выделяющееся при полном горении единицы топлива, определяет теплоту его сгорания и имеет размерность (кДж/кг или кДж/м3). При окислении водорода и водородсодержащих составляющих топлива образуется водяной пар, который вместе с влагой топлива и воздуха переходит в продукты горения. В зависимости от того, в каком виде находится в дымовых газах водяной пар, различают высшую и низшую теплоту сгорания топлива.
Высшая теплота сгорания топлива 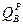 соответствует условию, при котором продукты горения охлаждаются до температуры 20°C, а пары воды конденсируются и конденсат охлаждается до температуры t=20°C, с выделением теплоты парообразования (r=2257кДж/кг) и охлаждения конденсата (q=335,2 кДж/кг). Общее количество теплоты, выделившееся в этом случае, составит 2592,2 кДж/кг. Низшая теплота сгорания топлива
соответствует условию, при котором продукты горения охлаждаются до температуры 20°C, а пары воды конденсируются и конденсат охлаждается до температуры t=20°C, с выделением теплоты парообразования (r=2257кДж/кг) и охлаждения конденсата (q=335,2 кДж/кг). Общее количество теплоты, выделившееся в этом случае, составит 2592,2 кДж/кг. Низшая теплота сгорания топлива 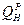 соответствует условию, при котором содержащаяся в продуктах горения влага находится в виде пара при температуре 20°C. При охлаждении 1 кг водяных паров до 20°C возвращается лишь 164 кДж теплоты.
соответствует условию, при котором содержащаяся в продуктах горения влага находится в виде пара при температуре 20°C. При охлаждении 1 кг водяных паров до 20°C возвращается лишь 164 кДж теплоты.
Следовательно, количественное различие между высшей и низшей теплотой горения топлива составит:
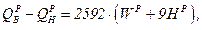 (5)
(5)
где  - содержание в процентах по массе соответственно
- содержание в процентах по массе соответственно
влаги и водорода.
В практических расчетах обычно пользуются величиной QH, поскольку в тепловых устройствах пары воды, содержащиеся в продуктах горения, удаляются из рабочего пространства в газообразном состоянии.
Низшая теплота сгорания газового топлива определяется как сумма тепловых эффектов реакции горения каждого компонента, содержащегося в одном кубическом метре топлива (кДж/м3):
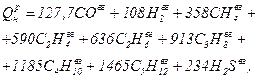 (6)
(6)
где 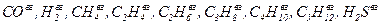 -
-
содержание соответствующих компонентов в газовом топливе, %.
Низшая теплота сгорания рабочей массы жидкого и твердого топлива определяется по формуле Д.И. Менделеева, кДж/кг
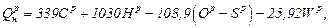 (7)
(7)
где Ср, Нр, Ор, Sр – содержание в процентах по массе соответственно
углерода, водорода, кислорода и серы.
Дата добавления: 2015-10-16; просмотров: 63 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Расчет рабочей массы топлива | | | Определение расхода воздуха |