
|
Читайте также: |
ТЕРМОДИНАМИКА. ФИЗИЧЕСКИЕ ПРОЦЕССЫ В БИОЛОГИЧЕСКИХ МЕМБРАНАХ
Основные понятия термодинамики. Первое и второе начала термодинамики
Термодинамика изучает количественные закономерности превращения энергии в различных процессах (тепловых, механических, электрических и др.), обусловленных тепловым движением молекул. Современная термодинамика связана с рассмотрением большого круга вопросов, представляющих интерес для естественных наук и философии.
Термодинамика построена в основном на двух началах, полученных из многовекового опыта человеческой деятельности. Первое начало описывает количественную и качественную сторону процессов превращения энергии; второе начало позволяет судить о направлении этих процессов.
Термодинамическое состояние любой системы характеризуется тремя параметрами: давлением, объемом, температурой. Они связаны между собой уравнением состояния, которое для идеального газа является уравнением Менделеева-Клапейрона, для реальных газов и жидкостей – уравнение Ван-дер-Ваальса.
Переход системы из одного состояния в другое называется термодинамическим процессом.
Процесс называется обратимым, если возможен обратный переход без изменений в окружающей среде и самой системе.
Термодинамической системой называется макроскопическое тело (или группа тел), которому свойственны процессы, сопровождающееся переходом теплоты в другие виды энергии и обратные процессы.
Если внешние условия неизменны, то через некоторое время термодинамическая система приходит в равновесие.
При любом способе перехода системы из одного состояния в другое изменение внутренней энергии системы будет одинаковым и равным разности между количеством теплоты Q, полученным системой и совершаемой работой А.
 или
или 
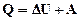
Все количество теплоты, переданное системе идет на изменение ее внутренней энергии и совершение работы (первое начало термодинамики).
 .
.
Если система периодически возвращается в исходное состояние, то ∆U=0 и
 .
.
То есть Совершаемая работа не может быть больше Q и, следовательно, вечный двигатель первого рода невозможен.
Для того, чтобы работа совершалась постоянно механизм должен возвращаться в исходное стояние, для этого необходимо газ охлаждать до начальной температуры, а следовательно часть энергии будет передано окружающей среде. Отсюда следует невозможность построения вечного двигателя второго рода (который всю полученную энергию переводит в работу без потерь)
Второе начало термодинамики: невозможен периодически действующий механизм, который все полученное от нагревателя тепло целиком переводил бы в работу. Часть этого тепла должна быть отдана «холодильнику».
Дата добавления: 2015-10-13; просмотров: 109 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Эмболия | | | Энтропия. Принцип минимума производства энергии |