
Читайте также:
|
Свойства аэрозолей определяются:
- природой веществ дисперсной фазы и дисперсионной среды
- частичной и массовой концентрацией аэрозоля
- размером частиц и распределением частиц по размерам
- формой первичных (неагрегированных) частиц
- структурой аэрозоля
- зарядом частиц.
Для характеристики концентрации аэрозолей, как и других дисперсных систем, используются:
массовая концентрация – масса всех взвешенных частиц в единице объема дисперсной системы:

массовая и объемная доли:
 , где m0 и V0 – общая масса и общий объем дисперсной системы
, где m0 и V0 – общая масса и общий объем дисперсной системы
численная концентрация – число частиц в единице объема дисперсной системы
 , где V0 –общий объем дисперсной системы
, где V0 –общий объем дисперсной системы
Nч – число частиц
Особенности молекулярно-кинетических свойств аэрозолей обусловлены:
· малой концентрацией частиц дисперсной фазы
(например, в 1 см3 гидрозоля золота содержится 1016 частиц, а в таком же объеме аэрозоля золота менее 107 частиц).
· малой вязкостью дисперсионной среды (воздуха), т.е., малым коэффициентом трения (В), возникающего при движении частиц
· малой плотностью дисперсионной среды, следовательно ρчаст» ρгаза
Все это приводит к тому, что движение частиц в аэрозолях происходит значительно интенсивнее, чем в гидрозолях.
1. Броуновское движение
Это непрерывное хаотичное равновероятностное для всех направлений движение частиц, распространяющихся за счет воздействия дисперсионной среды.
Согласно уравнению Эйншнейна, средний квадрат смещения частицы Dх2 за промежуток времени t вдоль оси x равен:

где K – коэффициент сопротивления (сила, действующая на частицу, движущуюся со скоростью 1м/с)
В случае справедливости закона Стокса K=3hd, так что уравнение приобретает вид:

Первые измерения броуновского движения частиц в газах, сделанные Де Бройлем, подтвердили справедливость уравнения Эйншнейна.
2. Диффузия
Это самопроизвольные процесс распространения дисперсионной фазы из области с большей концентрацией а область с меньшей концентрации.
где n – концетнрация частиц в данной плоскости.
По закуну Фика:

где D – коэффициент диффузии.

Тогда, можно выразить коэффициент диффузии в функции размера частицы:
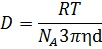
где член  представляет собой подвижность частицы.
представляет собой подвижность частицы.
3. Электрические свойства аэрозолей
До сих пор аэрозольные частицы рассматривались как незаряженные, и пренебрегали действием электрических сил как между самими частицами, так и между частицами и приложенным внешним электрическим полем. В реальности большинство аэродисперсных систем обладает электрическим зарядом, это свойство фактически является универсальным как для технологических, так и для природных атмосферных аэрозолей.
Электрические свойства частиц аэрозоля значительно отличаются от электрических свойств частиц в лиозоле.
1. Большинство аэрозолей несут заряд, который может постоянно перераспределяться между частицами;
2. Внешние электрические поля могут влиять как на величину заряда частиц, так и на характеристики их движения;
3. На частицах аэрозоля не возникает двойной электрический слой, так как из-за низкой диэлектрической проницаемости газовой среды в ней практически не происходит электролитическая диссоциация;
4. Заряд частиц носит случайный характер, и для частиц одной природы и одинакового размера может быть различным как по величине, так и по знаку.
5. В отсутствие специфической адсорбции заряды частиц очень малы и обычно превышают элементарный электрический заряд не более чем в 10 раз.
К основным процессам, приводящим к образованию заряда на частице, относятся прямая ионизация частиц; статическая электризация частиц; столкновения с ионами; ионизация частиц электромагнитным излучением (УФ, рентгеновским или гамма-излучением).
Согласно Смолуховскому, заряд зависит от числа положительных и отрицательных ионов, находящихся в капельке в момент ее отделения от жидкости, т.е. определяется концентрация ионов в жидкости, то есть:
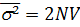
где  - средний квадрат заряда капельки, выраженный через число элементарных
- средний квадрат заряда капельки, выраженный через число элементарных
зарядов
N – концентрация ионов одного знака в жидкости
V – объем капельки
Эта теория была проверена Натансоном в опытах с жидкостями, имеющими очень низкую концентрацию ионов (менее 3×10-9 моль/л), например с трансформаторным маслом. Он нашел, что распределение зарядов вполне симметрично во всей области размеров капелек 0,5 – 2,1 мк.

Но заряд жидкой капли не может достичь предельного значения кроме случая, когда ее размеры очень малы.
На заряд накладывается дополнительное ограничение, известное как предел Рэлея. Сильно заряженная капля будет испаряться до тех пор, пока внешняя сила электрического поля на поверхности капли не превысит внутреннюю силу ее поверхностного натяжения. В этот момент капля разорвется на части, а ее заряд распределится по большей поверхности нескольких более мелких капелек.
Рэлей получил выражение для количества электронов на капле, необходимого для ее разрыва:

где σ – коэффициент поверхностного натяжения
d – диаметр капли
Правильность этой формулы была подтверждена экспериментально
4. Устойчивость
Под устойчивостью системы понимается способность системы сохранять свои свойства, дисперсионный состав, равномерное распределение частиц по объему.
Есть два вида устойчивости:
1. Молекулярно-кинетическая устойчивость – это устойчивость дисперсной системы по отношению к действию силы тяжести. Она препятствует седиментации и определяется наличием броуновского движения, зависит от степени дисперсности частиц, вязкости среды, температуры.
2. Агрегативная устойчивость – это способность системы сохранять свою степень дисперсности.
Аэрозоли являются агрегативно неустойчивыми системами. Устойчивость аэрозолей является лишь кинетической, термодинамические факторы устойчивости отсутствуют.
К нарушению устойчивости аэрозолей приводят следующие процессы:
1. седиментация частиц, которая по причине малой вязкости среды протекает быстрее, чем в гидрозолях;
2. коагуляция частиц, протекающая в газовой среде из-за интенсивного броуновского движения с большой скоростью, которая ещё более возрастает с увеличение концентрации аэрозоля. Ускорению коагуляции способствует повышенная влажность среды;
3. влияние температуры, особенно на устойчивость туманов, так как их равновесное состояние возможно только при условии, когда давление насыщенного пара дисперсных жидких частиц r равно давлению насыщенного пара жидкости, из которой они образованны (r0 ). При r > r0 идет испарение капель, а при r < r0 – конденсация.
а) Испарение
Продолжительность существования аэрозолей ограничивается скоростью испарения отдельных частиц; для данного вещества при постоянной температуре испарение будет происходить с максимальной скоростью в случае, когда окружающий воздух не содержит паров вещества; для вопроса об устойчивость аэрозолей эта максимальная скорость испарения имеет существенное значение.
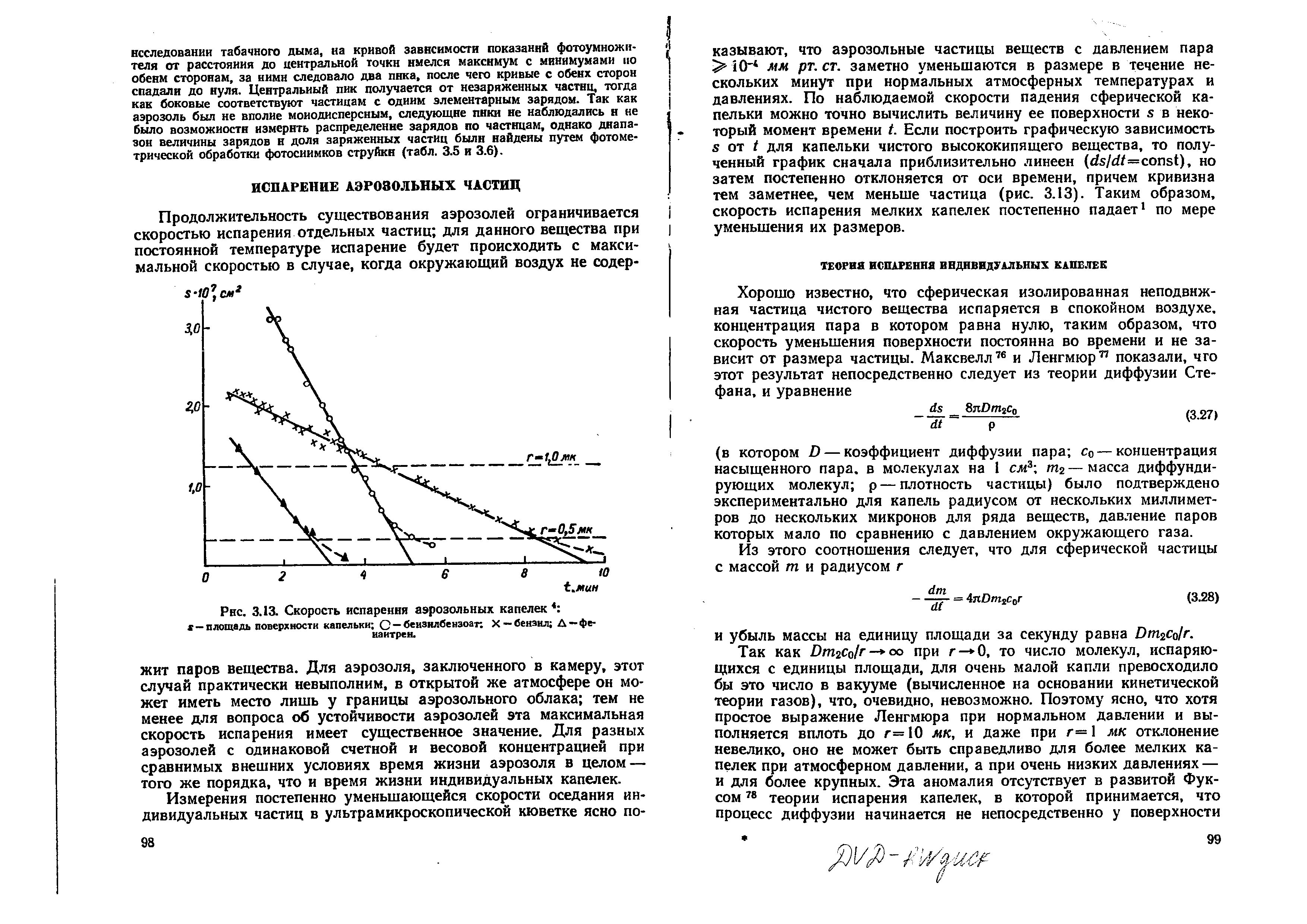
Если построить графическую зависимость площади поверхности s от времени t для капельки чистого высококипящего вещества, то полученный график сначала приблизительно линеен (ds/dt=const), но затем постепенно отклоняется от оси времени. Причем кривизна тем заметнее, чем меньше частица. То есть, скорость испарения мелких капелек постепенно падает по мере уменьшения их размеров.
Расчеты времени полного испарения капелек важны при сравнении устойчивости различных веществ в аэродисперсном состоянии, но полное испарение частиц маловероятно. Наличие нелетучих примесей, присутствовавших в исходном веществе, или возникших уже в дисперсном состоянии в результате окисления или разложения, или приобретенных при столкновении с частицами пыли в воздухе, может замедлять испарение и даже останавливать его.
Поэтому «время полуиспарения» капли, т.е время, в течение которого капля потеряет за счет испарения половину своей первоначальной массы, оказывается более удобным параметром.
б) Коагуляция
Коагуляция – наиболее важный процесс межчастичного взаимодействия в аэрозолях. Ее надо понимать как эффект слипания, агрегирования первичных частиц в процессе их взаимного движения и парных столкновений (тройные столкновения частиц обычно не учитываются как весьма маловероятные).
Слияние жидких капель называется коалесценцией, для твердых частиц часто используется термин агломерация. Оба эффекта в целом можно характеризовать как агрегацию частиц.
В общем случае под коагуляцией понимают уменьшение степени дисперсности частиц (т.е. их укрупнение) при снижении числовой концентрации частиц.
Рассмотрим теорию коагуляции Смолуховского.
Монодисперсный аэрозоль из сферических частиц, которые первоначально были
равномерно распределены в объеме газа. Они испытывают поступательное броуновское движение, которое приводит к их сближению и столкновениям. Каждое парное столкновение частиц приводит к их слипанию.
Рассматривается процесс броуновской диффузии частиц из неограниченного объема газа к одной неподвижной частице – так называемой «поглощающей сфере».
В итоге, решение уравнения Смолуховского имеет вид:

| 
|
Эти уравнения позволяют предсказать изменение числовой концентрации монодисперсных частиц во времени.
Видно, что данный процесс является достаточно медленным, а скорость изменения концентрации частиц сильно зависит от их начальной концентрации.
Зависимость числовой концентрации частиц n от времени для броуновской коагуляции монодисперсного аэрозоля (разные кривые соответствуют различной начальной концентрации частиц)
5. Оптические свойства
Определяются рассеянием светового потока при прохождении через аэрозоль.
Интенсивность излучения I, рассеянного в данном направлении определенным объемом аэрозоля, становится пропорциональной счетной концентрации частиц n и радиусу частиц в некоторой степени p, т.е.:
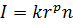
6. Специфические свойства
К особенностям физических свойств аэрозолей, связанным с газообразной дисперсной средой, относятся явления термофореза, фотофореза.
Явление термофореза наблюдается в аэрозолях под влиянием градиента температуры.
Термофорезом называют движение частиц аэрозоля в направлении области более низких температур. Причиной этого служит то, что более нагретую сторону частицы молекулы газа бомбандируют с большей скоростью. Чем менее нагретую. Частица получает импульс для движения в сторону более низкой температуры.
Фотофорезом называют перемещение частиц аэрозоля при одностороннем освещении. Направление движения зависит от многих свойств частиц – размера, формы, прозрачности и т.д.
Фотофорез отсутствует или проявляется очень слабо у веществ, хорошо отражающих свет, например фторида кальция, трехокиси сурьмы, и очень заметно у сильных поглотителей света: сажи, железных опилок.
Если сильнее нагревается сторона частицы, обращенная к источнику света, то благодаря усилившейся бомбардировке этой стороны молекулами окружающего газа частица смещается от источника света – имеет место положительный фотофорез. Если же сильнее будет нагреваться противоположная сторона частицы, то получается обратные эффект – отрицательный фотофорез.
Стоит сказать о роли фотофореза в медицине. Фотофорез лекарств метод, в основе которого лежит одновременное воздействие излучением и лекарственным веществом.
Суть фотофореза: на ограниченный участок кожи (до 80 см2) наносится около 1 мл р-ра лекарственного вещества и равномерно распределяется по поверхности кожи. Далее этот участок облучают расфокусированным лучом красного или инфракрасного света. Время облучения около 10-20 мин. В основе фотофореза лежит повышение проницаемости кожи под влиянием низкоинтенсивного лазерного излучения и ускорение диффузии лекарств.
Фотофорез имеет большой диапазон воздействия на организм. Он способен повышать повышать иммунитет, увеличивать выработку антител, усиливать клеточный обмен, синтез коллагена и эластина, улучшать микроциркуляцию крови и лимфы, усиливать проникновение питательных веществ в глубину кожи, нормализовать АД и т.д.
Дата добавления: 2015-09-04; просмотров: 354 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Основные безразмерные критерии подобия для описания аэродисперсных систем. | | | Методы получения аэрозолей |