
|
Читайте также: |

Синтез глікогену
Для синтезу полісахаридних ланцюгів глікогену глюкозо-6-фосфат повинен спочатку перетворитись у більш реакційноздатну форму – уридиндифосфатглюкозу (УДФ-глюкозу), яка є безпосереднім донором залишків глюкози в процесі синтезу. УДФ-глюкоза утворюється за дві реакції.
1. Перетворення глюкозо-6-фосфату у глюкозо-1-фосфат під дією фосфоглюкомутази:

2. Взаємодія глюкозо-1-фосфату з уридинтрифосфатом (УТФ), що каталізується глюкозо-1-фосфатуридилтрансферазою (УДФ-глюкозопірофосфорилазою):

Пірофосфат (ФФн) відразу ж гідролізується пірофосфатазою до двох молекул неорганічного фосфату, тому реакція йде у напрямку незворотного утворення УДФ-глюкози.
Далі залишок глюкози з УДФ-глюкози переноситься на кінець уже існуючої молекули глікогену. Реакцію каталізує глікогенсинтаза, яка відноситься до трансфераз, а не до синтетаз. У цій реакції утворюється новий альфа-1,4-глікозидний зв'язок між першим атомом вуглецю залишку глюкози, який приєднується, і гідроксилом у С-4 кінцевого залишку глюкози ланцюга глікогену:
УДФ-глюкоза + (глюкоза)n ® УДФ + (глюкоза)n+1
УДФ, який вивільняється, перетворюється знову в УТФ за рахунок АТФ (УДФ + АТФ ® УТФ + АДФ). Реакція багаторазово повторюється.
При відсутності у клітинах молекул глікогену, наприклад, коли внаслідок голодування запаси його повністю вичерпані, залишок глюкози із УДФ-глюкози переноситься на гідроксильну групу специфічного білка з подальшим нарощуванням вуглеводного ланцюга. Тому молекули глікогену містять сліди білка.
Утворення альфа-1,6-глікозидних зв'язків, які знаходяться у місцях розгалуження глікогену, каталізує фермент глікозил-(4®6)-трансфераза (фермент розгалужень). Це відбувається шляхом відриву фрагмента із 5 - 7 залишків глюкози із кінця лінійного ланцюга і перенесення його на гідроксил 6‑го вуглецю залишку глюкози, розміщеного ближче до внутрішньої частини молекули (рис.).

Після цього глікогенсинтаза приєднує до ланцюгів нові залишки глюкози. Точки розгалужень утворюються приблизно через кожні 8 - 12 залишків вздовж альфа-1,4-ланцюга. Така сильно розгалужена структура глікогену має важливе значення. По-перше, вона забезпечує наявність великої кількості кінців у молекулі, що забезпечує швидке приєднання чи звільнення молекул глюкози. Тому сильно розгалужена структура глікогену вигідніша, ніж менш розгалужена структура крохмалю. І, по-друге, цим досягається компактність, щільність упаковки молекул, які депонуються у клітинах у вигляді гранул діаметром 20 мкм. Із гранулами зв'язані ферменти синтезу й розпаду глікогену. Молекулярна маса молекул значно коливається (105-108).
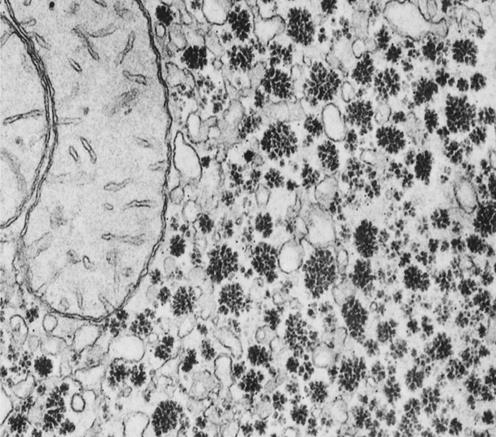
Основні запаси глікогену в організмі містяться в скелетних м'язах і печінці. Вміст у печінці складає 2-8 % маси органа і залежить від регулярності харчування і фізичного навантаження. Концентрація глікогену в скелетних м'язах, що знаходяться у стані спокою, – тільки 0,5-1 %, але із-за великої маси м'язів більша частина глікогену тіла знаходиться в них. У середньому у дорослої людини після споживання їжі міститься в печінці близько 100 г глікогену, а в м'язах (стан спокою) – 400 г. Глікоген м'язів служить джерелом енергії під час скорочення м'язів, а функція глікогену печінки – підтримувати постійність концентрації глюкози в крові.
Розпад глікогену
Шлях розпаду глікогену до вільної глюкози відрізняється від синтезу його (рис.).
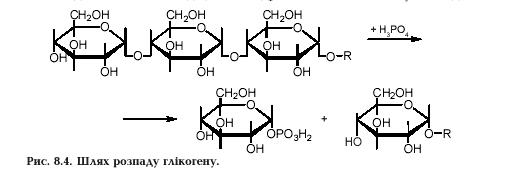
Він включає ряд інших ферментів. Глікоген-фосфорилаза каталізує першу реакцію катаболізму глікогену – розрив альфа-1,4-глікозидного зв'язку між залишками глюкози на кінцях ланцюгів шляхом фосфоролізу, тобто взаємодії з неорганічним фосфатом. Крайні залишки глюкози відщеплюються у формі глюкозо-1-фосфату.
Таким чином, спосіб розриву альфа-1,4-глікозидних зв'язків глікогену в тканинах відрізняється від гідролітичного розриву їх під дією амілази у ШКТ. Фосфорилазна реакція повторюється до тих пір, поки не залишаються 4 глюкозні залишки до точки розгалуження. Тоді фермент альфа-(1®6)-глікозидаза переносить триглюкозний фермент на кінець сусіднього ланцюга, а четвертий залишок глюкози, який зв'язаний альфа-1,6-глікозидним зв'язком, відщеплює гідролітичним шляхом у вигляді вільної глюкози. Далі глікоген-фосфорилаза каталізує відщеплення глюкозних залишків до нової точки розгалуження.

Структура глікогенфосфорилази (ГФ)
• Каталітичний центр
• Аллостеричний центр
• Центр для фосфорилювання (ковалентна модифікація)
• Дві форми ГФ
Фосфорилаза a (фосфорильована) – активна форма
Фосфорилаза b (дефосфоильована) – неактивна форма
Молекули глюкозо-1-фосфату перетворюються у глюкозо-6-фосфат під впливом фосфоглюкомутази, яка каталізує цю ж реакцію у зворотному напрямку в процесі біосинтезу глікогену. Перехід глюкозо-6-фосфату до вільної глюкози не може здійснюватись шляхом гексокіназної реакції, оскільки вона незворотна. У печінці і нирках є фермент глюкозо-6-фосфатаза, який каталізує реакцію гідролізу глюкозо-6-фосфату до глюкози:
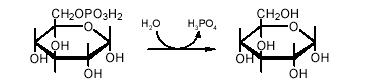

Вільна глюкоза виходить у кров і надходить в інші органи. У м'язах, мозку й інших тканинах глюкозо-6-фосфатаза відсутня. Таким чином, глікоген печінки служить джерелом глюкози для всього організму, а глікоген м'язів, мозку розпадається до глюкозо-6-фосфату, який використовується у цих тканинах.
Розпад глікогену до молочної кислоти (глікогеноліз)

Субстратом гліколізу в м'язах служать глюкоза, яка надходить із крові, і глюкозні залишки депонованого глікогену. Внаслідок послідовної дії глікогенфосфорилази і фосфоглюкомутази глюкозні залишки глікогену перетворюються в глюкозо-6-фосфат, який далі включається в процес гліколізу:

За умов глікогенолізу АТФ затрачається тільки один раз для утворення фруктозо-1,6-дифосфату. Тому при розпаді одного глюкозного залишку глікогену вихід АТФ складає 4-1=3 молекули:

Якщо ж врахувати затрати АТФ для біосинтезу глікогену (дві молекули АТФ для включення одного залишку глюкози), тоді чистий вихід складає тільки 1 молекулу АТФ на 1 залишок глюкози. Витрачання АТФ для синтезу глікогену в м'язах має місце в стані спокою, коли депонування глікогену достатньо забезпечене киснем і енергією. А під час інтенсивного фізичного навантаження анаеробний розпад глікогену до молочної кислоти зумовлює більший вихід АТФ, ніж розпад глюкози.
Спадкові порушення обміну глікогену
Відомі спадкові хвороби, пов'язані з дефектом якогось одного із ферментів обміну глікогену. Їх називають глікогенозами, чи глікогеновими хворобами. В табл. 8.2 наведені типи глікогенозів і їх характеристика.

При нестачі глікогенсинтази в печінці значно знижується вміст глікогену, в проміжках між споживанням їжі швидко настає зменшення концентрації глюкози в крові, а після надходження значної кількості вуглеводів спостерігається тривала гіперглікемія. Нестача ферментів розпаду глікогену зумовлює його накопичення в тканинах. При цьому структура глікогену може бути нормальною або, при відсутності альфа‑(1®6)-глюкозидази, аномальною, з дуже короткими боковими гілками. У хворих спостерігаються характерні для кожного типу клінічні симптоми: збільшення печінки (тип І, ІІІ, VI), м'язова слабість (тип V), затримка розумового розвитку і корчі внаслідок виражених гіпоглікемій (тип І). Нестача глікозил-(4®6)-трансферази також призводить до аномальної структури глікогену – з довгими малорозгалуженими ланцюгами. І хоч при цьому типі глікогенозу (IV) кількість глікогену може бути зниженою чи нормальною, але внаслідок, вірогідно, реакції організму на саме таку структуру молекул глікогену настають печінкова недостатність і смерть у ранньому віці. Рання смерть спостерігається і при глікогенозі типу ІІ (хворобі Помпе), коли відсутній фермент лізосом альфа-глюкозидаза. В нормі під дією цього ферменту розпадається тільки 1-3 % глікогену клітин печінки, м'язів, серця. При відсутності альфа-глюкозидази глікоген накопичується у вакуолях цитоплазми клітин.
Регуляція метаболізму глікогену
Регуляторні ферменти синтезу і розпаду глікогену – глікогенсинтаза і фосфорилаза.

Активність їх регулюється двома шляхами – ковалентною модифікацією (фосфорилюванням) молекули ферменту і під дією алостеричних ефекторів. Глікогенсинтаза існує в неактивній фосфорильованій формі й активній нефосфорильованій формі. Навпаки, неактивна форма глікогенфосфорилази (фосфорилаза b) є нефосфорильованою, а активна форма, фосфорилаза a, фосфорильована. Реакцію фосфорилювання глікогенсинтази каталізує цАМФ-залежна протеїнкіназа, а фосфорилази – цАМФ-залежна кіназа фосфорилази b. Під час реакції фосфатна група переноситься із АТФ на гідроксильну групу двох залишків серину молекул глікогенсинтази і фосфорилази b. Ферменти фосфопротеїнфосфатази каталізують протилежну реакцію – відщеплюють фосфатні групи шляхом гідролізу, тобто переводять глікогенсинтазу і фосфорилазу в дефосфорильовану форму (рис.).

Підкреслимо, що фосфорилювання зумовлює активацію фосфорилази й інактивацію глікогенсинтази, а дефосфорилювання – протилежні ефекти. Таким чином, якщо стимулюється синтез глікогену, то одночасно гальмується його розпад, і навпаки.
Активність кіназ і фосфатаз, а значить, синтез і розпад глікогену, знаходяться під гормональним контролем. Синтез глікогену стимулює інсулін, а розпад – адреналін і глюкагон. Дія адреналіну і глюкагону опосередковується через вторинний посередник – цАМФ. Зв'язування їх зі своїми рецепторами, локалізованими у клітинній мембрані, зумовлює активацію аденілатциклази, яка каталізує синтез цАМФ із АТФ (рис.).

цАМФ активує протеїнкіназу. Неактивна протеїнкіназа складається із двох каталітичних і двох регуляторних субодиниць. При підвищенні концентрації у клітині цАМФ він зв'язується з регуляторними субодиницями, що викликає розпад тетрамерної форми протеїнкінази. Звільнені каталітичні субодиниці протеїнкінази каталізують реакцію фосфорилювання кінази фосфорилази, що переводить її в активну форму і таким чином зумовлює утворення фосфорилази a. Одночасно каталітичні субодиниці протеїнкінази каталізують фосфорилювання глікогенсинтази, тим самим перетворюючи її в неактивну форму.
http://www.youtube.com/watch?v=oBL0OC3IavI
Багатостадійність передачі сигналу від гормону до фосфорилази, яка безпосередньо каталізує розпад глікогену, має важливе значення, оскільки в такому каскадному процесі досягається сильне і швидке підсилення сигналу. Так, зв'язування декількох молекул адреналіну зумовлює синтез більшої кількості молекул цАМФ, а далі кожна молекула ферменту активує велику кількість молекул наступного ферменту (протеїнкіназа – кіназа фосфорилази – фосфорилаза). Активність фосфорилази досягає максимуму вже через декілька хвилин після зв'язування адреналіну клітинами печінки, а підсилення сигналу складає близько 25 млн раз (декілька молекул гормону викликають надходження із печінки в кров декількох грам глюкози).
Послідовність реакцій, що призводить до інактивації глікогенсинтази, має на одну стадію менше, ніж послідовність активації фосфорилази (рис.).

Тому підсилення гормонального сигналу більше у системі розпаду глікогену. Максимальна швидкість синтезу глікогену м'язів не перевищує 0,3 % максимальної швидкості глікогенолізу.
При припиненні секреції адреналіну чи глюкагону аденілатциклаза переходить в неактивний стан. Наявний цАМФ розпадається під дією фосфодіестерази до АМФ, і в результаті утворюється тетрамерна неактивна форма протеїнкінази. Фосфатази каталізують дефосфорилювання кінази фосфорилази, фосфорилази а і глікогенсинтази. Таким чином, виключається розпад глікогену і стає можливим його синтез.
Адреналін стимулює розпад і гальмує синтез глікогену в печінці, скелетних м'язах, міокарді. Секреція його у стресових ситуаціях зумовлює вивільнення глюкози із печінки в кров для постачання інших органів, а в м'язах – розпад глікогену до молочної кислоти з виділенням енергії, що забезпечує швидке зростання м'язової активності. Глюкагон стимулює розпад глікогену печінки, але не впливає на глікоген м'язів. Секретується підшлунковою залозою при зниженні концентрації глюкози в крові.
Гормон підшлункової залози інсулін стимулює надходження глюкози в клітини і синтез глікогену. Механізми його дії ще до кінця не з'ясовані. Одним із них є активація інсуліном фосфодіестерази цАМФ, що приводить до зниження внутрішньоклітинного рівня цАМФ, у результаті стимулюється утворення неактивної фосфорилази й активної глікогенсинтази. У гепатоцитах інсулін підвищує активність глюкокінази.
Існує ряд додаткових способів регуляції активності ферментів розпаду і синтезу глікогену:
1. Неактивна фосфорилаза b м'язів може активуватись без фосфорилювання, тобто не перетворюючись у фосфорилазу а. Це здійснюється шляхом зв'язування в алостеричному центрі фосфорилази b АМФ. Алостеричній активації фосфорилази b із АМФ перешкоджає АТФ. У стані м'язового спокою, коли концентрація АТФ значно більша, ніж АМФ, фосфорилаза знаходиться в неактивній b-формі. Під час роботи м'язів концентрація АТФ знижується, а зростає концентрація АМФ, що зумовлює активацію фосфорилази b і, в результаті, розщеплення глікогену для синтезу АТФ. Але швидке і значне збільшення швидкості глікогенолізу в м'язах відбувається тільки у результаті перетворення фосфорилази b у фосфорилазу а.
2. Кіназа фосфорилази м'язів також може переходити в активну форму без фосфорилювання. Активатором служать іони кальцію, концентрація яких в саркоплазмі різко зростає у відповідь на нервовий імпульс, який зумовлює скорочення м'язів.
3. Неактивна фосфорильована форма глікогенсинтази активується алостерично глюкозо-6-фосфатом. При наявності достатньо високої концентрації глюкозо-6-фосфату фосфорильований фермент проявляє майже таку активність, як дефосфорильований.
4. Провідну роль у регуляції метаболізму глікогену в печінці відіграє концентрація глюкози. Її високий вміст викликає перехід фосфорилази а у фосфорилазу b й утворення активної глікогенсинтази, що приводить до зупинки розпаду глікогену і стимуляції його синтезу. При зниженні концентрації глюкози синтез глікогену пригнічується і починається розпад його.
Дата добавления: 2015-09-05; просмотров: 391 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| ПРИМЕР 2 | | | Глюконеогенез |