
Читайте также:
|
(таблицы и схемы)
 Схема 1. Физиология бактерий.
Схема 1. Физиология бактерий.
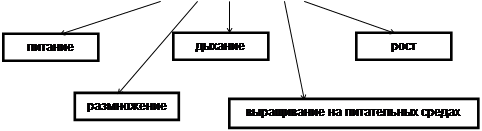
Таблица 1. Общая таблица физиологии бактерий.
| № | Понятие | Характеристика |
| Питание | Процесс приобретения энергии и веществ. | |
| Дыхание | Совокупность биохимических процессов, в результате которых освобождается энергия, необходимая для жизнедеятельности микробных клеток. | |
| Рост | Координированное воспроизведение всех клеточных компонентов и структур, ведущее в конечном итоге к увеличению массы клетки | |
| Размножение | Увеличение числа клеток в популяции | |
| Выращивание на питательных средах. | В лабораторных условиях микроорганизмы выращивают на питательных средах, которые должны быть стерильными, прозрачными, влажными, содержать определенные питательные вещества (белки, углеводы, витамины, микроэлементы и др.), обладать определенной буферностью, иметь соответствующий рН, окислительно-восстановительный потенциал. |
Таблица 1.1 Химический состав и физиологические функции элементов.
| № | Элемент состава | Характеристика и роль в физиологии клетки. | |
| Вода | Основной компонент бактериальной клетки, составляющий около 80 % ее массы. Она находится в свободном или связанном состоянии со структурными элементами клетки. В спорах количество воды уменьшается до 18.20 %. Вода является растворителем для многих веществ, а также выполняет механическую роль в обеспечении тургора. При плазмолизе – потере клеткой воды в гипертоническом растворе – происходит отслоение протоплазмы от клеточной оболочки. Удаление воды из клетки, высушивание приостанавливают процессы метаболизма. Большинство микроорганизмов хорошо переносят высушивание. При недостатке воды микроорганизмы не размножаются. Высушивание в вакууме из замороженного состояния (лиофилизация) прекращает размножение и способствует длительному сохранению микробных особей. | ||
| Белки | 40 – 80 % сухой массы. Определяют важнейшие биологические свойства бактерий и состоят обычно из сочетаний 20 аминокислот. В состав бактерий входит диаминопимелиновая кислота (ДАП), отсутствующая в клетках человека и животных. Бактерии содержат более 2000 различных белков, находящихся в структурных компонентах и участвующих в процессах метаболизма. Большая часть белков обладает ферментативной активностью. Белки бактериальной клетки обусловливают антигенность и иммуногенность, вирулентность, видовую принадлежность бактерий. | ||
| № | Элемент состава | Характеристика и роль в физиологии клетки. | |
| Нуклеиновые кислоты | Выполняют функции, аналогичные нуклеиновым кислотам эукариотических клеток: молекула ДНК в виде хромосомы отвечает за наследственность, рибонуклеиновые кислоты (информационная, или матричная, транспортная и рибосомная) участвуют в биосинтезе белка. | ||
| Углеводы | Представлены простыми веществами (моно- и дисахариды) и комплексными соединениями. Полисахариды часто входят в состав капсул. Некоторые внутриклеточные полисахариды (крахмал, гликоген и др.) являются запасными питательными веществами. | ||
| Липиды | Входят в состав цитоплазматической мембраны и ее производных, а также клеточной стенки бактерий, например наружной мембраны, где, кроме биомолекулярного слоя липидов, имеется ЛПС. Липиды могут выполнять в цитоплазме роль запасных питательных веществ. Липиды бактерий представлены фосфолипидами, жирными кислотами и глицеридами. Наибольшее количество липидов (до 40 %) содержат микобактерии туберкулеза. | ||
| Минеральные вещества | Обнаруживают в золе после сжигания клеток. В большом количестве выявляются фосфор, калий, натрий, сера, железо, кальций, магний, а также микроэлементы (цинк, медь, кобальт, барий, марганец и др.).Они участвуют в регуляции осмотического давления, рН среды, окислительно-восстановительного потенциала, активируют ферменты, входят в состав ферментов, витаминов и структурных компонентов микробной клетки. | ||
Таблица 1.2. Азотистые основания.
| № | Азотистые основания | Характеристика | Примечание |
| Пуриновые | Аденин, Гуанин | Состав нуклеотида: дезоксирибоза, азотистые основания - аденин, гуанин, цитозин, тимин, остаток Н3РО4. Комплементарность азотистых оснований А = Т, Г = Ц. Двойная спираль. Способна к самоудвоению | |
| Пиримидиновые | Цитозин, Тимин или Урацил (у РНК вместо Тимина) |
Таблица 1.2.1 Ферменты
| № | Признак | Характеристика | |
| Определение | Специфичные и эффективные белковые катализаторы, присутствующие во всех живых клетках. | ||
| Функции | Ферменты снижают энергию активации, обеспечивая протекание таких химических реакций, которые без них могли бы проходить только при высокой температуре, избыточном давлении и при других нефизиологических условиях, неприемлемых для живой клетки. | ||
| Ферменты увеличивают скорость реакции примерно на 10 порядков, что сокращает полупериод какой-либо реакции с 300 лет до одной секунды. | |||
| Ферменты «узнают» субстрат по пространственному расположению его молекулы и распределению зарядов в ней. За связывание с субстратом отвечает определённый участок молекулы ферментативного белка — его каталитический центр. При этом образуется промежуточный фермент-субстратный комплекс, который затем распадается с образованием продукта реакции и свободного фермента. | |||
| Разновидности | Регуляторные (аллостерические) ферменты воспринимают различные метаболические сигналы и в соответствии с ними изменяют свою каталитическую активность. | Эффекторные ферменты - ферменты катализирующие некоторые реакции (подробнее табл. 1.2.2.) | |
| Функциональная активность | Функциональная активность ферментов и скорость ферментативных реакций зависят от условий, в которых находится данный микроорганизм и прежде всего от температуры среды и ее pH. Для многих патогенных микроорганизмов оптимальными являются температура 37°С и pH 7,2-7,4. |
 |

Таблица 1.2.2. Классы эффекторных ферментов
| № | Класс фермента | Катализирует: |
| Оксидоредуктазы | Перенос электронов | |
| Трансферазы | Перенос различных химических групп | |
| Гидролазы | Перенос функциональных групп на молекулу воды | |
| Лиазы | Присоединение групп по двойным связям и обратные реакции | |
| Изомеразы | Перенос групп внутри молекулы с образованием изомерных форм | |
| Лигазы | Образование связей С-С, C-S, С-О, C-N за счёт реакций конденсации, сопряжённых с распадом аденозинтрифосфата (АТФ) |
Таблица 1.2.3. Типы ферментов по образованию в бактериальной клетке
| № | Тип | Характеристика | Примечания |
Иидуцибельные (адаптивные)
 ферменты
«индукция субстратом» ферменты
«индукция субстратом»
| 1. Ферменты, концентрация которых в клетке резко возрастает в ответ на появление в среде субстрата-индуктора. 2. Синтезируются бактериальной клеткой только при наличии в среде субстрата данного фермента | ||
| Репрессибельные ферменты | Синтез этих ферментов подавляется в результате избыточного накопления продукта реакции, катализируемой данным ферментом. | Примером репрессии ферментов может служить синтез триптофана, который образуется из антраниловой кислоты с участием антранилатсинтетазы. | |
| Конститутивные ферменты | Ферменты, синтезируемые вне зависимости от условий среды | Ферменты гликолиза | |
| Мультиферментные комплексы | Внутриклеточные ферменты, объединенные структурно и функционально | Ферменты дыхательной цепи, локализованные на цитоплазматической мембране. |
Таблица 1.2.4. Специфические ферменты
| № | Ферменты | Идентификация бактерий |
| Супероксид дисмутаза и каталаза | Все аэробы или факультативные анаэробы обладают супероксид дисмутазой и каталазой — ферментами, защищающими клетку от токсичных продуктов кислородного метаболизма. Практически все облигатные анаэробы не синтезируют эти ферменты. Только одна группа аэробных бактерий — молочнокислые бактерии каталазонегативны. | |
| Пероксидаза | Молочнокислые бактерии аккумулируют пероксидазу — фермент, катализирующий окисление органических соединений под действием Н202 (восстанавливается до воды). | |
| Аргининдигидролаза | Диагностический признак, позволяющий различить сапрофитические виды Pseudomonas от фитопатогенных. | |
| Уреаза | Среди пяти основных групп семейства Enterobacteriaceae только две — Escherichiae и Erwiniae— не синтезируют уреазу. |
Таблица 1.2.5. Применение ферментов бактерий в промышленной микробиологии.
| № | Ферменты | Применение |
| Амилаза, целлюлаза, протеаза, липаза | Для улучшения пищеварения применяют готовые препараты ферментов, облегчающих соответственно гидролиз крахмала, целлюлозы, белка и липидов | |
| Инвертаза дрожжей | При изготовлении сладостей для предупреждения кристаллизации сахарозы | |
| Пектиназа | Используют для осветления фруктовых соков | |
| Коллагеназа клостридий и стрептокиназа стрептококков | Гидролизуют белки, способствуют заживлению ран и ожогов | |
| Литические ферменты бактерий | Секретируются в окружающую среду, действуют на клеточные стенки патогенных микроорганизмов и служат эффективным средством в борьбе с последними, даже если они обладают множественной устойчивостью к антибиотикам | |
| Рибонуклеазы, дезоксирибонуклеазы, полимеразы, ДНК-лигазы и прочие ферменты, направленно модифицирующие нуклеиновые кислоты | Используют в качестве инструментария в биоорганической химии, генной инженерии и генотерапии |
Таблица 1.2.6. Классификация ферментов по локализации.
| № | Класс | Локализация | Функции |
| Эндоферменты | 1. В цитоплазме 2. В цитоплазматической мембране 3. В периплазматическом пространстве | Функционируют только внутри клетки. Они катализируют реакции биосинтеза и энергетического обмена. | |
| Экзоферменты | Выделяются в окружающую среду. | Выделяются клеткой в среду и катализируют реакции гидролиза сложных органических соединений на более простые, доступные для ассимиляции микробной клеткой. К ним относятся гидролитические ферменты, играющие исключительно важную роль в питании микроорганизмов. |
Таблица 1.2.7. Ферменты патогенных микробов (ферменты агрессии)
| № | Ферменты | Функция | Образование некоторых ферментов в лабораторных условиях | |||
| Лецитовителлаза = лецитиназа | Разрушает клеточные мембраны | 1. Посев исследуемого материала на питательную среду ЖСА
2. Результат: зона помутнения вокруг колоний на ЖСА.
| ||||
| Гемолизин | Разрушает эритроциты | 1. Посев исследуемого материала на питательную среду кровяной агар.
2. Результат: полная зона гемолиза вокруг колоний на кровяном агаре.
| ||||
| Коагулаза-положительные культуры | Вызывает свертывание плазмы крови | 1. Посев исследуемого материала на стерильную цитратную плазму крови. 2. Результат: свёртывание плазмы | ||||
| Коагулаза-отрицательные культуры | Выработка маннита | 1. Посев на питательную среду маннит в анаэробных условиях. 2. Результат: Появление окрашенных колоний (в цвет индикатора) | ||||
| № | Ферменты | Функция | Образование некоторых ферментов в лабораторных условиях | |||
| Гиалуронидаза | Гидролизирует гиалуроновую кислоту — основной компонент соединительной ткани | 1. Посев исследуемого материала на питательную среду, содержащую гиалуроновую кислоту. 2. Результат: в пробирках, где содержится гиалуронидаза, не происходит образования сгустка. | ||||
| Нейраминидаза | Отщепляет от различных гликопротеидов, гликолипидов, полисахаридов сиаловую (нейраминовую) кислоту, повышая проницаемость различных тканей. | Выявление: реакция определения антител к нейраминидазе (РИНА) и другие (иммунодиффузные, иммуноэнзимные и радиоиммунные методы). |
Таблица 1.2.8. Классификация ферментов по биохимическим свойствам.
| № | Ферменты | Функция | Обнаружение |
| Сахаролитические | Расщепление сахаров | Дифференциально - диагностические среды такие, как среды Гисса, среда Олькеницкого, среда Эндо, среда Левина, среда Плоскирева. | |
| Протеолитические | Расщепление белков | Микробы засевают уколом в столбик желатина и после 3-5 суток инкубирования при комнатной температуре отмечают характер разжижения желатина. Протеолитическую активность определяют также по образованию продуктов разложения белка: индола, сероводорода, аммиака. Для их определения микроорганизмы засевают в мясо-пептонный бульон. | |
| Ферменты, выявляемые по конечным продуктам | · Образование щелочей · Образование кислот · Образование сероводорода · Образование аммиака и др. | Для отличия одних видов бактерий от других на основании их ферментативной активности применяются дифференциально-диагностические среды |
Схема 1.2.8. Ферментный состав.

Таблица 1.3. Пигменты
| № | Пигменты | Синтез микроорганизмом |
| Жирорастворимые каротиноидные пигменты красного, оранжевого или желтого цветов | Образуют сарцины, микобактерии туберкулеза, некоторые актиномицеты. Эти пигменты предохраняют их от действия УФ-лучей. | |
| Пигменты черного или коричневого цвета — меланины | Синтезируются облигатными анаэробами Bacteroides niger и др. не растворимы в воде и даже сильных кислотах | |
| Пирроловый пигмент ярко-красного цвета, – продигиозин | Образуется некоторыми серациями | |
| Водорастворимый фенозиновый пигмент, – пиоцианин. | Продуцируются синегнойными бактериями (Pseudomonas aeruginosa). При этом питательная среда с нейтральным или щелочным pH окрашивается в сине-зеленый цвет. |
Таблица 1.4. Светящиеся и ароматообразующие микроорганизмы
| № | Явление | Условие и характеристика |
| Свечение (люминесценция) | Бактерии вызывают свечение тех субстратов, например чешуи рыб, высших грибов, гниющих деревьев, пищевых продуктов, на поверхности которых размножаются. Большинство светящихся бактерий относятся к галофильным видам, способным размножаться при повышенных концентрациях солей. Они обитают в морях и океанах и редко — в пресных водоемах. Все светящиеся бактерии являются аэробами. Механизм свечения связан с освобождением энергии в процессе биологического окисления субстрата. | |
| Ароматообразование | Некоторые микроорганизмы вырабатывают летучие ароматические вещества, например уксусно-этиловый и уксусно-амиловый эфиры, которые придают аромат вину, пиву, молочнокислым и другим пищевым продуктам, вследствие чего применяются в их производстве. |
Таблица 2.1.1.Метаболизм
| № | Понятие | Определение |
| Метаболизм | Биохимические процессы, протекающие в клетке, объединены одним словом — метаболизм (греч. metabole — превращение). Этот термин равнозначен понятию «обмен веществ и энергии». Различают две стороны метаболизма: анаболизм и катаболизм. | |
| 1. Анаболизм — совокупность биохимических реакций, осуществляющих синтез компонентов клетки, т. е. та сторона обмена веществ, которую называют конструктивным обменом. | 2. Катаболизм — совокупность реакций, обеспечивающих клетку энергией, необходимой, в частности, и для реакций конструктивного обмена. Поэтому катаболизм определяют еще как энергетический обмен клетки. | |
| Амфиболизм | Промежуточный обмен веществ, превращающий низкомолекулярные фрагменты питательных веществ в ряд органических кислот и фосфорных эфиров, называют |
Схема 2.1.1. Метаболизм

Таблица 2.1.3. Обмен веществ и превращение энергии клетки.
| № | Обмен веществ | Характеристика | Примечания | |||
| Функция | Обмен веществ обеспечивает присущее живому организму как системе динамическое равновесие, при котором взаимно уравновешиваются синтез и разрушение, размножение и гибель. | Обмен веществ — главный признак жизни | ||||
Пластический обмен
 Синтез белков, жиров, углеводов.
Синтез белков, жиров, углеводов.
| Это совокупность реакций биологического синтеза. | Из веществ поступающих в клетку извне, образуются молекулы, подобные соединениям клетки, то есть происходит ассимиляция. | ||||
Энергетический обмен
распад
| Процесс противоположный синтезу. Это совокупность реакций расщепления. | При расщеплении высокомолекулярных соединений выделяется энергия, необходимая для реакции биосинтеза, то есть происходит диссимиляция. · При расщеплении глюкозы энергия выделяется поэтапно при участии ряда ферментов. |
Таблица 2.1.2. Различие в метаболизме для идентификации.
| № | Параметры |
| Способность к утилизации различных веществ в качестве источника углерода. | |
| Способность к образованию специфических конечных продуктов в результате разложения субстратов. | |
| Способность смешать рН среды культивирования в кислую или щелочную сторону. Метаболизм большинства бактерий осуществляется посредством биохимических реакций разложения органических (реже неорганических) веществ и синтеза компонентов бактериальной клетки из простых углеродсодержащих соединений. |
Таблица 2.2 Анаболизм (конструктивный метаболизм)
| № | Группа реакций анаболизма | Синтезируются: |
| Биосинтез мономеров | Аминокислот, нуклеотидов, моносахаров, жирных кислот | |
| Биосинтез полимеров | Белков, нуклеиновых кислот, полисахаридов и липидов |
Схема 2.2.2. Биосинтез аминокислот у прокариот.
Автор – Л.Б. Борисов, стр. 52 «Медицинская микробиология»

Схема 2.2.1. Биосинтез углеводов у микроорганизмов.

Автор – Л.Б. Борисов, стр. 51 «Медицинская микробиология»
Рисунок 2.2.3. Биосинтез липидов

Таблица 2.2.4. Этапы энергетического обмена – Катаболизм.
| № | Этапы | Характеристика | Примечание |
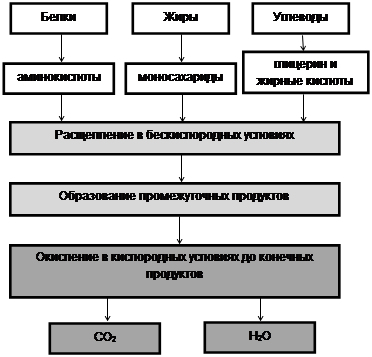
| Подготовительный | Молекулы дисахаридов и полисахаридов, белков распадаются на мелкие молекулы – глюкозу, глицерин и жирные кислоты, аминокислоты. Крупные молекулы нуклеиновых кислот на нуклеотиды. | На этом этапе выделяется небольшое количество энергии, которая рассеивается в виде теплоты. | |
| Бескислородный или неполный или анаэробный или брожение или диссимиляция. | Образующиеся на этом этапе вещества при участии ферментов подвергаются дальнейшему расщеплению. Например: глюкоза распадается на две молекулы молочной кислоты и две молекулы АТФ. | В реакциях расщепления глюкозы участвует АТФ и H3PO4. В ходе бескислородного расщепления глюкозы в виде химической связи в молекуле АТФ сохраняется 40 % энергии, остальная рассеивается в виде теплоты. Во всех случаях распада одной молекулы глюкозы образовывается две молекулы АТФ. | |
| Стадия аэробного дыхания или кислородного расщепления. | При доступе кислорода к клетке образовавшиеся во время предыдущего этапа вещества окисляются (расщепляются) до конечных продуктов CO2 и H2O. | Суммарное уравнение аэробного дыхания:

|
Схема 2.2.4. Брожение.

 Схема 2.2.5. Пировиноградная кислота.
Схема 2.2.5. Пировиноградная кислота.
 |
Таблица 2.2.5. Брожение.
| № | Тип брожения | Представители | Конечный продукт | Примечания |
| Молочнокислое | · Streptococcus · Bifidobacterium · Lactobacterium | Образуют из пирувата молочную кислоту | В одних случаях (гомоферментное брожение) образуется только молочная кислота, в других также побочные продукты. | |
| Муравьинокислое | · Enterobacteriaceae | Муравьиная кислота – один из конечных продуктов. (наряду с ней – побочные) | Некоторые виды энтеробактерий расщепляют муравьиную кислоту до H2 и CO2/ | |
| Маслянокислое | · Clostridium | Масляная кислота и побочные продукты | Некоторые вид ы клостридий наряду с масляной и другими кислотами образуют бутанол, ацетон и др. (тогда его называют ацетоно-бутиловое брожение). | |
| Пропионовокислое | · Propionobacterium | Образуют из пирувата пропионовую кислоту | Многие бактерии при сбраживании углеводов наряду с другими продуктами образуют этиловый спирт. При этом он не является основным продуктом. |
Таблица 2.3.1. Белоксинтезирующая система, ионный обмен.
| № | Название элемента | Характеристика |
| Рибосомные субъединицы 30S и 50S | В случае бактериальных рибосом 70S субчастица 50S содержит рРНК 23S (длина ~3000 нуклеотидов) и субчастица 30S содержит рРНК 16S (длина ~1500 нуклеотидов); большая рибосомная субчастица кроме «длинной» рРНК содержит также одну или две «коротких» рРНК (5S рРНК бактериальных рибосомных субчастиц 50S или 5S и 5.8S рРНК больших рибосомных субчастиц эукариот). (подробнее – см. рис. 2.3.1.) | |
| Матричная РНК (мРНК) | РНК, содержащая информацию о первичной структуре (аминокислотной последовательности) белков | |
| Полный комплект двадцати аминоацил-тРНК, для образования которых необходимы соответствующие аминокислоты, аминоацил-тРНК-синтетазы, тРНК и АТФ | Это заряженная энергией и связанная с тРНК аминокислота, готовая для подвоза к рибосоме и включения в синтезирующийся на ней полипептид. | |
| Транспортная РНК (тРНК) | Рибонуклеиновая кислота, функцией которой является транспортировка аминокислот к месту синтеза белка. | |
| Белковые факторы инициации | (у прокариот - IF-1, IF-2, IF-3) Получили свое название потому, что они участвуют в организации активного комплекса (708-комплекса) из субъединиц 30S и 50S, мРНК и инициаторной аминоацил-тРНК (у прокариот — формилметионил-тРНК), который «запускает» (инициирует) работу рибосом — трансляцию мРНК. | |
| Белковые факторы элонгации | (у прокариот - EF-Tu, EF-Ts, EF-G) Участвуют в удлинении (элонгации) синтезируемой полипептидной цепи (пептидила). Белковые факторы терминации или освобождения (англ. — release factors — RF) обеспечивают кодон-специфическое отделение полипептида от рибосомы и окончание синтеза белка. | |
| № | Название элемента | Характеристика |
| Белковые факторы терминации | (у прокариот - RF-1, RF-2, RF-3) | |
| Некоторые другие белковые факторы (ассоциации, диссоциации субъединиц, высвобождения и пр.). | Белковые факторы трансляции, необходимые для функционирования системы | |
| Гуанозинтрифосфат (ГТФ) | Для осуществления трансляции необходимо участие ГТФ. Потребность белоксинтезирующей системы в ГТФ очень специфична: он не может быть заменен ни одним из других трифосфатов. На биосинтез белка клетка затрачивает энергии больше, чем на синтез любого другого биополимера. Образование каждой новой пептидной связи требует расщепления четырех высокоэнергетических связей (АТФ и ГТФ): двух для того, чтобы нагрузить аминокислотой молекулу тРНК, и еще двух в ходе элонгации — одну при связывании аа-тРНК и другую при транслокации. | |
| Неорганические катионы в определенной концентрации. | Для поддержания рН системы в физиологических пределах. Ионы аммония используются некоторыми бактериями для синтеза аминокислот, ионы калия — для связывания тРНК с рибосомами. Ионы железа, магния выполняют роль кофактора в ряде ферментативных процессов |
Рисунок 2.3.1. Схематическое изображение структур прокариотических и эукариотических рибосом.
Автор – Коротяев, стр. 68 «Медицинская микробиология»

Таблица 2.3.2. Особенности ионного обмена у бактерий.
| № | Особенность | Характеризуется: | |
| Высокое осмотическое давление | Благодаря значительной внутриклеточной концентрации ионов калия в бактериях поддерживается высокое осмотическое давление. | ||
| Потребление железа | Для ряда патогенных и условно-патогенных бактерий (эшерихии, шигеллы и др.) потребление железа в организме хозяина затруднено из-за его нерастворимости при нейтральных и слабощелочных значениях pH | Сидерофоры –специальные вещества, которые, связывая железо, делают его растворимым и транспортабельным. | |
| Ассимиляция | Бактерии активно ассимилируют из среды анионы SO2/ и Р034+ для синтеза соединений, содержащих эти элементы (серосодержащие аминокислоты, фосфолипиды и др.). | ||
| Ионы | Для роста и размножения бактерий необходимы минеральные соединения — ионы NH4+, К+, Mg2+ и др. (подробнее, смотри табл. 2.3.1.) |
Таблица 2.3.3. Ионный обмен
| № | Название минеральных соединений | Функция |
| NH4+ (ионы аммония) | Используются некоторыми бактериями для синтеза аминокислот | |
| K+ (ионы калия) | 1) Используются для связывания т-РНК с рибосомами 2) Поддерживают высокое осмотическое давление | |
| Fe2+ (ионы железа) | 1) Выполняют роль кофакторов в ряде ферментативных процессов 2) Входят в состав цитохромов и других гемопротеидов | |
| Mg2+ (ионы магния) | ||
| SO42- (сульфат-анион) | Необходимы для синтеза соединений, содержащих эти элементы (серосодержащие аминокислоты, фосфолипиды и др.) | |
| PO43- (фосфат-анион) |
Схема 2.4.1. Энергетический метаболизм.

Таблица 2.4.1. Энергетический метаболизм (биологическое окисление).
| № | Процесс | Необходимо: |
| Синтез структурных компонентов микробной клетки и поддержание процессов жизнедеятельности | Достаточное количество энергии. Эта потребность удовлетворяется за счет биологического окисления, в результате которого синтезируются молекулы АТФ. | |
| Энергия (АТФ) | Железобактерии получают энергию, выделяющуюся при непосредственном окислении ими железа (Fe2+ в Fe3+), которая используется для фиксации С02, бактерии, метаболизирующие серу, обеспечивают себя энергией за счет окисления серосодержащих соединений. Однако подавляющее большинство прокариот получает энергию путем дегидрогенирования. Получение энергии происходит также в процессе дыхания (подробную таблицу смотри в соответствующем разделе). |
Схема 2.4. Биологическое окисление у прокариот.
 | |||||
 | |||||
 | |||||
 | |||||
 | |||||
Таблица 2.4.2. Энергетический метаболизм.
| № | Понятие | Характеристика |
| Сущность энергетического метаболизма | Обеспечение энергией клеток, необходимой для проявления жизни. | |
| АТФ | Молекула АТФ синтезируется в результате переноса электрона от его первичного донора до конечного акцептора. | |
| Дыхание | · Дыхание – биологическое окисление (расщепление). · В зависимости от того, что является конечным акцептором электронов различают дыхание: 1. Аэробное – при аэробном дыхании конечным акцептором электронов служит молекулярный кислород O2. 2. Анаэробное – конечным акцептором электронов служат неорганические соединения: NO3-, SO3-, SO42- | |
| Мобилизация энергии | Энергия мобилизуются в реакциях окисления и восстановления. | |
| Реакция Окисления | Способность вещества отдавать электроны (окисляться) | |
| Реакция Восстановления | Способность вещества присоединять электроны. | |
| Окислительно-восстановительный потенциал | Способность вещества отдавать (окисляться) или принимать (восстанавливаться) электроны. (количественно выражение) |
Схема 2.5. Синтез.

Таблица 2.5.1. Синтез
| № | Название | Характеристика |
| Цитоплазма | В цитоплазме происходит синтез исходных продуктов. | |
| Цитоплазматическая мембрана | Исходные продукты из цитоплазмы переносятся на наружную поверхность цитоплазматической мембраны. | |
| Морфогенез | На ЦПМ начинается морфогенез, то есть образование клеточных структур (капсул, клеточной стенки и др.) при участии ферментов. |
Таблица 2.5.1. Синтез
| № | Биосинтез | Из чего | Примечания |
| I | Биосинтез углеводов | Автотрофы синтезируют глюкозу из CO2. Гетеротрофы синтезируют глюкозу из углеродсодержащих соединений. | Цикл Кальвина (см. схему 2.2.1.) |
| II | Биосинтез аминокислот | Большинство прокариот способны синтезировать все аминокислоты из: · Пирувата · α-кетоглутората · фумората | Источник энергии – АТФ. Пируват образуется в гликолитическом цикле. Ауксотрофные микроорганизмы – потребляют готовые в организме хозяина. |
| III | Биосинтез липидов | Липиды синтезируются из более простых соединений - продуктов метаболизма белков и углеводов | Важную роль играют ацетилпереносящие белки. Ауксотрофные микроорганизмы – потребляют готовые в организме хозяина или из питательных сред. |
Таблица 2.5.2. Основные этапы биосинтеза белка.
| № | Этапы | Характеристика | Примечания | ||||||||
| Транскрипция |  Процесс синтеза РНК на генах.
Это процесс переписывания информации с ДНК – гена на мРНК – ген. Процесс синтеза РНК на генах.
Это процесс переписывания информации с ДНК – гена на мРНК – ген.
| Осуществляется с помощью ДНК – зависимой РНК – полимеразы.
Перенос информации о структуре белка к рибосомам происходит с помощью мРНК. | |||||||||
| Трансляция (передача) | Процесс собственного биосинтеза белка.
 Процесс расшифровки генетического кода в мРНК и осуществление его в виде полипептидной цепи.
Процесс расшифровки генетического кода в мРНК и осуществление его в виде полипептидной цепи.
| Поскольку каждый кодон содержит три нуклеотида, один и тот же генетический текст можно прочитать тремя разными способами (начиная с первого, второго и третьего нуклеотидов), то есть в трех разных рамках считывания. |
Ѻ Примечание к таблице: Первичная структура каждого белка – последовательность расположения в нём аминокислот.
Схема 2.5.2. Цепи переноса электронов от первичного донора водорода (электронов) до конечного его акцептора O2 .
 |
Таблица 3.1. Классификация организмов по типам питания.
| № | Элемент-органоген | Типы питания | Характеристика |
| Углерод (С) | 1. Аутотрофы | Сами синтезируют все углеродосодержащие компоненты клетки из CO2. | |
| 2. Гетеротрофы | Не могут удовлетворять свои потребности за счёт CO2, используют готовые органические соединения. | ||
| 2.1. Сапрофиты | Источник питания – мёртвые органические субстраты. | ||
| 2.2. Паразиты | Источник питания – живые ткани животных и растений. | ||
| Азот (N) | 1. Прототрофы | Удовлетворяют свои потребности с помощью атмосферного и минерального азота | |
| 2. Ауксотрофы | Нуждаются в готовых органических азотистых соединениях. | ||
| Водород (H) | Основным источником является H2O | ||
| Кислород (O) |
Таблица 3.1.2. Превращение энергии
| № | Классификация | Название | Требуется: |
| По источнику энергии | 1. Фототрофы | Солнечный свет | |
| 2. Хемотрофы | Окислительно-восстановительные реакции | ||
| По донору электронов | 1. Литотрофы | Неорганические соединения (H2, H2S, NH3, Fe и др.) | |
| 2. Органотрофы | Органические соединения |
Таблица 3.1.3. Способы углеродного питания
| № | Источник энергии | Донор электронов | Способ углеродного питания |
| Энергия солнечного света | Неорганические соединения | Фотолитогетеротрофы | |
| Органические соединения | Фотоорганогетеротрофы | ||
| Окислительно-восстановительные реакции | Неорганические соединения | Хемолитогетеротрофы | |
| Органические соединения | Хемоорганогетеротрофы |
Таблица 3.2. Механизмы питания:
| № | Механизм | Условия | Градиент концентрации | Затраты энергии | Субстратная специфичность |
| Пассивная диффузия | Концентрация питательных веществ в среде превышает концентрацию в клетке. | По градиенту концентрации | – | – | |
| Облегчённая диффузия | Участвуют белки пермеазы. | По градиенту концентрации | – | + | |
| Активный транспорт | Участвуют белки пермеазы. | Против градиента концентрации | + | + | |
| 3А | Транслокация химических групп | В процессе переноса происходит химическая модификация питательных веществ. | Против градиента концентрации | + | + |
Таблица 3.3. Транспорт питательных веществ из бактериальной клетки.
| № | Название | Характеристика |
| Фосфотрансферазная реакция | Происходит при фосфорилировании переносимой молекулы. | |
| Контрансляционная секреция | В этом случае синтезируемые молекулы должны иметь особую лидирующую последовательность аминокислот, чтобы прикрепиться к мембране и сформировать канал, через который молекулы белка смогут выйти в окружающую среду. Таким образом выходят из клетки соответствующих бактерий токсины столбняка, дифтерии и другие молекулы | |
| Почкование мембраны | Молекулы, образующиеся в клетке, окружаются мембранным пузырьком, который отшнуровывается в окружающую среду. |
Таблица 4. Рост.
| № | Понятие | Определение понятия. |
| Рост | Необратимое увеличение количества живого вещества, наиболее часто обусловленное делением клеток. Если у многоклеточных организмов обычно наблюдается увеличение размеров тела, то у многоклеточных увеличивается количество клеток. Но и у бактерий следует выделять увеличение количества клеток и увеличение клеточной массы. | |
| Факторы, влияющие на рост бактерий in vitro. | 1. Культуральные среды:
· Синтетические, натуральные, полусинтетические (по происхождению)
· Простые и сложные (по составу)
· Жидкие, плотные, полужидкие (по консистенции)
· Накопительные
·  Элективные, основные, дифференциально-диагностические (по целевому назначению)
Mycobacterium leprae не способны in vitro к
Chlamydia росту (внутрикл. паразиты)
2. Температура (растут в интервале):
· Мезофильные бактерии (20-40оС)
· Термофильные бактерии (50-60оС)
· Психрофильные (0-10оС) Элективные, основные, дифференциально-диагностические (по целевому назначению)
Mycobacterium leprae не способны in vitro к
Chlamydia росту (внутрикл. паразиты)
2. Температура (растут в интервале):
· Мезофильные бактерии (20-40оС)
· Термофильные бактерии (50-60оС)
· Психрофильные (0-10оС)
| |
| Оценка роста бактерий | Количественную оценку роста обычно проводят в жидких средах, где растущие бактерии образуют гомогенную суспензию. Увеличение количества клеток устанавливают, определяя концентрацию бактерий в 1 мл, либо определяют увеличение клеточной массы в весовых единицах, отнесённых к единице объёма. |

Таблица 4.1. Факторы роста
| № | Факторы роста | Характеристика | Функция | |
| Аминокислоты | 1. Лейцин 2. Тирозин 3. Аргинин | Многие микроорганизмы, особенно бактерии, нуждаются в тех или других аминокислотах (одной или нескольких), поскольку они не могут их самостоятельно синтезировать. Такого рода микроорганизмы называются ауксотрофными по тем аминокислотам или другим соединениям, которые они не способны синтезировать. | ||
| Пуриновые основания и их производные | Нуклеотиды: 1. Аденин 2. Гуанин | Являются факторами роста бактерий. В нуклеотидах нуждаются некоторые виды микоплазм. Требуются для построения нуклеиновых кислот. | ||
| Пиримидиновые основания и их производные | Нуклеотиды 1. Цитозин 2. Тимин 3. Урацил | |||
| № | Факторы роста | Характеристика | Функция | |
| Липиды | 1. Нейтральные липиды | Входят в состав мембранных липидов | ||
| 2. Фосфолипиды | ||||
| 3. Жирные кислоты | Являются компонентами фосфолипидов | |||
| 4. Гликолипиды | У микоплазм входят в состав цитоплазматической мембраны | |||
| 5. Стеролы | ||||
| Витамины (в основном группы B) | 1. Тиамин (B1) | Золотистый стафилококк, пневмококк, бруцеллы | ||
| 2. Никотиновая кислота (B3) | Все виды палочковидных бактерий | |||
| 3. Фолиевая кислота (B9) | Бифидобактерии и пропионовокислые | |||
| 4. Пантотеновая кислота (B5) | Некоторые виды стрептококков, бациллы столбняка | |||
| 5. Биотин (B7) | Дрожжи и азотфиксирующие бактерий Rhizobium | |||
| Гемы – компоненты цитохромов | Гемофильным бактериям, микобактериям туберкулеза | |||
Таблица 5. Дыхание.
| № | Название | Характеристика |
| Дыхание | Биологическое окисление (ферментативные реакции) | |
| Основание | Дыхание основано на окислительно-восстановительных реакциях, идущих с образованием АТФ – универсального аккумулятора химической энергии. | |
| Процессы | При дыхании происходят процессы: · Окисление – отдача донорами водорода или электронов. · Восстановление – присоединение водорода или электронов к акцептору. | |
| Аэробное дыхание | Конечным акцептором водорода или электронов служит молекулярный кислород. | |
| Анаэробное дыхание | Акцептором водорода или электронов является неорганическое соединение – NO3-, SO42-, SO32-. | |
| Брожение | Акцептором водорода или электронов являются органические соединения. |
Таблица 5.1. Классификация по типу дыхания.
| № | Бактерии | Характеристика | Примечания |
| Строгие анаэробы | · Энергетический обмен происходит без участия свободного кислорода. · Синтез АТФ при потреблении глюкозы в анаэробных условиях (гликолиз) происходит за счет фосфорилирования субстрата. · Кислород для анаэробов не служит конечным акцептором электронов. Более того, молекулярный кислород оказывает на них токсическое действие | · у строгих анаэробов отсутствует фермент каталаза, поэтому накапливающаяся в присутствии кислорода оказывает на них бактерицидное действие; · у строгих анаэробов отсутствует система регуляции окислительно-восстановительного потенциала (редокс-потенциала). | |
| Строгие аэробы | · Способны получать энергию только путём дыхания и поэтому обязательно нуждаются в молекулярном кислороде. · Организмы, получающие энергию и образующие АТФ при помощи только окислительного фосфорилирования субстрата, где окислителем может выступать только молекулярный кислород. Рост большинства аэробных бактерий прекращается при концентрации кислорода в 40—50 % и выше. | К строгим аэробам относят, например, представителей рода Pseudomonas | |
| № | Бактерии | Характеристика | Примечания |
| Факультативные анаэробы | · Растут как в присутствии, так и в отсутствии молекулярного кислорода · Аэробные организмы содержат чаще всего три цитохрома, факультативные анаэробы — один или два, облигатные анаэробы не содержат цитохромов. | К факультативным анаэробам относят энтеробактерии и многие дрожжи, способные переключаться с дыхания в присутствии 02 на брожение в отсутствии 02. | |
| Микроаэрофилы | Микроорганизм, требующий, в отличие от строгих анаэробов, для своего роста присутствия кислорода в атмосфере или питательной среде, но в пониженных концентрациях по сравнению с содержанием кислорода в обычном воздухе или в нормальных тканях организма хозяина (в отличие от аэробов, для роста которых необходимо нормальное содержание кислорода в атмосфере или питательной среде). Многие микроаэрофилы так же являются капнофилами, то есть им требуется повышенная концентрация углекислого газа. | В лаборатории такие организмы легко культивируются в «свечной банке». «Свечная банка» это ёмкость, в которую перед запечатыванием воздухонепроницаемой крышкой вносят горящую свечу. Пламя свечи будет гореть до тех пор, пока не потухнет от недостатка кислорода, в результате чего в банке образуется атмосфера, насыщенная диоксидом углерода, с пониженным содержанием кислорода. |
Таблица 6. Характеристика размножения.
| № | Название | Характеристика |
| Размножение | Термином «размножение» обозначают увеличение числа клеток в популяции. Большинство прокариот размножаются поперечным делением, некоторые почкованием. Грибы размножаются путем спорообразования. | |
| Где происходит | При размножении микробной клетки наиболее важные процессы происходят в ядре (нуклеоиде), содержащем всю генетическую информацию в двунитевой молекуле ДНК |
Схема 6. Зависимость продолжительности генерации от различных факторов.

Таблица 6.1. Фазы размножения бактерий.
| № | Фаза | Характеристика |
| I | Исходная стационарная фаза | Продолжается 1-2 часа. В течение данной фазы число бактериальных клеток не увеличивается. |
| II | Лаг-фаза (фаза задержки размножения) | Характеризуется началом интенсивного роста клеток, но скорость их деления остается невысокой. |
| III | Лог-фаза (логарифмическая) | Отличается максимальной скоростью размножения клеток и увеличением численности бактериальной популяции в геометрической прогрессии |
| IV | Фаза отрицательного ускорения | Характеризуется меньшей активностью бактериальных клеток и удлинением периода генерации. Это происходит в результате истощения питательной среды, накопления в ней продуктов метаболизма и дефицита кислорода. |
| V | Стационарная фаза | Характеризуется равновесием между количеством погибших, вновь образующихся и находящихся в состоянии покоя клеток. |
| VI | Фаза гибели | Происходит в постоянной скоростью и сменяется УП-УШ фазами уменьшения скорости отмирания клеток. |
Схема 7. Требования к питательным средам.

Таблица 7. Размножение бактерий на питательных средах.
| № | Питательная среда | Характеристика |
| Плотные питательные среды | На плотных питательных средах бактерии образуют колонии – скопления клеток. | |
| S – тип(smooth – гладкий и блестящий) Круглые, с ровным краем, гладкие, выпуклые. | R – тип(rough – шершавый, неравный) Неправильной формы с изрезанными краями, шероховатые, вмятые. | |
| Жидкие питательные среды | · Придонный рост (осадок) · Поверхностный рост (плёнка) · Диффузный рост (равномерное помутнение) |
Таблица 7.1. Классификация питательных сред.
| № | Классификация | Виды | Примеры |
| По составу | Простые | 1. МПА – мясо-пептонный агар 2. МПБ – мясо-пептонный бульон 3. ПВ – пептонная вода | |
| Сложные | 1. Кровяной агар 2. ЖСА – желточно-солевой агар 3. Среды Гисса | ||
| По назначению | Основные | 1. МПА 2. МПБ | |
| Элективные | 1. ЖСА 2. Щелочной агар 3. Щелочная пептонная вода | ||
| Дифференциально - диагностические | 1. Эндо 2. Левина 3. Плоскирева 4. Гисса 5. Ресселя | ||
| Специальные | 1. Вильсона-Блера 2. Китта-Тароцци 3. Тиогликолевый бульон 4. Молоко по Тукаеву | ||
| По консистенции | Плотные | 1. Кровяной агар 2. Щелочной агар | |
| Жидкие | 1. МПБ 2. ПВ | ||
| Полужидкие | 1. Полужидкий агар | ||
| По происхождению | Натуральные | 1. МПА 2. МПБ | |
| Полусинтетические | 1. Эндо 2. Сабуро | ||
| Синтетические | 1. Коззера 2. Симмонсона |
Таблица 7.2. Принципы выделения чистой культуры клеток.
| Механический принцип | Биологический принцип |
| МЕТОДЫ 1. Фракционных разведений Л. Пастера 2. Пластинчастых разведений Р. Коха 3. Поверхностных посевов Дригальського 4. Поверхностных штрихов | МЕТОДЫ Приймают во внимание: а - тип дыхания (метод Фортнера); б - подвижность (метод Шукевича); в - кислотоустойчивость; г - спорообразование; д - температурный оптимум; е - избирательную чувствительность лабораторных животных к бактериям |
Таблица 7.2.1. Этапы выделения чистой культуры клеток.
| № | Этап | Характеристика |
| 1 этап исследования | Забирают патологический материал. Его изучают - внешний вид, консистенция, цвет, запахом и другие признаки, готовят мазок, красят и исследуют под микроскопом. | |
| 2 этап исследования | На поверхности плотной питательной среды микроорганизмы образуют сплошной, густой рост или изолированные колонии. Колония– это видимые невооруженным глазом скопления бактерий на поверхности или в толще питательной среды. Как правило, каждая колония формируется из потомков одной микробной клетки (клоны), потому их состав достаточно однороден. Особенности роста бактерий на питательных средах являются проявлением их культуральных свойств. | |
| 3 этап исследования | Изучают характер роста чистой культуры микроорганизмов и проводят ее идентификацию. |
Таблица 7.3. Идентификация бактерий.
| № | Название | Характеристика |
| Биохимическая идентификация | Определение вида возбудителя по его биохимическим свойствам | |
| Серологическая идентификация | С целью установления видовой принадлежности бактерий часто изучают их антигенное строение, то есть проводят идентификацию по антигенным свойствам | |
| Идентификация по биологическим свойствам | Иногда идентификацию бактерий проводят, заражая лабораторных животных чистой культурой и наблюдая за теми изменениями, которые вызывают возбудители в организме | |
| Культуральная идентификация | Определения вида возбудителей по их культуральным признакам | |
| Морфологическая идентификация | Определение вида бактерий по их морфологическим признакам |
Тесты рейтингового контроля
1. Какой из процессов не относится к физиологии бактерий?
a. Рост
b. Размножение
c. Мутация
d. Питание
2. Какие вещества составляют 40 – 80 % сухой массы бактериальной клетки?
a. Углеводы
b. Белки
c. Жиры
d. Нуклеиновые кислоты
3. Какие классы ферментов синтезируют микроорганизмы?
a. Оксиредуктазы
b. Все классы
c. Трансферазы
d. Лигазы
4. Ферменты, концентрация которых в клетке резко возрастает в ответ на появление в среде субстрата-индуктора?
a. Иидуцибельные
b. Конституционные
c. Репрессибельные
d. Мультиферментные комплексы
5. Фермент патогенности, выделяемый золотистым стафилококком?
a. Нейраминидаза
b. Гиалуронидаза
c. Лецитиназа
d. Фибринолизин
6. Протеолитические ферменты выполняют функцию?
a. Расщепление белков
b. Расщепление жиров
c. Расщепление углеводов
d. Образование щелочей
7. Брожение энтеробактерий?
a. Молочнокислое
b. Муравьинокислое
c. Пропионовокислое
d. Маслянокислое
8. Какие минеральные соединения используются для связывания т-РНК с рибосомами?
a. NH4
b. K+
c. Fe2+
Дата добавления: 2015-08-20; просмотров: 408 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Методы выделения чистых культур, основанные на биологическом принципе | | | Вопрос 1 |