
|
Читайте также: |
Перегонкой называется процесс разделения жидких и парогазовых смесей, состоящих из двух или большего числа летучих компонентов.
Сущность процесса заключается в том, что при одной и той же температуре компоненты смеси имеют различную упругость насыщенных паров, т.е. обладают различной летучестью. Компонент, кипящий при более низкой температуре, называется низкокипящим компонентом (НК), а другой компонент (в случае двух компонентных смесей) кипит при более высокой температуре и называется высококипящим компонентом (ВК). Обычно устанавливается определенная температура кипения смеси, которая зависит от её состава и условий проведения процесса. При кипении смеси, состоящих из различных по летучести компонентов, более летучий компонент переходит в паровую фазу в относительно большом количестве, чем менее летучий. Это приводит к обогащению паровой фазы низкокипящим компонентом, а жидкой фазы – высококипящим. Образующиеся пары отводятся в конденсатор, где конденсируются и дистиллят, который представляет собой почти чистый НК, а оставшаяся в аппарате жидкость называется кубовым остатком и представляет собой почти чистый ВК.
Различают простую перегонку (дистилляцию) и сложную перегонку (ректификацию). Простой перегонкой называется процесс однократного испарения и конденсация образующихся паров, а ректификацией – процесс многократного испарения и конденсации паров на так называемых контактных ступенях массообменного аппарата (тарелках) при противоточном движении паровой (снизу вверх) и жидкой (сверху вниз) фаз.
Процесс перегонки широко используется в пищевой промышленности. Особое большое распространение он получил в спиртовой и ликероводочной промышленности, а также в виноделии и производстве эфирных масел. Процесс перегонки применяется также в нефтеперегонном деле, в производстве синтетического каучука, в лесохимической и других отраслях промышленности.
Простая перегонка применяется в тех случаях, когда компоненты смеси сильно различаются по летучести, или когда не требуется большого обогащения дистиллята высококипящим компонентом. Отличительной особенностью простой перегонки по сравнению с ректификацией является постепенное обеднение дистиллята низкокипящим компонентом, а в результате чего первые порции дистиллята получаются наиболее крепкими, а последующие – менее крепкими. Поэтому важным моментом при проведении простой перегонки является время т процесса, течении которого получается требуемый средний состав дистиллята. Этому моменту соответствует вполне определённое количество кубового остатка в аппарате, которое находится на основании уравнения материального баланса.
Пусть в некоторый начальный момент времени в аппарате имеется количество жидкой смеси L, а содержание в ней низкокипящего компонента х. За некоторый промежуток времени d количество жидкости уменьшится и составит (L - dL), а её состав – (x – dx). В соответствии с материальнымбалансом количество образовавшегося пара за этот промежуток времени равняется dG = dL, а содержание в неё низко кипящего компонента y* является равновесным с (x – dx). Тогда материальный баланс по НК выразится уравнением
Lx = (L – dL)(x – dx) + dLy* (1)
Раскрывая скобки и пренебрегая произведением dLdx, как бесконечно малой величиной второго порядка, после разделеня переменных получим

Это дифференциальное уравнение должно быть проинтегрировано в пределах изменения массы жидкости в кубе от начальной L=F до конечной L=W(где W – масса исходной смеси, или питания, и W – масса остатка) и соответствующего падания её концентрации от  до
до 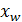 за всю операцию перегонки
за всю операцию перегонки
 =
= 
В результате интегрирования получим
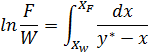
Вид функции 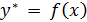 определяется формой кривой равновесия и не может быть установлен аналитически для каждого конкретного случая перегонки. Поэтому интегрирование правой части уравнения (4) проводят графически – путём построения зависимости 1/(
определяется формой кривой равновесия и не может быть установлен аналитически для каждого конкретного случая перегонки. Поэтому интегрирование правой части уравнения (4) проводят графически – путём построения зависимости 1/(
Для ряда значений x в пределах от 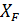 до
до  находят из диаграммы у-х равновесным им значения у* и по размеру площади под кривой, ограниченной абсциссами
находят из диаграммы у-х равновесным им значения у* и по размеру площади под кривой, ограниченной абсциссами  и
и  , определяют (с учётом масштабов диаграммы) значение искомого интеграла.
, определяют (с учётом масштабов диаграммы) значение искомого интеграла.
По уравнению (4), зная массу F загруженной в куб смеси и ее состав  , а также заданный состав остатка
, а также заданный состав остатка  , находят массу остатка W. Масса перегнанной жидкости F – W.
, находят массу остатка W. Масса перегнанной жидкости F – W.
Средний состав  получаемого дистиллята рассчитывают из уравнения материального баланса по низкокипящему компоненту
получаемого дистиллята рассчитывают из уравнения материального баланса по низкокипящему компоненту
 , (5)
, (5)
откуда
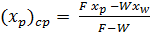 (6)
(6)
Расчёт простой перегонки обычно имеет целью определить массу жидкости, которую необходимо перегнать, для того чтобы получить в кубе остаток заданного состава и дистилля требуемого среднего состава.
Пустую перегонку проводят при атмосферном давлении или под вакуумом, присоединяя сборники дистиллята к источнику вакуума. Применение вакуума даёт возможность разделять термически малостойкие смеси и, вследствие понижения температуры кипения раствора, использовать для обогрева куба пар более низких параметров.
Интеграл в правой части уравнения (4) может быть найден графическим способом при известной линии равновесия для данной смеси, т.е. зависимости у* = f(x). Для этого по оси абсцисс откладывают значения концентрации НК в жидкости х, а по оси ординат – величину 1/у* - х) (рис. 1). Площадь под кривой в пределах от 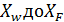 выражает числовое значение интеграла в правой части уравнения (4) (рис.1).
выражает числовое значение интеграла в правой части уравнения (4) (рис.1).
Пример:
Определить графически величину интеграла 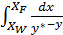
Принятый масштаб на рис.1.
- по оси ординат 1 см – 1
- по оси абсцисс 1 см – 0,01
1  =0,01
=0,01
При площади, определяющей значение интеграла в пределах 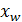 =0.017 и
=0.017 и 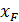 =0.09 (мольные доли), равной 28,75
=0.09 (мольные доли), равной 28,75  , получим
, получим
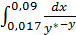 =28,75 * 0,01 = 0,2875,
=28,75 * 0,01 = 0,2875,
следовательно
 = 0,2875,
= 0,2875,
откуда
 = 1,3335, кг
= 1,3335, кг
Уравнение по условию задано F, то W =F/1.3335, кг
Уравнение теплового баланса простой перегонки
Q=  +
+ 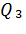 (7)
(7)
Количество теплоты на подогрев исходной смеси от  до
до 
 = (
= ( + F(1-
+ F(1-  )
)  )(
)( -
-  ) (8)
) (8)
Где  - теплоёмкость спирта (определяется по номограмме в зависимости от температуры), кДж/(кг*К);
- теплоёмкость спирта (определяется по номограмме в зависимости от температуры), кДж/(кг*К);  =4,19 кДж/(кг*К) – теплоёмкость воды;
=4,19 кДж/(кг*К) – теплоёмкость воды;  – концентрация спирта в исходной смеси, масс.доли.
– концентрация спирта в исходной смеси, масс.доли.
Количество теплоты на испарение смеси при 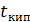
 =((F - W)
=((F - W) 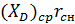 + (F – W)(1-
+ (F – W)(1- 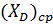 )
)  ) (9)
) (9)
Где  = 855 кДж/кг – теплота парообразования спирта,
= 855 кДж/кг – теплота парообразования спирта,  = 2290 кДж/кг – теплота парообразования воды.
= 2290 кДж/кг – теплота парообразования воды.
Количество теплоты на нагрев кубового остатка от  до
до 
 = (W
= (W  + W (1 -
+ W (1 -  )
)  )(
)( -
-  ) (10)
) (10)
Цель работы
– изучить процесс простой перегонки бинарной смеси этиловый спирт–вода. Определить среднюю концентрацию дистиллята и к.п.д. установки.
Описание экспериментальной установки
Установка для простой перегонки состоит из перегонного куба 1 (рис.2) с двумя электронагревателями (ТЭН) 2, соединённого трубопроводом 3 с конденсатором 4, внутри которого установлен змеевиковый трубчатый охладитель 5.
Установка работает следующим образом.
Общее включение напряжения питания осуществляется автоматом 6, установленным справа на стенке щита управления 7. Исходная смесь, предварительно взвешенная, заливается в перегонный куб 1 через воронку 8. Одновременно контролируется уровень жидкости в кубе 1 по водомерному стеклу 9. Уровень не должен быть ниже красной черты, соответствующей полному погружению ТЭНов в жидкость. После заливки воронка 8 вывинчивается и отверстие закрывается специальной заглушкой. Подача воды в конденсатор 4 осуществляется от водопроводной сети через запорный вентиль 10 и расходомер 11. Слив воды осуществляется лагометром 13 по термометрам сопротивления 14,15. Переключение режима измерения температуры с термометра 14 на термометр 15 осуществляется тумблером 16.
Установка и поддержание заданного давления в перегонном кубе 1 осуществляется электроконтактным манометром (ЭКМ) 17.
Включение и отключение электронагревателей 2 осуществляется кнопочной станцией 18. Визуальный контроль включения ведётся по сигнальным лампочкам 19. Переключение режима нагрева с одного на два ТЭНа осуществляется пакетным выключателем 20. Плавная регулировка напряжения питания на ТЭНах 2 возможно ручкой 21 лабораторного автотрансформатора (ЛАТР). Контроль напряжения питания и тока в системе питания ТЭНов 2 осуществляется амперметром 22 и вольтметром 23.
Отбор проб и полная разгрузка конденсатора 4 и перегонного куба 1 возможна через винтили 24,25. Измерение объёма проб осуществляется мерным стаканом 26.
Методика проведения эксперимента
1 Построить для исходной смеси (спирт – вода) кривую равновесия у –х и диаграмму t –xy (см. Приложение 1).
2 С помощью ареометра измерить плотность раствора исходной смеси и по таблице (см. Приложение 2) определить его концентрацию 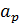 в масс. %.
в масс. %.
3 Исходный раствор (в количестве, заданном преподавателем) залить в перегонный куб 1 и определить его объём по водомерному стеклу 9.
4 Начальную температуру исходной смеси  , найти по показаниям лагометра 13, подключённого к термометру сопротивления 14.
, найти по показаниям лагометра 13, подключённого к термометру сопротивления 14.
5 По диаметру t – xy определить температуру кипения исходной смеси  при наличии её концентрации
при наличии её концентрации  (в мольных долях). Для этого концентрацию спирта в исходной смеси их массовых процентов
(в мольных долях). Для этого концентрацию спирта в исходной смеси их массовых процентов  перевести в мольные доли по формуле
перевести в мольные доли по формуле
Где 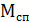 ,
,  – соответственно молекулярная масса спирта и воды.
– соответственно молекулярная масса спирта и воды.
6 Одновременно включить секундомер и электронагреватели 2. Снять показания амперметра 22 и вольтметра 23 на щите управления.
7 Открыть вентиль на линии подачи охлаждающей воды в змеевиковый трубчатый охладитель 5 конденсатора 4 (расход воды указывается преподавателем).
8 Отметить по секундомеру (не выключая его) время подогрева смеси спирт-вода  до температуры кипения
до температуры кипения  , ранее определённой по диаграмме t – xy/
, ранее определённой по диаграмме t – xy/
9 По истечению некоторого времени (по указанию преподавателя) выключить секундомер и определить время перегонки  , отключить нагрев и охлаждающую воду.
, отключить нагрев и охлаждающую воду.
10 Отобрать три пробы дистиллята и одну пробу кубового остатка в мерные цилиндры 26, охладить их до комнатной температуры (15-20 ℃). С помощью ареометра определить плотности растворов в пробах и найти их концентрации в масс. %.
11 Измеренные значения величин занести в табл. 1.
Таблица 1
Обработка экспериментальных данных
1 Концентрации спирта в исходной смеси 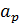 , в кубковом остатке
, в кубковом остатке  и в дистилляте
и в дистилляте  из % масс. Перевести в мольные доли
из % масс. Перевести в мольные доли  ,
,  ,
, 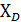 по формуле (11).
по формуле (11).
2 На основании уравнения (4) определить количество кубового остатка W, предварительно вычислив величину интеграла  .
.
Для этого необходимо выписать данные по равновесию смеси и записать в табл. 2.
Таблица 2
В координатах 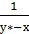 – х построить график (рис. 1). Площадь под кривой в найденных пределах
– х построить график (рис. 1). Площадь под кривой в найденных пределах 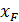 и
и 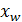 представляет значение искомого интеграла (см. пример расчёта).
представляет значение искомого интеграла (см. пример расчёта).
3 Из уравнения материального баланса по всему веществу определить количество дистиллята D
D=F-W, кг
4 Рассчитать средний состав полученного дистиллята из уравнения материального баланса по низкокипящему компоненту (спирту)
5 Вычислить погрешность в определении концентрации дистиллята
6 Определить общее количество теплоты на перегонку по уравнению (7).
7 Рассчитать мощность, затраченную на перегонку
8 Определить мощность, потребляемую электронагревателями
9 Определить к.п.д. у становки
Отчёт по работе
1 Цель работы, краткие теоретические сведения, схема и описание экспериментальной установки, порядок проведения работы и вычислений.
2 Опытные и расчётные данные, кривая равновесия у-х и диаграмма t-xy.
3 Результаты расчётов.
4 Выводы по работе.
Вопросы для самопроверки
1 Что называется простой перегонкой?
2 В чём заключается сущность процессов перегонки?
3 Чем обогащается паровая фаза, а чем – жидкая?
4 в каких случаях применяют пустую перегонку, а в каких – сложную?
5 Недостатки простой перегонки?
6 какие основные параметры необходимо контролировать в процессе простой перегонки?
7 Из каких аппаратов состоит установка для простой перегонки?
8 Как определяется температура кипения смеси?
9 На что расходуется теплота в простой перегонке?
10 Как определяется к.п.д. перегонной установки?
Дата добавления: 2015-08-17; просмотров: 90 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Введение | | | Далее открываем каталог товаров (также можно выбрать товар с сайта, там есть ссылка на сайт) |