
| SiO2 | Al2O3 | FeO | Fe2O3 | MnO | CaO | MgO | P2O5 | S | CO2 | H2O | Сумма |
| 0,099 | 0,06 | – | – | – | 2.979 | 0,07 | – | 0,003 | 0,099 | – | 3.31 |
Рассчитанное количество извести обеспечит необходимую основность только в том случае, если все количество СаО растворяется в шлаке, образуя гомогенный расплав. Так как часть извести (мелочь) выдувается при загрузке, то приходится загружать извести несколько больше расчетного количества. Согласно практическим данным указанные потери извести принимаем равными 25 % от расчетного количества. Следовательно, в конвертер необходимо загрузить 3.31 · 1,25 = 4.14 кг извести (см. табл. 2.5).
Таблица 2.5
Вещества, переходящие в шлак (кроме окислов железа)
из различных источников (в кг)
| SiO2 | Al2O3 | MnO | CaO | MgO | P2O5 | S | Сумма | |
| Из 6,19 кг извести | 0,099 | 0,06 | – | 2.979 | 0,07 | – | 0,03 | 3.238 |
| Из источников, приведенных в табл. 2.3 | 0.778 | 0,04 | 0,293 | 0,15 | 0,10 | 0,167 | 0,029 | 1.557 |
| Вес шлака без оксидов железа | 0.877 | 0,1 | 0.293 | 3.129 | 0,17 | 0,167 | 0,032 | 4.768 |
Содержание оксидов железа в ходе LD-процесса зависит от многих факторов: концентрации углерода в металле, температуры, основности шлака, давления дутья, интенсивности продувки, количества сопел в фурме, положения фурмы (высоты выходного сечения над металлом) и т.д. Причем вклад отдельных факторов может изменяться в зависимости от величины остальных. В настоящее время еще недостаточно фактического материала, который позволил бы учесть влияние всех перечисленных факторов. Особенно трудно учесть количественно влияние положения фурмы, давления дутья, интенсивности продувки и количества сопел в фурме.
| Изм. |
| Лист |
| № докум. |
| Подпись |
| Дата |
| Лист |
| КП.150101.9ЧМ51.ПЗ |
Для определения окисленности шлака при более низких содержаниях углерода в металле в конце продувки, в работе [1] рекомендуется следующая эмпирическая формула:
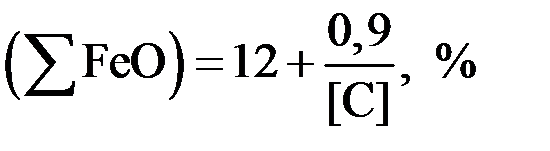 .
.
При [C] = 0,045 %, основности шлака 2,5, температуре металла в конце продувки 1620 оС общее содержание оксидов железа в шлаке равно

В конечных шлаках кислородно-конвертерного процесса отношение двухвалентного железа к трехвалентному можно принять равным примерно трем.
Поэтому концентрация FeO в шлаке равна (см. табл. 2.6)
2 / 3 · 32 = 21.3 %,
а общее количество железа в шлаке в виде оксидов составит
32 · (56/72) = 24.9 %.
Концентрация Fe2O3 в шлаке определяется из уравнения
(Fe2O3, %) ּ (112/160) + (FeO, %) ּ (56/72) = (Fe, %),
| Изм. |
| Лист |
| № докум. |
| Подпись |
| Дата |
| Лист |
| КП.150101.9ЧМ51.ПЗ |
Fe2O3 = 11.90 %,
FeO + Fe2O3 = 33.2 %.
Вес шлака без оксидов железа (см. табл. 2.5) равен 4.768 кг. Поэтому количество FeO и Fe2O3 в шлаке составит (см. табл. 2.6):
FeO =  · 21.3= 1.81кг;
· 21.3= 1.81кг;
Fe2O3 =  · 11.90= 1.01 кг.
· 11.90= 1.01 кг.
Таблица 2.6
Дата добавления: 2015-08-20; просмотров: 73 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| К концу продувки (в кг) | | | Расчет количества стали, получающейся из 100 кг чугуна |