
|
Читайте также: |
В общем случае крекингомназывают процесс расщепления углеводородов на несколько более мелких молекул под действием повышенных температур (термический крекинг). Если его осуществляют в присутствии катализатора, то он называется каталитическим крекингом. Продукты термического и каталитического крекинга отличаются друг от друга вследствие различного механизма протекания реакций.
Целевым продуктом процесса каталитического крекинга является бензиновая фракция, имеющая высокое октановое число, которое в основном обеспечивают представители таких групп углеводородов, как арены, алкены и алканы разветвленного строения. В то же время при протекании реакций термического крекинга идет обогащение продуктов в основном алкенами и алканами с неразветвленной углеродной цепью. В связи с этим на современных установках каталитического крекинга для повышения качества получаемого бензина необходимо создать условия для предотвращения термического крекинга углеводородов.
Вследствие большого числа индивидуальных веществ, входящих в состав сырья, невозможно описать все химические реакции, протекающие при крекинге нефтяных фракций. Поэтому либо ограничиваются рассмотрением реакций, которые присущи веществам, относящимся к одной группе углеводородов (арены, алкены, алканы, циклоалканы, углеводороды смешанного гибридного строения), либо описывают схемы, учитывающие основные направления, конечные и промежуточные продукты крекинга. При этом конечные и промежуточные продукты разделяют по фракционному составу (по температурам кипения) на газ (до 28оС), бензин (28-200оС), легкий (200-350оС) и тяжелый (свыше 350оС) газойли, а также кокс. При таком подходе становится наглядной схема последовательно-параллельных реакций расщепления молекул нефтяного сырья (рис.1.1). Однако она не учитывает изменения состава продуктов в результате превращения молекул одних групп углеводородов в другие.

Рисунок 1.1 – Схема основных превращений сырья в процессе каталитического крекинга
В зависимости от условий крекинга (состав сырья, свойства катализатора, температура, продолжительность контакта сырья с катализатором, кратность последнего к сырью и т.п.) интенсивность протекания тех или иных реакций существенно изменяется, что оказывает непосредственное влияние на выход и качество получаемых продуктов. В связи с этим для более точного прогнозирования результатов каталитического крекинга необходимо рассматривать не только реакции, связанные с разрывом
С-С связи, но и с изменением углеродного скелета молекул.
1.1 Основные химические реакции различных компонентов сырья
Наиболее важными реакциями каталитического крекинга являются следующие:
- крекинг алканов (парафиновых углеводородов);
- крекинг циклоалканов (нафтеновых углеводородов) с образованием алкенов (непредельных углеводородов);
- деалкилирование (отрыв боковой цепи) алкилароматических углеводородов;
- расщепление боковых цепей алкилароматических и раскрытие нафтеновых колец нафтено-ароматических (гибридных) углеводородов;
- крекинг непредельных углеводородов с образованием алкенов меньшей молярной массы;
- изомеризация алканов и алкенов;
- перераспределение алкильных групп между ароматическими углеводородами;
- диспропорционирование алкенов с низкой молярной массой;
- перераспределение водорода;
- полимеризация алкенов, конденсация аренов и коксообразование.
Реакционная способность углеводородов по отношению к разрыву связи С–С убывает в такой последовательности: алкены и циклоалкены > арены (ароматические углеводороды) с числом атомов углерода в алкильной группе более 3 > нафтеновые и изопарафиновые углеводороды > нафтено-ароматические > н-парафиновые > полиметилбензолы > моноалкилбензолы с числом атомов углерода менее 3.
В связи с тем, что реальное сырье состоит из смеси большого количества различных углеводородов, при каталитическом крекинге одновременно протекают все перечисленные выше реакции.
Алканы и циклоалканы. В зависимости от природы нефтей суммарное количество алканов (парафиновых углеводородов) в них изменяется от 20 до 60%, а при переходе к вакуумным фракциям их содержание обычно уменьшается. Они в нефтяных системах представлены н-алканами, имеющими прямую углеродную цепь, и изо-алканами, характерным признаком которых является разветвленная углеродная цепь. Примерами таких углеводородов могут служить н-гексан и 2,3-диметилбутан:
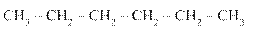

н-гексан 2,3-диметилбутан
Очень часто атомы углерода (С) и водорода (Н) в таких структурных формулах не показывают и поэтому схематичное изображение этих углеводородов выглядит следующим образом:


Алканы являются насыщенными углеводородами (каждый атом углерода связан с четырьмя соседними атомами – углерода и водорода) и описываются формулой СnН2n+2. В нефтях содержание н-алканов составляет 1-20%. Существует два вида нефтей, резко отличающихся распределением этих углеводородов. Наиболее распространенными являются нефти типа Сургутской, Понка и другие, в которых н-алканы концентрируются в основном в легких фракциях, а в тяжелых – содержатся в ограниченных количествах. Значительно реже встречаются нефти, у которых максимум содержания н-алканов приходится на углеводороды С15-С22.
При температуре хранения ниже 20-25°С н-алканы, присутствующие в вакуумных дистиллятах, образуют твердую фазу и в этом состоянии имеют кристаллическое строение. Поэтому прямогонные и особенно гидроочищенные вакуумные фракции при комнатной температуре, как правило, находятся в виде твердого вещества (температура застывания 28-38°С).
Изоалканы более многочисленны и разнообразны по своему строению, чем н-алканы. Из монозамещенных изомеров наиболее распространены в вакуумных фракциях 2- и 3-метилалканы.
При каталитическом и термическом крекинге крупного алкана в результате разрыва связей С-С образуется минимум две более мелких молекулы, содержащих, как правило, 3 и более атомов углерода – одна алкана (в том числе, может быть, н-алкана) и вторая – непредельного углеводорода:

Расщепление углеродной цепи происходит ближе к ее середине по
b-связи (a-связь – соответствует соединению группы СН3 к остальной части углеродного скелета молекулы углеводорода). При каталитическом крекинге скорость такого распада только в 30-60 раз выше, чем при термическом крекинге. Поэтому при дезактивации катализатора или существенном отклонении режима процесса резко возрастает доля реакций термического крекинга алканов, особенно неразветвленного строения, что приводит к падению октанового числа получаемого бензина. В связи с этим большое содержание алканов (особенно н-алканов) в сырье каталитического крекинга является не очень желательным.
Расщепление углеродной цепи по b-связи объясняет тот факт, что газы крекинга в основном состоят из предельных и непредельных углеводородов С3-С4, а метан, этан и этилен присутствуют в незначительных количествах.
Кроме разрыва углеродной цепи при использовании катализаторов велика вероятность протекания, в отличие от термического крекинга, реакции изомеризации алканов и алкенов:

(R- углеводородный радикал неразветвленного строения)

Поэтому при каталитическом крекинге алканов получаемый бензин имеет более высокое октановое число по сравнению с бензином термического крекинга.
Изоалканы крекируются легче и глубже по сравнению с н-алканами. При этом водорода и метана получается больше, а образующиеся фракции С4-С6 содержат меньше непредельных углеводородов, так как гидрирование (присоединение водорода по двойным связям С=С) разветвленных молекул алкенов происходит легче, чем неразветвленных.
Циклоалканы (нафтеновые углеводороды), как и алканы, относятся к насыщенным соединениям. Отличительной их особенностью является наличие в структуре молекулы нафтенового кольца, которое может быть образовано 3-12 и более атомами углерода, например:


циклогексан циклопентан
Схематичное изображение этих углеводородов выглядит соответственно:


циклогексан циклопентан
Циклоалканы, как правило, наиболее представительные соединения в нефтях и их содержание часто колеблется в интервале 40-70% мас. По своему строению они различаются как количеством атомов углерода в цикле и числом циклов в молекуле, так и строением заместителей. Обычно их содержание растет по мере утяжеления нефтяных фракций. В зависимости от размера цикла нафтеновые углеводороды подразделяют на малые (С3, С4), нормальные (С5-С7), средние (С8-С11) и макроциклы (более С12). Наибольшей устойчивостью отличаются 5- и 6-членные циклы, в связи с чем они преобладают в нефтях.
Существуют моно-, би- и полициклические циклоалканы. Бициклические нафтеновые углеводороды в нефтях представлены соединениями типа декалина, норборнана, бициклооктанов, бициклононанов, а трициклические – гомологами адамантана, пергидрофенантрена и пергидроантрацена:



декалин норборнан бициклооктан (пенталон)


бициклононан адамантан
(гидриндан)


пергидрофенантрен пергидроантрацен
Обще количество полициклических циклоалканов невелико, и они не оказывают большого влияния на характер протекающих реакций.
В тяжелых нефтяных фракциях молекулы циклоалканов содержат от 1 до 6 циклов, однако основная часть циклоалканов имеет 1-3 цикла (I, II). Методом хромато-масс-спектроскопии идентифицированы углеводороды ряда 1, 1, 3-триметил, 2-алкилциклогексана состава С10-С22 (I):
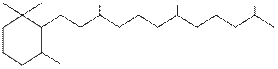

(I) (II)
Нафтеновые углеводороды вакуумных дистиллятов различаются не только по числу колец в молекуле, но и по их природе. Соотношение шести- и пятичленных колец в смесях циклоалканов можно вычислить, исходя из того, что при одной и той же молярной массе их плотности достаточно сильно разнятся. С увеличением молярной массы содержание пятичленных циклов в нефтяных фракциях снижается.
Сырье, богатое нафтеновыми углеводородами, является желательным для процесса каталитического крекинга, так как при его использовании достигается высокий выход качественного бензина при низкой скорости образования кокса. Моно- и полициклические нафтеновые углеводороды с длинными алкильными цепями в условиях крекинга подвергаются реакциям деалкилирования (а), раскрытия кольца с образованием алке-
нов (б, в), дегидрирования (г):

(а)

(б)
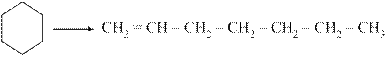
(в)

(г)
Дальнейшее превращение непредельных углеводородов, образовавшихся при крекинге циклоалканов, приводит к возникновению, как минимум, в два раза большего количества низкомолекулярных алкенов:

В результате этого в продуктах крекинга циклоалканов присутствуют ароматические углеводороды, много алкенов и мало алканов, причем в значительной степени разветвленного строения. Вследствие этого октановое число* получаемых в процессе каталитического крекинга бензинов увеличивается при росте в сырье содержания циклоалканов (рис. 1.2).

Рисунок 1.2 – Зависимость октанового числа бензина (ИМ) от соотношения циклоалканов и алканов в сырье двух установок российских НПЗ, перерабатывающих различные типы нефтей
Арены и гибридные углеводороды. Отличительным признаком аренов (ароматических углеводородов) является наличие в молекуле одного или нескольких бензольных колец. Типичным представителем моноциклических аренов является бензол:
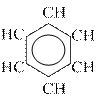
 (схематичное изображение)
(схематичное изображение)
Взаимодействие p-электронов в нем приводит к сопряжению углерод-углеродных связей. Следствием этого являются следующие свойства аренов:
- эквивалентность всех С – С связей в незамещенных моноциклах;
- плоское строение цикла с длинами связей С–С, занимающими промежуточное значение между простой и двойной связью;
- склонность к реакциям электрофильного замещения водорода на различные группы.
Ароматические углеводороды обнаружены во всех нефтях и присутствуют во всех фракциях, выкипающих выше 80°С. Арены представлены различными гомологическими рядами: моноциклические – гомологами бензола, бициклические – нафталина и дифенила, трициклические – фенантрена и антрацена. В основном с ростом молярной массы нефтяных фракций общее содержание в них аренов возрастает. Однако количество полициклических ароматических углеводородов снижается с увеличением бензольных колец в молекуле. В высококипящих фракциях ароматические фрагменты часто входят в состав гибридных соединений. С некоторыми полярными соединениями арены образуют достаточно устойчивые комплексы, что является очень важным с технологической и экологической точек зрения.
Масс-спектрометрическим методом установлено, что типичная молекула алкилбензола тяжелых нефтяных фракций содержит несколько метильных или этильных групп и один длинный алкильный заместитель:

В вакуумных дистиллятах обнаружены также моноароматические углеводороды состава С32-С35, содержащие до 5 насыщенных циклов:
 где R – Н, CН3, С2Н5
где R – Н, CН3, С2Н5
Из нефтей выделены и идентифицированы фенантрен, антрацен, пирен, флуорен, циклопентанфенантрен, хризен, бензперилен и коронен:



фенантрен антрацен пирен



флуорен циклопентафенантрен хризен


бензперилен каронен
Крекинг ароматических и содержащих ароматические фрагменты гибридных углеводородов сопровождается протеканием реакций деалкилирования и конденсации. При деалкилировании алкилароматических углеводородов сырья образуются низкомолекулярные алкеновые и ароматические углеводороды (голоядерные или с более короткими боковыми цепями):

Скорость крекинга боковой цепи гибридных углеводородов возрастает при переходе от первичного (атом углерода образует связь только с одним атомом углерода и тремя – водорода) ко вторичному (атом углерода образует связь с двумя атомами углерода и двумя – водорода) и третичному атому углерода (атом углерода образует связь с тремя атомами углерода и одним – водорода), связанному с ароматическим ядром. В пределах данного класса веществ скорость крекинга увеличивается с удлинением длины боковой цепи. Метильные группы (первичный атом углерода) при крекинге легко мигрируют по ароматическому ядру, но от него, как правило, не отщепляются:

Ароматические углеводороды могут конденсироваться с образованием вначале полициклических структур, а затем асфальтенов и кокса:

Поэтому при переработке сырья со значительным содержанием ароматических углеводородов (особенно полициклических) при одинаковой глубине превращения образуется значительно больше кокса, чем при переработке сырья, содержащего преимущественно моноциклические ароматические углеводороды.
Следует иметь в виду, что термодинамические условия крекинга (температура, давление) не позволяют раскрывать бензольные кольца ароматических соединений, которые содержатся в больших количествах в утяжеленных видах сырья. Поэтому реакции разрыва бензольного кольца для этого процесса не характерны.
Конденсация аренов, как и полимеризация образующихся при их деалкилировании олефинов, приводит к высоким выходам водорода и кокса, а также к получению повышенного количества тяжелого газойля. При этом выход бензина и его октановое число снижаются. Кроме того, замечено, что полициклические ароматические углеводороды тормозят крекинг алканов и циклоалканов. В связи с этим, присутствие ароматических углеводородов, особенно полициклических, в сырье процесса каталитического крекинга является нежелательным.
Гетероатомные соединения нефти представлены разнообразными серу-, азот- и кислородсодержащими структурами. В больших количествах они являются нежелательными компонентами сырья каталитического крекинга, так как или ухудшают экологические показатели получаемых топлив, или являются коррозионно-активными веществами, или ядами для катализаторов. Гетероатомные соединения обладают склонностью к структурированию и часто выполняют роль природных поверхностно-активных веществ. При подготовке сырья для каталитического крекинга их следует удалять из нефтяных фракций. Для этого обычно используют гидрогенизационные процессы.
Сернистые соединения – наиболее распространенные и изученные гетероатомные вещества нефтяных фракций. Содержание серы в нефтях колеблется от сотых долей до 5-7%. Эти вещества иногда составляют более половины всех гетероатомных соединений и представлены в основном различными типами тиолов (R-SH, меркаптаны), тиоэфиров (R-S-R, сульфиды), дисульфидов (R-S-S-R),


тиофанов, тиофенов, и их производных.
Одним из основных видов сернистых соединений вакуумных дистиллятов являются сульфиды. С повышением температуры кипения нефтяных фракций уменьшается доля алкилсульфидов и возрастает доля моноциклических, а затем полициклических сульфидов. Основную их часть во многих нефтях составляют тиоцикланы, содержащие до 7 конденсированных нафтеновых колец. Атом серы в тиоцикланах расположен преимущественно в a-положении по отношению к соседнему циклу и поэтому трудно удаляется при гидроочистке.
Наименее стабильны меркаптаны, ди- и полисульфиды, которые обычно расщепляются при температурах до 100-110°С. Сульфиды более устойчивы, а тиофены подвергаются деструкции при температурах выше 360-370°С. При распаде сернистых соединений образуются сероводород и, так называемая, “ активная сера ”, которые вызывают коррозию металлов. Кроме этого, сгорая в двигателях вместе с компонентами топлив, они образуют оксиды серы, отрицательно влияющие на окружающую среду. В связи с этим присутствие данного класса соединений в нефтепродуктах является нежелательным.
Азотистые соединения представлены в нефтях преимущественно циклическими веществами основного и нейтрального характера и их содержание обычно колеблется в пределах от 0,02 до 0,4% мас., однако иногда может достигать 1,5 и более процентов. Общее содержание азота в вакуумных дистиллятах составляет от 0,06 до 0,16%. Нередко до 95% имеющихся в нефти атомов азота сосредоточены в смолах и асфальтенах. В вакуумных дистиллятах среди соединений азота могут присутствовать алкилзамещенные пиридина, хинолина и бензохинолина. В относительно больших количествах в них встречаются гомологи карбазола и бензкарбазола:



пиридин хинолин бензохиналин


карбазол бенкарбазол
Азотистые соединения отрицательно сказываются на эксплуатационных свойствах катализаторов крекинга. Обладая основным характером, они нейтрализуют кислотные центры катализатора, в результате чего он теряет свои каталитические свойства.
Кислородсодержащие соединения в нефтях составляют в среднем от 0,1 до 1,0% мас. Значительная часть кислорода сосредоточена в смолисто-асфальтеновых веществах.
Анализ кислородсодержащих соединений, выделенных из вакуумных дистиллятов различных нефтей, показал, что основными из них являются карбоновые кислоты, фенолы, кетоны, сложные эфиры, фурановые производные и спирты. Наиболее распространены соединения кислого характера – карбоновые кислоты и фенолы. Кроме алифатических и нафтеновых кислот обнаружены и кислоты ароматического и гибридного характера следующего строения:




В кислых компонентах, выделенных из фракций 370-535°С и 535-675°С различных нефтей, идентифицированы соединения ряда
о-фенилфенола:
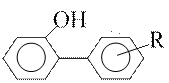
Суммарное количество кислот и фенолов обычно оценивают кислотным числом – количеством миллиграммов КОН, пошедшим на титрование 1 грамма нефтепродукта.
Отрицательного воздействия на катализатор крекинга и экологические характеристики получаемых топлив кислородсодержащие соединения не оказывают. Однако они могут концентрироваться в образующейся в процессе крекинга кислой воде и в случае сброса ее на очистные сооружения завода создадут существенные проблемы экологического характера.
Смолисто-асфальтеновые вещества (САВ) концентрируются преимущественно в тяжелых нефтяных остатках и, в зависимости от глубины отбора дистиллятных фракций, составляют в них до 60-70% мас. Для САВ характерны обменные, диполь-дипольные взаимодействия, водородные связи. В результате этого молекулы асфальтенов образуют между собой и со смолами стойкие ассоциаты.
Из-за трудности разделения и идентификации индивидуальных веществ остаточных фракций их характеристикой служит количественное содержание групповых компонентов. Исследование тяжелых остатков начинается с выделения асфальтенов путем осаждения их низшими алканами. Затем углеводородную часть с помощью адсорбционной хроматографии делят на парафино-нафтеновые, моно-, би- и полициклические соединения, толуольные и спирто-толуольные смолы. Парафино-нафтеновые, моно- и бициклические нафтеновые и ароматические соединения нефтяных остатков имеют молярную массу в среднем 400-600 кг/кмоль.
В состав САВ принято включать смолы, асфальтены, карбены и карбоиды. Карбоиды – вещества нерастворимые в сероуглероде. Карбены – вещества растворимые в сероуглероде, но нерастворимые в тетрахлоруглероде. Асфальтены растворимы в бензоле, сероуглероде, тетрахлоруглероде, но не растворимы в низкокипящих алканах. Смолы же растворимы во всех нефтяных фракциях, в том числе и низкокипящих алканах.
Асфальтены представляют собой твердые вещества темно-бурого или черного цвета. При 250-300°С они переходят в пластическое состояние, вспениваются, а при большей температуре разлагаются с образованием кокса и газа. Обычно асфальтены образуют между собой прочные ассоциаты пачечного строения, в состав которых входит 4-5 молекул. Средний элементный состав асфальтенов следующий (% мас.): углерод – 80-84%, водород – 7,5-8,5%, сера – 4,6-8,3%, кислород – до 6%, азот – 0,4-1% и другие элементы, включая металлы (железо, никель, кобальт, натрий, магний, ванадий и т.д.). Содержание гетероатомов в них намного больше, чем в маслах и смолах. Ассоциаты асфальтенов образуют ядра дисперсной фазы нефтяных остатков.
Смолы при обычной температуре – это твердые вещества. Они относятся к высокомолекулярным органическим соединениям циклической и гетероциклической структуры высокой степени конденсации, фрагменты которых связаны между собой алифатическими цепями. Смолы хорошо растворимы во всех нефтяных фракциях. Их элементный состав представлен кроме углерода (79-87% мас.) и водорода (8,5-9,5% мас.), кислородом (1-16% мас.), серой (1-10% мас.), азотом (до 2% мас.), а также другими элементами. По своей природе и потенциалу межмолекулярных взаимодействий смолы близки к асфальтенам. Поэтому в нефтяных системах, в которых в качестве дисперсной фазы присутствуют асфальтены, они, как правило, образуют адсорбционно-сольватные оболочки. Смолы характеризуются более высоким отношением водорода (Н) к углероду (С), чем асфальтены. Они, обладая хорошей растворимостью в углеводородах нефти, способствуют образованию стабильной системы: асфальтены-смолы-масла. Молекулы смол являются структурными блоками, из которых в результате протекания реакций дегидрирования, уплотнения и конденсации образуются молекулы асфальтенов. Смолы отличаются от асфальтенов по молекулярно-массовому распределению. Для смол (первичного происхождения) оно составляет 460-1600, а для асфальтенов 1600-6000 атомных единиц. В результате термических и термоокислительных процессов в нефти и нефтепродуктах могут образовываться смолы и асфальтены вторичного происхождения согласно схеме:
Полициклические арены ® смолы ® асфальтены ® карбены ® карбоиды
Смолы и асфальтены вторичного происхождения имеют значительно меньшие молярные массы, отличаются высокой степенью конденсации и малым содержанием насыщенных радикалов. Поэтому дисперсные системы, образованные ими, как правило, менее устойчивы к расслоению, чем остатки перегонки нефти.
Карбены и карбоиды в сырой нефти обычно отсутствуют. Они являются результатом термических и термокаталитических превращений асфальтенов и смол.
В молекулах смол и асфальтенов в значительных количествах содержатся гетероатомные включения. Так, атомы азота встречаются во фрагментах пиридинового, пиррольного и порфиринового характера; атомы серы – в виде сульфидных, тиольных групп и в составе тиофеновых циклов; атомы кислорода – в виде гидроксильных, карбоксильных, эфирных, карбонильных групп и фурановых колец. Определить точное строение смол и асфальтенов современными экспериментальными методами чрезвычайно сложно вследствие их большого разнообразия. Поэтому предлагаются различные гипотетические модели.
Асфальтены отличаются от остальных компонентов тем, что их фрагменты имеют три и более ароматических или гетероциклических кольца, а “молекула” состоит из 4-5 фрагментов. Рентгеноструктурный анализ показал, что молекулы образуют пачки из 4-5 параллельных слоев, Такая псевдосферическая частица представляет собой зародыш твердой фазы коллоидных размеров. За счет адсорбции и сольватации на нем смол и ароматических углеводородов образуются устойчивые дисперсные системы. Косвенно о содержании САВ в сырье каталитического крекинга можно судить по его коксуемости.
В нефтях различного происхождения обнаружено около 50 микроэлементов (железо, никель, ванадий, хром, марганец, натрий и т.п.). Общее их количество незначительно и основная часть сосредоточена в тяжелых нефтяных остатках.
Достаточно хорошо на примере порфириновых соединений ванадия и никеля изучены, так называемые, внутримолекулярные комплексы, которые имеют следующее строение:


Они концентрируются обычно в асфальтенах, а никельпорфирины – еще и в смолах. В порфириновых соединениях связано до 20% ванадия и никеля. В сернистых нефтях обычно превалирует ванадий, а в малосернистых (с большим содержанием азота) – никель. Среди всех микроэлементов ванадий и никель находятся в значительно больших концентрациях, чем остальные. Микроэлементы являются нежелательными компонентами сырья каталитического крекинга, так они отравляют катализатор. Во время эксплуатации катализатора ванадий и никель накапливаются на его поверхности в оксидном виде и ускоряют протекание нежелательных при крекинге реакций. При их значительных концентрациях на катализаторе образуются повышенные количества водорода и кокса.
Для устранения дезактивирующего действия металлов сырье каталитического крекинга подвергают предварительной подготовке с целью уменьшения в нем содержания каталитических ядов. Наиболее перспективными и распространенными способами подготовки сырья являются перегонка нефти на модернизированных вакуумных блоках АВТ и гидроконверсия вакуумного газойля. Предварительное гидрооблагораживание сырья каталитического крекинга улучшает его свойства и влияет на групповой состав.
1.2 Механизм протекания реакций в процессе
каталитического крекинга
Реакции углеводородов на катализаторах крекинга протекают по карбокатионному механизму. Карбкатионы (карбоний-ионы) – это органические ионы с положительным зарядом на одном из атомов углерода. Они могут образоваться в результате отрыва от насыщенного углеводорода гидрид-иона (протона с двумя электронами) или присоединения к ненасыщенному углеводороду протона. Карбкатионы являются промежуточными продуктами в каталитическом крекинге и образуются только благодаря наличию у катализатора кислотных центров. Кислота – это вещество способное отдавать протон или принимать неподеленную пару электронов. В катализаторе крекинга отдают протоны кислотные центры Бренстеда, а принимают неподеленную пару электронов кислотные центры Льюиса (более подробно о кислотных центрах катализатора будет сказано в главе 2).
Реакция крекинга фактически не может иметь места, пока углеводород не приблизится к поверхности катализатора настолько, что окажется в зоне действия кислотного центра катализатора:
НА«Н+ + А–,
где НА – условное изображение алюмосиликатного катализатора в виде кислоты,
Н+ – протон (атом водорода без электрона, имеющий положительный заряд),
А– – отрицательно заряженная кристаллическая решетка цеолита, входящего в состав катализатора.
Участие в реакции протона водорода с катализатора (Бренстедовский кислотный центр) доказано с помощью меченых атомов. Карбкатионы являются активными промежуточными продуктами многих реакций, протекающих при каталитическом крекинге. Они содержат трехвалентный положительно заряженный атом углерода и легче всего образуются при взаимодействии протона катализатора с алкенами:

Небольшие количества алкенов могут образоваться при термическом распаде алканов при повышенных температурах в сырье, направляемом в реактор каталитического крекинга.
Образование карбоний-иона возможно также протонированием алкана бренстедовским кислотным центром:

Альтернативно в протонированном алкане может произойти расщепление связи С—С:

Ароматические углеводороды также могут быть акцепторами протонов, в результате чего образуется карбоний-ион:

В условиях каталитического крекинга карбоний-ионы могут существовать только в виде ионных пар: карбоний-ион – отрицательный активный центр поверхности катализатора.
Карбоний-ион, образующийся при взаимодействии углеводорода с кислотными центрами катализатора, претерпевает быстрые дальнейшие превращения:
- скелетная изомеризация карбоний-ионов (перегруппировка атомов водорода или метильных групп):

- отрыв гидрид-иона от молекулы насыщенного углеводорода с образованием нового карбоний-иона:
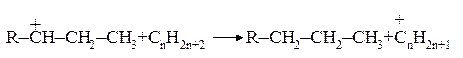
- распад карбоний-иона по связи в b-положении относительно заряженного атома углерода с образованием a-олефина и более мелких первичных карбкатионов с последующей их быстрой перегруппировкой в более устойчивые вторичные карбоний-ионы:

Последовательное превращение карбоний-иона продолжается до достижения наиболее устойчивой структуры:

Высокой стабильностью обладают карбоний-ионы с зарядом у третичного атома углерода (а) и с ароматическим фрагментом (б):


(а) (б)
Устойчивость карбоний-ионов определяет степень их участия в дальнейших реакциях. Например, высокая стабильность третичных карбониевых ионов обусловливает высокий выход изопарафиновых углеводородов в условиях промышленного каталитического крекинга:

Реакция переноса гидрид-иона (Н-переноса) наряду с расщеплением и изомеризацией углеродного скелета в значительной степени определяет качество продуктов крекинга.
В результате изомеризации карбоний-иона образуются более разветвленные и, соответственно, более стабильные частицы, например:

и
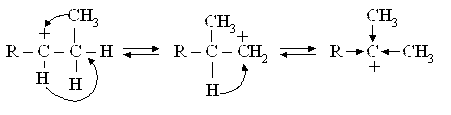
В результате подобных превращений продукты каталитического крекинга обогащены изомерными углеводородами, за счет чего повышается октановое число бензина. Этот эффект усиливается вследствие перераспределения водорода между непредельными углеводородами и циклоалканами, присутствующими в реакционной массе:

алкен циклоалкан алкан арен
Арены, как и разветвленные алканы, повышают детонационную стойкость моторных топлив и это вносит дополнительный вклад в повышение октанового числа бензина.
Вследствие малой устойчивости карбоний-ионов  и
и  в газах каталитического крекинга преобладают углеводороды С3-С4.
в газах каталитического крекинга преобладают углеводороды С3-С4.
Ниже приведены ряды классов углеводородов по убыванию их склонности к химическим превращениям при каталитическом крекинге:
алкены > арены с большим числом боковых цепей > циклоалканы > алканы.
Реакционная способность различных углеводородов в условиях промышленного процесса объясняется избирательностью адсорбции на поверхности катализатора – в первую очередь адсорбируются ненасыщенные углеводороды (алкены, арены). Наименьшей адсорбируемостью обладают алканы.
Дата добавления: 2015-08-02; просмотров: 888 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Введение | | | Образование кокса |