
Читайте также:
|
Вычислите растворимость при 25 0С в моль/л:
| 01 – иодида серебра; | 02 – сульфида серебра; |
| 03 – карбоната бария; | 04 – сульфида меди (II); |
| 05 – сульфида железа (II); | 06 – дихромата серебра |
| 07 – иодида висмута (III); | 08 – фосфата бария; |
| 09 – дихромата бария; | 10 – фторида магния; |
| 11 – хромата серебра; | 12 – фосфата магния; |
| 13 – фосфата серебра; | 14 – фторида бария; |
| 15 – арсената серебра. |
Вычислите произведение растворимости соли при некоторой температуре, если известно, что:
16 – в 1 л насыщенного раствора Ag2CrO4 содержится при некоторой температуре 0,025 г соли;
17 – в 1 л насыщенного раствора Pb3(РО4)2 содержится в 1,2*10-6 г соли;
18 – в 50 мл насыщенного раствора Ag2CO3 содержится 6,3*10 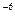 моля СО
моля СО 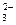 ;
;
19 – в 100 мл насыщенного раствора PbI2 содержится 0,0268 г свинца в виде ионов;
20 – растворимость Fe(ОН)3 равна 1,9*10-10 моль/л;
21 – в 2 л Н2О при 25 0С может растворяться 2,2*10-4 г AgBr;
22 – растворимость СаСО3 при 18 0С равна 1,3*10-4 моль/л;
23 – растворимость PbBr2 при 18 0С равна 2,7*10-2 моль/л;
24 – растворимость AgCl в воде при 25 0С составляет 0,0018 г/л;
25 – растворимость PbI2 при 18 0С равна 1,5*10-3 моль/л.
Выпадет ли осадок при сливании:
26 – равных объемов 10-4 М нитрата серебра и 10-4 М бромида калия;
27 – 0,5 л 10-6 М нитрата серебра и 1 л 10-5 М бромида калия;
28 – равных объемов 10-2 М хлорида бария и 10-8 М фторида калия;
29 – равных объемов 10-3 М хлорида кальция и 10-3 М серной кислоты;
30 – равных объемов 10-5 М иодида натрия и 10-5 М нитрата серебра.
Дата добавления: 2015-07-25; просмотров: 88 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Вычисление степени диссоциации (a) и концентрации ионов водорода в растворах слабых электролитов | | | Обменные реакции в растворах электролитов |