
|
Читайте также: |
Вернемся к самому началу нашего метода МО, к уравнению
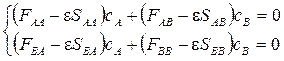
Теперь, когда атомы А и В разные, нам уже не удастся так легко с ним разделаться. Нет, посчитать с хорошей программой и компьютером, конечно, можно, но нам сейчас важнее опять-таки качественный результат. Его легче получить, если положить SAB = SBA = 0. Тогда
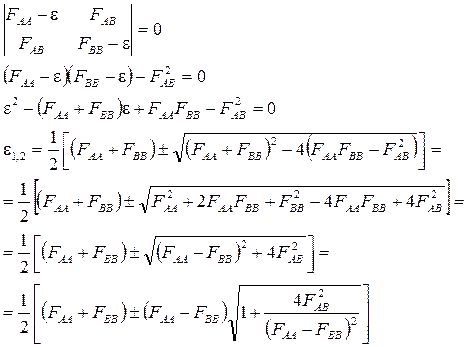
Да, легче не становится… Допустим, однако, что энергии наших орбиталей cА и cВ различаются достаточно сильно, и

Тогда наш квадратный корень можно разложить в ряд Тейлора
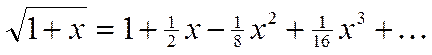 ,
,
и ограничиться только первым членом (на самом деле эта приближенная формула работает очень неплохо):

Пусть FAA > FBB (иначе просто поменяется знак, и все будет в порядке). Тогда низший уровень опустится относительно FBB, а верхний поднимется на такую же величину относительно FAA. То, что они сместились на одну и ту же величину связано, конечно, с тем, что мы положили SAB = SBA = 0. Для нас же важно то, что это изменение энергии тем больше, чем меньше разность энергий взаимодействующих орбиталей.
Рассмотрим молекулу LiH. Потенциалы ионизации равны 13,6 эВ и 5.4 эВ. Как распределится в нашей МО j = с 1c1 + с 2c2 электронная плотность? Надо взять энергию e2 и подставить ее в одно из уравнений, например:

Будем считать, что атом А – это атом лития, а В – атом водорода (мы просто рассматривали, что FAA > FBB). Тогда вклад сА 2s-АО лития в связывающую МО
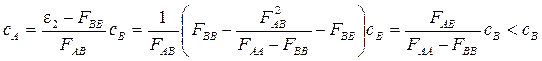
В низшую из двух МО больший вклад вносит АО с более низкой энергией, а в высшую – АО с более высокой.
Рассмотрим HF
И LiF.
Дата добавления: 2015-07-20; просмотров: 61 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Другие гомоядерные молекулы. | | | Внимательно прочтите следующие строки |