
|
Читайте также: |
3.1.1 Теоретический и действительный расход воздуха
 |
Расчетная формула для определения теоретического количества воздуха (м3), необходимого для сжигания 1 м3 сухого газообразного топлива:
V0 = 0.0476 [0.5CO + 0.5H2 + 1.5H2S + Σ(m+n/4)CmHn – O2] (8)
где CO, H2 и т.д. – компоненты топлива, %
V0 = 0,0476 [2 · 91,2 + 3,5 · 2,8 + 5 · 0,9 + 6,5 · 0,6] = 9,548 м3
Действительный расход воздуха на 1 м3 газообразного топлива определяется из выражения:
Vв = α · Vт (9)
где α – коэффициент избытка воздуха в печи.
При α1 = 1,2:
Vв = 1,2 · 9,548 = 11,458 м3
3.1.2 Состав и объем продуктов сгорания
Vг = Vсг + Vвп (10)
где Vсг – сухие газы,
Vвп – водяные пары.
Объем сухих газов при α = 1:
Vсг = VCO2 + VN2 + VO2 (11)
VCO2 = 0.01·(CO2 + CO + H2S + Σ m·CmHn)
VCO2 = 0.01 · (0.5 + 91,2+ 2 · 2,8 + 3 · 0,9 + 4 · 0,6) = 1,024 м3
Объем сухих газов при α = 1.6:
 (12)
(12)


Vт – теоретическое количество воздуха (м3), необходимого для сжигания 1 м3 сухого газообразного топлива.
 ,
,
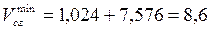 м3 (при α=1);
м3 (при α=1);
Vсг = 8,6 + (1,6 – 1) · 9,548 = 14,33 м3 (при α = 1,6).
Vсг = 8,6 + (1,2 – 1) · 9,548 = 10,51 м3 (при α = 1,2).
Vвп = 1,974 (из таблицы 1);
 - (при α = 1,2);
- (при α = 1,2);
 - (при α = 1,6);
- (при α = 1,6);
Всего: Vг = 14,33 + 1,974 = 16,304 м3.
Теплота сгорания:
QHP=358 ·CH4 + 640 ·C2H6 + 915 ·C3H8 + 1190 ·C4H10 + 1465 ·C5H12 (13)
QHP=358 ·91.2 +640 ·2.8 +915 ·0.9 +1190 ·0.6 = 35979,1кДж/м3.
Расчет горения природного газа приведен в таблице 1.
 Таблица 1 – Расчет горения природного газа
Таблица 1 – Расчет горения природного газа
| Состав 1м3 газа, м3 | Реакция горения | Требуется для горения, м3 | Образуется при горении, м3 | |||||||
| O2 | N2 | воздуха | CO2 | H2O | N2 | O2 | сухих газов | всех газов | ||
| CH4=0,912 | CH4+2O2= CO2+2H2O | 2·0,91= =1,82 | 2,002·3,7 = 7,4 | 2,002 +7,4 = 9,4 | 0,912 | 2·0, 912 =1,824 | 0,033+ 7,4=7,43 | |||
| C2H6=0,028 | C2H6+3,5O2= =2CO2+3H2O | 3,5· 0,028= =0,098 | 2·0,028= =0,056 | 3·0,028=0,084 | ||||||
| C3H8=0,009 | C3H8+5O2= =3CO2+4H2O | 5·0,009=0,045 | 3·0,009= =0,018 | 4·0,009=0,036 | ||||||
| C4H10=0,006 | C4H10+6,5O2 =4CO2+5H2O | 6,5·0,006=0,039 | 4·0,006= =0,024 | 5·0,006=0,03 | ||||||
| N2=0,033 | Переходит в газы | -- | -- | -- | ||||||
| При α=1 | 2,002 | 7,4 | 9,4 | 1,01 | 1,974 | 7,43 | -- | 8,6 | 10,5 | |
| При α=1,2 | 2,402 | 8,88 | 11,28 | 1,01 | 1,974 | 8,91 | 0,58 | 10,51 | 12,48 | |
| При α=1,6 | 3,203 | 11,84 | 15,04 | 1,01 | 1,974 | 11,88 | 0,75 | 14,33 | 16,3 |
Из расчета горения следует, что на 1 м 3 природного газа при α =1,2 требуется 11,28 м 3 воздуха, из 1 м3 газа образуется 1,974 м 3 водяных паров и 10,51м 3 сухих газов. Проверяем возможность достижения требуемой температуры обжига 1100°С, если воздух поступает подогретым до 200°С. Приход тепла при горении 1 м 3 газа составит
 |
Qнp + cвtвVв + cmtm, кДж (14)
где Qнp – теплота сгорания;
При холодном газе теплосодержанием самого топлива cmtm ввиду его незначительной величины можно в расчете пренебречь, учитывая теплоту сгорания топлива и теплосодержание воздуха
Qнp + cвtвVв = 35500 + 1,297 · 200 · 11,28 = 38426 кДж,
где св - теплоемкость воздуха, при tв = 200 °С, св = 1,297 кДж/м3·°С;
VB -объем воздуха для горения 1 м3 топлива, из расчета горения VВ = 11,28 м3.
Следовательно теплосодержание продуктов горения должно составить 38426 кДж.
Предполагаем, что теоретическая температура продуктов горения равна 1800°С, тогда теплосодержание сухих продуктов горения и водяных паров составит
iпр.гор = (cс.газVс.газ + cв.пVв.п)tm., (15)
где Vс.газ - объем сухих газов от сгорания 1 м 3 топлива, Vс.газ = 10,51 м 3;
Vв.п. - объем водяных паров из 1 м3 газа образуется 1,974 м 3;
tm - теоретическая температура горения, °С;
сс.газ. - теплоемкость сухих газов при t = 1800 °С составит сс.газ. =1,62 кДж/(м 3·°С), для водяных паров св.п. = 1,92 кДж/м3-°С
iпр.гор = (1,62 · 10,51 + 1,92 · 1,974) · 1800 = 37476 кДж
Полученное теплосодержание меньше тепла, выделенного в топке на
 38426 - 37476 = 950 кДж.
38426 - 37476 = 950 кДж.
Предполагаем температуру 1900° С.
сс.газ. = 1,63 кДж/м 3·°С;
св.п. = 1,94 кДж/м3·°С;
iпр.гор = (1,63 · 10,51 + 1,94 · 1,974)1900 = 39824 кДж
39824- 38426 = 1398 кДж,
т.е. на 1398 кДж больше выделенного тепла, следовательно температура горения лежит между 1800 °С и 1900 °С.
1800 +(100/2348)·950 = 1841°С
Принимая пирометрический коэффициент для туннельной печи равным 0,75, находим действительную температуру горения:
tд = tm· χ (16)
tд = 1841 · 0,75 = 1380 °С,
что при подогреве воздуха до 200 °С обеспечит требуемую температуру обжига кирпича.
Дата добавления: 2015-07-25; просмотров: 170 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Описание установки | | | Тепловой баланс туннельной печи за 1 ч работы |