
Читайте также:
|
| Аминокислоты и образующиеся из них биогенные амины | Формула биогенного амина | Функции биогенных аминов в организме |
| Серин ¯ Коламин ¯ Холин ¯ Ацетилхолин | HOCH2CH2NH2 HOCH2CH2N(CH3)3ОН CH3COOCH2CH2N(CH3)3ОН | Входит в состав кефалина Входит в состав лецитина Медиатор, нейромедиатор |
| Цистеин ¯ Цистеамин | HSCH2CH2NH2 | Структурный элемент КоА и пантетеина |
| Аспарагиновая кислота ¯ β-Аланин | H2NCH2CH2COOH | Структурный элемент КоА |
| Триптофан ¯ 5-Окситриптофан ¯ Серотонин |

| Медиатор, нейромедиатор |
| Гистидин ¯ Гистамин | 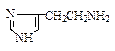
| Медиатор |
| Тирозин ¯ 3,4-Диоксифенил аланин (ДОФА) ¯ Дофамин ¯ Норадреналин ¯ Адреналин |



| Нейромедиатор Медиатор, нейромедиатор гормон Медиатор, нейромедиатор гормон |
| Треонин ¯ Аминопропанол | CH3CHOHCH2NH2 | Составная часть витамина В12 |
| Глутаминовая кислота ¯ (ГАМК) | H2NCH2CH2CH2COOH | Нейромедиатор |
| Аргинин ¯ Агматин ¯ Путресцин ¯ Спермидин ¯ Спермин | 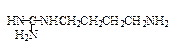

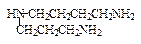

| Компонент рибосом Компонент рибосом, трупный яд Компонент рибосом Компонент рибосом |
| Лизин ¯ Кадаверин | H2NCH2CH2CH2CH2CH2NH2 | Компонент рибосом, трупный яд |
Нейромедиаторы и медиаторы. Термином медиатор обозначают вещества, передающие нервное возбуждение через синаптическую щель от одной клетки периферической нервной системы к соседней. Нейромедиаторы – это вещества, воздействующие на постсинаптическую мембрану синапса центральной нервной системы и вызывающие ее деполяризацию (передача нервного импульса) или, напротив, гиперполяризацию (торможение передачи нервного импульса). К нейромедиаторам относятся некоторые аминокислоты, а также пептиды, белки и биогенные амины (см. табл. 1.2).
В связи с этим в клетках головного мозга идет активный метаболизм аминокислот. В головном мозге концентрация аминокислот, в особенности выполняющих функции нейромедиаторов, в 7-8 раз выше, чем в плазме крови. Наиболее высоким является уровень глутаминовой и аспарагиновой аминокислот (5-10 ммоль и 2-3 ммоль соответственно).
К аминокислотам, выполняющим функции нейромедиаторов, относятся глицин, аспарагиновая кислота, глутаминовая кислота, ГАМК и ДОФА.
Метаболиты. Углеродные скелеты 20 протеиногенных аминокислот превращаются в процессе метаболизма в семь различных продуктов деградации.
1. Пировиноградная кислота – глицин, аланин, серин, цистеин, треонин,
(пируват) триптофан, метионин.
2. Щавелево-уксусная кислота – аспарагин, аспарагиновая кислота.
(оксалоацетат)
3. Фумаровая кислота – фенилаланина, тирозин.
(фумарат)
4. Сукцинил-КоА – изолейцин, Валин.
5. 2-Оксоглутаровая кислота – глутаминовая кислота, глутамин,
(2-оксоглутарат) гистидин, аргинин, пролин.
6. Ацетил-КоА – лейцин, лизин; изолейцин.
7. Ацетоуксусная кислота – лейцин, лизин, фенилаланин, тирозин,
(ацетоацетат) триптофан.
Пять метаболитов (пируват, оксалоацетат, фумарат, сукцинил-КоА, 2-оксоглутарат) являются предшественниками в процессе синтеза глюкозы (глюконеогенез). Аминокислоты, деградация которых дает один из пяти указанных выше метаболитов, называются глюкогенными аминокислотами. За исключением лейцина и лизина все остальные 18 протеиногенных аминокислот являются глюкогенными.
Ацетил-КоА и ацетоацетат не могут включаться в глюконеогенез. Они используются организмами для синтеза жирных кислот, изопреноидов и кетоновых тел (ацетон, ацетоуксусная кислота, 3-гидроксимасляная кислота). Аминокислоты, которые образуют ацетил-КоА или ацетоацетат, называют кетогенными аминокислотами. Фактически только кетогенными являются лейцин и лизин, а такие аминокислоты, как изолейцин, фенилаланин, тирозин и триптофан, могут быть и глюкогенами и кетогенами.
1.1.3. Физико-химические свойства аминокислот
В кристаллическом состоянии аминокислоты находятся в виде биполярных ионов (цвиттерионов). Вследствие этого они имеют высокие температуры плавления и большинство из них растворимы в воде лучше, чем в спирте (табл.1.3).
В водном растворе аминокислоты также присутствуют, главным образом, в виде цвиттерионов, которые находятся в равновесии с неионизированной формой, например, для глицина соотношение равновесных концентраций неионизированной и цвиттерионной форм равно 1:260000:
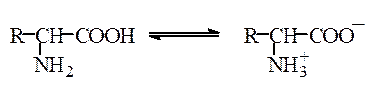
Неионизированная форма Цвиттерионная форма
Дикарбоновые аминокислоты и диаминокарбоновые кислоты существуют в водных растворах в виде смесей неионизированных и различно заряженных форм. Например, аспарагиновая кислота существует в виде следующих форм с соотношением концентраций:
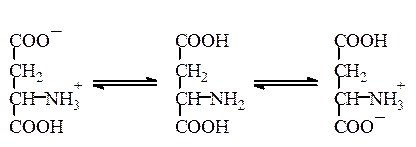
1 600 1 28 000
В случае лизина устанавливается следующее равновесие:
 16
16
320 000 1 1 800 000
Аминокислоты гораздо лучше растворимы в водных растворах кислот и щелочей, чем в воде, что обусловлено их амфотерностью.
В кислой среде аминокислота ведет себя как основание с константой диссоциации сопряженной кислоты Ka (α-NH2) и заряжается положительно, а в щелочной – как кислота с константой диссоциации Ka (α-COOH) и заряжается отрицательно:
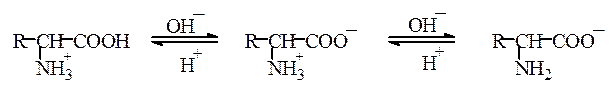
Поскольку в аминокислотах содержатся как минимум две ионогенные группы, суммарный заряд молекул зависит от pH среды. Проиллюстрируем зависимость заряда аминокислоты от рН на примере гистидина, содержащего три ионогенные группы. На рис. 1.4 приведена кривая титрования гистидина сильной кислотой и щелочью, на которой отмечаются три точки перегиба, соответствующие трем ионизирующимся группировкам (COOH, NH2, имидазольное кольцо).
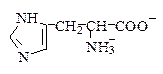
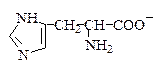

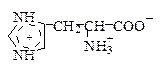
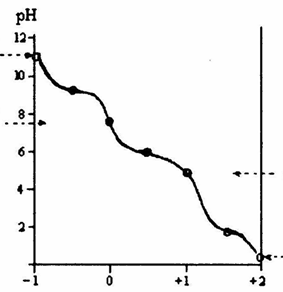
Р и с.1.4. Кривая титрования гистидина сильной кислотой и щелочью
Таблица 1.3
Дата добавления: 2015-07-25; просмотров: 146 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Протеиногенные аминокислоты | | | Физические свойства L-аминокислот 1 страница |