
Читайте также:
|
По окончании лечения у большинства больных (78,1 %) отмечено улучшение общего состояния. Значимых различий по динамике субъективных показателей между группами не получено.
Наименее токсичным явилось лечение с использованием только лучевого метода. Присоединение 5-фторурацила при проведении ЛТ в режиме обычного фракционирования увеличило количество эзофагитов с 19,2 % до 51,8 % (р < 0,05).
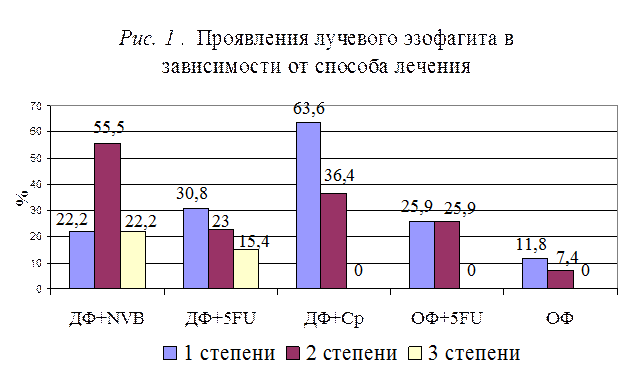
Примечание: ДФ+NVB – динамическое фракционирование на фоне навельбина; ДФ+5FU – динамическое фракционирование на фоне 5-фторурацила; ДФ+Cp – динамическое фракционирование на фоне карбоплатина; ОФ+5FU – обычное фракционирование на фоне 5-фторурацила; ОФ – обычное фракционирование.
Так как изменение режима фракционирования при облучении на фоне 5-фторурацила (обычное в сравнении с динамическим) не оказало значимого влияния на частоту и тяжесть эзофагитов (51,8 % против 69,2 %, p = 0,2), а использование различных химиопрепаратов при одном и том же режиме облучения (динамическом) привело к их увеличению в разной степени, можно сделать заключение, что эти изменения обусловлены не столько режимом фракционирования, сколько использованием химиопрепаратов с более выраженным радиомодифицирующим эффектом.
Отмечено статистически значимое увеличение количества лучевых дерматитов первой степени в группах динамического фракционирования, которые не влияли на общее состояние пациентов и не препятствовали проведению лечения в полном объёме (рис.2).
Рис.2. Проявления лучевого дерматита в зависимости от способа лечения

Значимых различий по частоте возникновения пульмонитов в группах не выявлено (рис. 3).

Острые лучевые реакции возникали во всех группах при подведении физической СОД = 24 – 34 Гр, что указывает на большую роль в их возникновении величины СОД, чем режима фракционирования РОД и общего времени облучения.
Нами не отмечено влияния режима фракционирования разовой дозы на частоту возникновения и тяжесть лучевых повреждений лёгочной ткани (в группе ДФ + 5FU – 53,8 %, в группе ОФ + 5FU – 55,5 %). Статистически значимых различий в частоте возникновения постлучевых пневмофиброзов в группах синхронного химиолучевого лечения не было (рис. 4). Нами так же не выявлено связи их развития с количеством и выраженностью острых лучевых реакций. Факторами, усугубляющими степень тяжести постлучевого пневмофиброза, явились наличие сопутствующих хронических воспалительных заболеваний лёгких или ателектаза.

В тоже время нами отмечен факт увеличения частоты и тяжести острых лучевых реакций при проведении облучения на ЛУЭ с меньшей энергией. Так, количество эзофагитов возросло с 23,8 % при проведении ЛТ на ЛУЭ – 15 МэВ до 83,3 % – при облучении на ЛУЭ SL-75-5, 6 МэВ (р = 0,005). Дерматиты отмечены в 16,6 % случаев при лечении на ЛУЭ – 15 МэВ и в 50 % – на ЛУЭ SL-75-5, 6 МэВ (р = 0,02). Энергия излучения используемых источников не влияла на частоту возникновения острых и поздних лучевых реакций лёгочной ткани. Пульмониты возникли в 33,3 % при облучении на ЛУЭ – 15 МэВ и в 50 % – при лечении на ЛУЭ SL-75-5, 6 МэВ, пневмофиброзы – соответственно в 40,4 % и 66,6 % (p > 0,05).
Таким образом, при лучевой терапии больных РЛ преимущество имеет тормозное излучение больших энергий, позволяющее снизить лучевые нагрузки на кожу и пищевод.
Гематологическая токсичность во всех группах встречалась редко и не требовала специального лечения.
Анализ непосредственных результатов показал, что проведение конвенциального облучения на фоне 5-фторурацила не увеличило количество объективных эффектов (полный регресс + частичный регресс) по сравнению с только лучевой терапией. Хотя, по литературным данным, 5-фторурацил давно применяется в качестве модификатора при лучевом лечении больных НМРЛ [Дарьялова С.Л., 1999; Черниченко А.В., 2008], его сенсибилизирующий эффект, по нашим данным, проявился незначительно.
Наилучшие результаты нами получены при проведении облучения в режиме динамического фракционирования на фоне навельбина. Объективный эффект в группе составил 61,1 %, в том числе полный регресс (ПР) – 33,3 %, что достоверно выше по сравнению со II (7,7 % и 0), с IV (18,5 % и 7,4 %) и V (18,5 % и 7,4 %) группами соответственно (р < 0,05) (рис. 5). Таким образом, только изменение режима фракционирования не повлияло на непосредственные результаты лечения. В данном случае, очевидно, проявилось действие навельбина.
Рис. 5 Непосредственные результаты ЛТ в зависимости от способа лечения

Изучение отдалённых результатов лечения больных НМРЛ различными способами показало, что средняя продолжительность жизни (СПЖ) пациентов, которым ЛТ проведена в режиме динамического фракционирования на фоне навельбина, составила 16,5 ± 2,5 мес., что достоверно выше СПЖ больных в группах конвенциального облучения (9,6 ± 1,1 мес. в IV группе и 10,4 ± 1,1 мес. в V группе, р < 0,05).
Анализ СПЖ с учётом стадии заболевания так же выявил преимущество методики динамического фракционирования на фоне навельбина как при неоперабельных опухолях ранних стадий (II B ст.), так и при наиболее местнораспространённых опухолях (III B ст.)
СПЖ больных II B ст. заболевания, которым облучение проводили в режиме динамического фракционирования на фоне навельбина, составила 35,0 ± 4,1 мес., тогда как в группах обычного фракционирования при только лучевой терапии – 13,2 ± 6,1 мес., а при лечении на фоне 5-фторурацила – 7,5 ± 1,1 мес. (р <0,05). СПЖ пациентов III B стадии в группе динамического фракционирования на фоне навельбина составила 15,5 ± 4,5 мес., что достоверно выше по сравнению с другими группами (II гр. – 9,5 ± 1,5 мес., III гр. – 7,0 ± 1,3 мес., IV гр. – 9,0 ± 1,4 мес., V гр. – 9,7 ± 1,6 мес., p < 0,05).
По показателю медианы выживаемости, не зависящему от времени наблюдения, динамическое фракционирование на фоне навельбина оказалось так же более предпочтительным способом лечения: 12,5 мес. по сравнению с 11,0 мес. во II и IV группах, 9,0 мес. – в III группе и 7,5 мес. – в V группе.
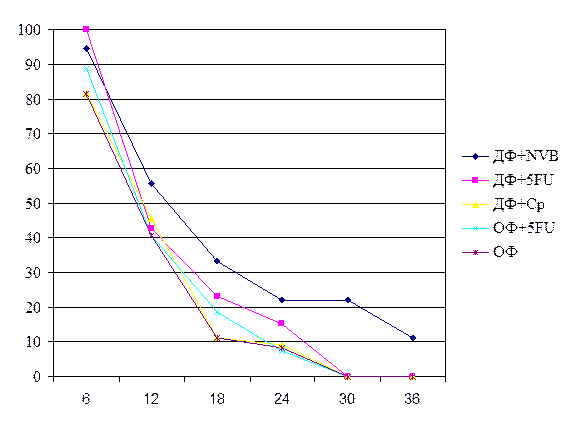
Показатели выживаемости больных НМРЛ приведены на рис. 6. На протяжении всего периода наблюдения наиболее высокой оказалась выживаемость больных группы динамического фракционирования на фоне навельбина. Более года после проведения ЛТ в режиме ДФ на фоне навельбина прожили 55,5 % больных, 42,7 % – в группе ДФ на фоне 5-фторурацила, 45,5 % – в группе ДФ на фоне карбоплатина и одинаковое количество (40,7 %) в группах обычного фракционирования.
Наметившаяся тенденция увеличения продолжительности жизни в группах динамического фракционирования в наибольшей степени проявилась при оценке двух- и трёхлетней выживаемости: 2 года в группе динамического фракционирования на фоне навельбина прожили 22,2 % больных, в группе динамического фракционирования на фоне 5-фторурацила – 15,3 %, в группе динамического фракционирования на фоне карбоплатина – 9,1 %, в группе обычного фракционирования на фоне 5-фторурацила – 7,4 % и в группе обычного фракционирования без радиомодификации – 8,3 %. Три года прожили 11,1% больных только группы динамического фракционирования на фоне навельбина.
Наименьшая выживаемость отмечена в группах больных, которым лучевая терапия проведена в режиме обычного фракционирования. При этом присоединение 5-фторурацила не повлияло на отдалённые результаты. Изменение же режима фракционирования при облучении на фоне 5-фторурацила увеличило двухлетнюю выживаемость с 7,4 % в группе обычного фракционирования до 15,3 % в группе динамического фракционирования (p > 0,05).
По нашим данным, фактором, оказавшим существенное влияние на выживаемость, явился непосредственный эффект (F = 8,2 %; р = 0,005). Таким образом, более высокие показатели выживаемости больных группы динамического фракционирования на фоне навельбина обусловлены значительно большей непосредственной эффективностью.
Рис. 6. Выживаемость больных неоперабельным НМРЛ в зависимости от способа лечения

|
|
 .
.
Длительность лучевого лечения больных НМРЛ в режиме динамического фракционирования составила 36,5 ± 0,7 дней, что на 2 недели меньше, чем при конвенциальном облучении (51,8 ± 0,9 дней, р < 0,001). Сокращение общих сроков лучевого лечения при использовании динамического фракционирования, на наш взгляд, является важным, экономически обоснованным, преимуществом методики.
В нашем исследовании показана эффективность ОФЭКТ с 99mТс-депреотидом в дифференциальной диагностике очаговых поражений лёгких.
Среднее значение захвата 99mТс-депреотида при злокачественных новообразованиях было выше 2,2; при воспалении – до 1,4.
После сопоставления с морфологическим диагнозом результаты ОФЭКТ с 99mТс-депреотидом распределились следующим образом: истинноположительные – 20 (рак лёгкого); истинноотрицательные – 3 (воспаление); ложноположительные – 2 (1 случай – неспецифическое воспаление и 1 – туберкулома). Ложноотрицательных заключений не было.
В результате расчётов по стандартным формулам была установлена следующая эффективность методики: чувствительность – 100%, специфичность – 60%, точность – 92%.
Кроме того, у 11 пациентов, наряду с визуализацией первичного очага, было выявлено накопление РФП в лимфатических узлах средостения и у одного больного – в костях скелета, обусловленное метастатическим поражением, что имело значение для уточнения диагноза, планирования лечения и прогноза.
Каких-либо нежелательных явлений, вызванных введением препарата, не зарегистрировано.
Мы также провели изучение лимфоцитопоэза больных НМРЛ как одного из факторов, влияющих на эффективность лечения заболевания и его исход. Показатели субпопуляционного состава мононуклеарной фракции периферической крови до начала терапии были получены и сопоставлены в двух группах больных, отдалённые результаты лечения которых резко отличались. В группе больных благоприятного прогноза (БП) на протяжении 2 – 15 месяцев до летального исхода (в среднем 5,9 ± 0,9 мес. и 6,7 ± 0,95 мес., разница недостоверна), уровень гемопоэтических стволовых клеток был в пределах нормы (0,136 ± 0,022 %), а в группе пациентов неблагоприятного прогноза (НП) – выше (0,222 ± 0,0316 %) (р = 0,05). Аналогичные соотношения были выявлены в более короткие сроки (3,9 ± 0,34 мес. и 3 ± 0,43 мес.) до смерти и в уровне субпопуляции ранних Т-лимфоцитов CD4+Leu8+: у больных группы БП этот показатель составлял 9,1 ± 2,56 %, а в группе НП был значительно выше (23 ± 4,52 %), (р = 0,02). В последний месяц жизни у больных в группе НП зарегистрировано резкое и необратимое снижение как гемопоэтических стволовых, так и ранних клеток Т-лимфоцитарного ряда до 0,13 ±0,019 % (p = 0,05) и 3 ± 1,69 % (p = 0,003) соответственно. Достоверного снижения других показателей выявить не удалось. Таким образом, различия в результатах лечения в группах больных БП и НП по темпу гибели явились следствием неравенства исходного общего статуса пациентов до начала лечения по критериям состояния системы кроветворения и некоторых фракций лимфоцитов промежуточной зрелости. Суть этого неравенства заключается в экстремальной, но не стабильной продукции гемопоэтических стволовых клеток и фракций ранних Т-лимфоцитов до начала лечения в группе НП.
Выводы
1. Разработанный способ лечения больных неоперабельным немелкоклеточным раком лёгкого, сочетающий облучение в режиме динамического фракционирования с введением навельбина, удовлетворительно переносится и является эффективным по критериям локального ответа и средней продолжительности жизни: объективный эффект составил 61,1 %, средняя продолжительность жизни – 16,5 ± 2,5 мес. (соответственно в группах: динамического фракционирования на фоне 5-фторурацила – 7,7 % и 12,9 ± 2,2 мес.; обычного фракционирования на фоне 5-фторурацила – 18,5 % и 9,6 ± 1,1 мес.; обычного фракционирования – 18,6 % и 10,4 ± 1,1 мес., p < 0,05).
2. Режим динамического фракционирования не увеличивает частоту и выраженность острых лучевых реакций пищевода и лёгких по сравнению с конвенциальным облучением: эзофагиты при проведении лучевой терапии в режиме динамического фракционирования на фоне 5-фторурацила возникли в 69,2 % случаев, пульмониты – в 38,5 %; при облучении в конвенциальном режиме на фоне 5-фторурацила в 51,8 % и 37 % соответственно, (p > 0,05).
3. Использование навельбина при проведении синхронной химиолучевой терапии повышает частоту и тяжесть острых лучевых реакций пищевода по сравнению с облучением на фоне 5-фторурацила: 100 % против 69,2 % (p = 0,03), не оказывая существенного влияния на лучевые реакции кожи и лёгких (дерматиты возникли в 77,7 % в группе динамического фракционирования на фоне навельбина и 69,3 % в группе динамического фракционирования на фоне 5-фторурацила, пульмониты – в 50 % и 39,5 % соответственно, p > 0,5).
4. Лучевая терапия в режиме динамического фракционирования на фоне цитостатиков не увеличивает частоту постлучевых пневмофиброзов по сравнению с конвенциальным облучением: в группе динамического фракционирования на фоне навельбина пневмофиброзы возникли в 77,7 %; в группе динамического фракционирования на фоне 5-фторурацила – в 53,8 %; в группе динамического фракционирования на фоне карбоплатина – в 54,5 %; в группе обычного фракционирования на фоне 5-фторурацила – в 55,5 %, (p > 0,05).
5. Режим динамического фракционирования позволяет сократить сроки лучевой терапии с 51,8 ± 0,9 дней до 36,5 ± 0,7 дней по сравнению с конвенциальным облучением (p < 0,05), не ухудшая непосредственные и отдалённые результаты лечения.
6. Однофотонная эмиссионная компьютерная томография с 99mТс-депреотидом является эффективным, безопасным и малоинвазивным методом визуализации злокачественных поражений лёгких, регионарных и отдалённых метастазов.
7. Установлена связь продолжительности жизни и темпа смертности больных неоперабельным немелкоклеточным раком лёгкого с исходным (до начала лечения) уровнем в крови гемопоэтических стволовых клеток CD34+ и субпопуляций ранних Т-лимфоцитов CD4+Leu8+, что определяет их прогностическую значимость. Отклонение указанных показателей от средних значений повышает риск смерти пациентов.
Дата добавления: 2015-07-25; просмотров: 44 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Внедрение. | | | Список работ, опубликованных по теме диссертации |