
|
Читайте также: |
Большинство ферментов катализирует реакции, в которых участвует более чем один субстрат. В случае если кофермент не является простетической группой, его также можно рассматривать как ещё один субстрат. Следовательно, участников ферментативной реакции может быть несколько: непосредственно фермент, несколько субстратов и кофермент.
В этих случаях механизм ферментативной реакции, как правило, может идти по одному из двух путей: по механизму "пинг-понг" (механизму двойного замещения) или последовательному. Рассмотрим оба механизма.
1. Механизм "пинг-понг"
Схематично механизм "пинг-понг" может быть представлен следующим образом:
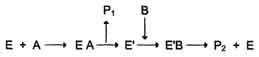
Субстрат А, взаимодействуя с ферментом (Е), превращается в продукт (Р1). Фермент остаётся в результате этого преобразования не в нативной форме, а в изменённой (Е') в результате модификации кофермента. Далее к активному центру Е' присоединяется субстрат В, подвергающийся преобразованию в продукт (Р2) с высвобождением нативной формы фермента (Е).
Хороший пример механизма "пинг-понг" - реакции трансаминирования с участием ферментов аминотрансфераз (кофермент пиридоксальфосфат). Аминотрансферазы, открытые отечественным учёным А.Е. Браунштейном, катализируют обратимые реакции переноса аминогруппы с аминокислоты на кетокислоту. Механизм "пинг-понг" данной реакции схематично представлен на рис. 2-7.
Другой пример механизма "пинг-понг" - реакции дегидрирования с участием кофермента FAD (флавинадениндинуклеотид) или FMN (флавинмононуклеотид), которые прочно связаны с ферментом и, следовательно, не могут рассматриваться в качестве второго субстрата.
Схематично структура этих коферментов и соответствующие им химические формулы представлены на рис. 2-8.
FMN и FAD участвуют в окислительно-восстановительных реакциях, акцептируя 2 е- и 2 Н4 в изоаллаксазиновомкольце.
Схему реакции дегидрирования (как пример механизма "пинг-понг" с участием кофермен-тов FMN и FAD) можно представить в следующем виде:
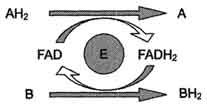
где АН2 - донор водорода, окисляемый субстрат 1; А - окисленная форма субстрата 1; В - акцептор водорода - субстрат 2; ВН2 - восстановленная форма субстрата 2; Е (FAD), Е (FADH2) - окисленная и восстановленная формы кофермента FAD, входящего в состав фермента Е.
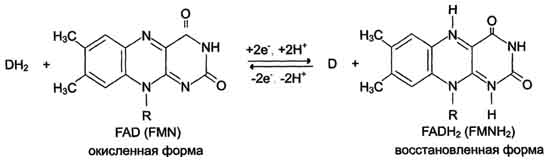
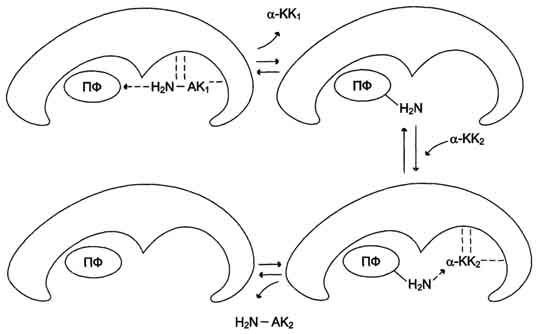
Рис. 2-7. События в активном центре аминотрансферазы как пример механизма "пинг-понг". Кофермент пиридоксальфосфат (ПФ), связанный с ферментом, принимает α-аминогруппу от первой аминокислоты (АК1), которая при этом превращается в α-кетокислоту 1 (КК1) и высвобождается из активного центра фермента. Далее в активный центр фермента присоединяется ос-кетокислота 2 (КК2), которая забирает аминогруппу от кофермента и превращается в α-аминокислоту (АК2).
В качестве примера FAD-зависимой реакции можно привести сукцинатдегидрогеназную реакцию. В этой реакции в качестве второго субстрата участвует убихинон - один из посредников ЦПЭ (см. схему на с. 90).
Дата добавления: 2015-08-17; просмотров: 94 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Б. Коферменты | | | Последовательный механизм |