
|
Читайте также: |
1. В какую сторону сместится равновесие реакций разложения сероводорода ΔН = 20 кДж/моль, димеризации оксида азота (IV) Н = –33 кДж/моль, горения оксида углерода (II) ΔН = –283 кДж/моль при повышении температуры; при повышении давления?
2. Рассмотрите систему взаимодействия водорода и серы с образованием сероводорода. Как сместится равновесие при изменении (увеличении, уменьшении) концентрации исходных и конечных веществ? Влияет ли давление на смещение равновесия? Вывести константу равновесия этого процесса.
3. Найти константу равновесия и исходные концентрации веществ в равновесной системе: оксид серы (IV), кислород, оксид серы (VI), если равновесные концентрации всех компонентов системы соответственно равны: 0,04, 0,06 и 0,02 моль/л.
Ответ: константа 16,67; Сисх. оксида серы (IV) = 0,06 моль/л; Сисх. кислорода = 0,07 моль/л.
4. Если в колонне синтеза оксида серы (VI) при 6000С установилось равновесие 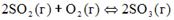 ,
,  <0, то при увеличении температуры давление в системе …
<0, то при увеличении температуры давление в системе …
1) увеличивается 2) становится равным атмосферному 3) не изменяется 4) уменьшается
5. Равновесие в системе 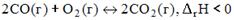 сместится вправо при …
сместится вправо при …
1) уменьшении температуры 2) уменьшении давления
3) увеличении температуры 4) повышении давления
6. При повышении давления в системе
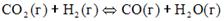 ,
, 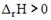 …
…
1) состояние равновесия не изменяется 2) увеличивается содержание продуктов
3) увеличивается содержание исходных веществ 4) увеличивается содержание исходных веществ и продуктов
7. В какой системе увеличение давления и понижение температуры смещает химическое равновесие в сторону продуктов реакции?
1) 2SO2(г) + O2(г) ↔2SО3(г) + Q 2) N2(г) + О2(г) ↔ 2NO(г) – Q
3) CO2(г) + 2C(тв.) ↔2CO(г) – Q 4) 2NH3(г) ↔N2(г) + 3H2(г) – Q
8. При повышении давления равновесие смешается вправо в системе
1) 2СО2(г) ↔2СО(г) + О2(г) 2) C2H4(г) ↔ С2Н2(г) + Н2(г)
3) РС13(г) + С12(г) ↔ РС15(г) 4) Н2(г) + С12(г) ↔2 НС1(г)
9. Изменение давления оказывает влияние на смешение равновесия в системе
1) 2SO2(г) + О2(г) ↔2SO3 (г) 2) СО(г) + Н2О(г) ↔ СО2(г) + Н2(г)
3) 2НI(г) ↔ Н2(г) + I2(г) 4) N2(г) + О2(г) ↔2NO(г)
10. Обратимой реакции соответствует уравнение
1) КОН + НС1 = KCI + Н2О 2) N2 + 3Н2 = 2NH3
3) FeCl3 + 3NaOH = Fe(OH)3 + 3NaCl 4) Na2О + 2HCI = 2NaCl + H2О
Дата добавления: 2015-07-20; просмотров: 43 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Задания для самоконтроля (включены в коллоквиум и зачетное занятие) | | | Анонс нового безаммиачного красителя Oro Del Marocco |