
|
Читайте также: |
Классификация и состав пластмасс. Теплопластичные и термоактивные пластмассы. Основные физико-химические свойства пластмасс. Особенности применения пластмасс на автомобилях.
Клеящие материалы.
Понятие о клеящих материалах. Разновидности клеев. Особенности применения клеящих материалов на автомобилях и их марки.
Лакокрасочные материалы.
Назначение, основные свойства лакокрасочных материалов, классификация по составу и назначению, марки.
Резины, обивочные, уплотнительные и изоляционные материалы.
Требования и основные показатели качества резины, применяемой для изготовления шин. Состав резины, ее свойства. Характеристика составных частей резиновой смеси. Ткани и другие материалы, применяемые при изготовлении шин.
Обивочные, уплотнительные и изоляционные материалы, применяемые на автомобиле.
1.7. Охрана труда и окружающей среды при использовании
эксплуатационных материалов
Токсичность, огнеопасность и взрывоопасность ЭМ.
Концентрационные и температурные пределы взрываемости и самовоспламеняемости паров жидких и газообразных топлив в воздухе. Статическое электричество и меры борьбы с ним при хранении, выдаче и транспортировании жидких и газообразных топлив. Техника безопасности и пожароопасности при приеме, хранении и выдаче ЭМ.
2. Основные формулы, необходимые для решения задач
в контрольных работах
2.1. Сгорание топлива в двигателе
Для определения теплот сгорания топлива используются формулы Д.И.Менделеева. Теплота сгорания ( ) топлива равна сумме теплот, полученных при сгорании его отдельных компонентов.
) топлива равна сумме теплот, полученных при сгорании его отдельных компонентов.
Для жидких топлив:
 (2.1.1)
(2.1.1)
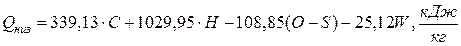 (2.1.2)
(2.1.2)
 (2.1.3)
(2.1.3)
 , (2.1.4)
, (2.1.4)
где  – высшая теплота сгорания, т.е. количество теплоты, выделяемой при сгорании 1 кг твердого или жидкого топлива, включая теплоту, выделившуюся при конденсации воды, которая образуется за счет сгорания водорода, входящего в состав топлива, кДж;
– высшая теплота сгорания, т.е. количество теплоты, выделяемой при сгорании 1 кг твердого или жидкого топлива, включая теплоту, выделившуюся при конденсации воды, которая образуется за счет сгорания водорода, входящего в состав топлива, кДж;  – количество теплоты, выделившейся при сгорании 1 кг топлива, не учитывает теплоту, выделившуюся при конденсации паров воды, кДж; C, H, O, S, – элементарный состав топлива, % (масс.); W – количество воды, содержащееся в топливе, % (масс.); 2512,08 – количество теплоты, затрачиваемой для превращения 1 кг воды в пар, кДж; q – масса паров воды, образующаяся при сгорании 1 кг топлива, кг.
– количество теплоты, выделившейся при сгорании 1 кг топлива, не учитывает теплоту, выделившуюся при конденсации паров воды, кДж; C, H, O, S, – элементарный состав топлива, % (масс.); W – количество воды, содержащееся в топливе, % (масс.); 2512,08 – количество теплоты, затрачиваемой для превращения 1 кг воды в пар, кДж; q – масса паров воды, образующаяся при сгорании 1 кг топлива, кг.
Коэффициенты показывают, какая теплота может быть получена при сгорании 1% того или иного элемента топлива. Коэффициенты учитывают затрату части энергии на разрушение химических связей в сложных соединениях топлив (при расчетах теплот сгорания допустимо округление коэффициентов до целых единиц).
Расчет количества кислорода воздуха, необходимого для сгорания топлива.
 (2.1.5)
(2.1.5)
где  – количество кислорода (кг), необходимое теоретически на сгорание 1 кг топлива;
– количество кислорода (кг), необходимое теоретически на сгорание 1 кг топлива;
 (2.1.6)
(2.1.6)
 – количество воздуха (кг),необходимое теоретически для сгорания 1 кг топлива;
– количество воздуха (кг),необходимое теоретически для сгорания 1 кг топлива;
 (2.1.7)
(2.1.7)
 – объем воздуха (м3), необходимый теоретически для сгорания 1 кг топлива.
– объем воздуха (м3), необходимый теоретически для сгорания 1 кг топлива.
Избыток или недостаток воздуха в горючей смеси характеризуется  – коэффициентом избытка воздуха:
– коэффициентом избытка воздуха:
Нормальная смесь 
Богатая смесь 
Бедная смесь 
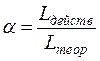 ;
;  , (2.1.8)
, (2.1.8)
где 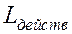 – действительная масса (или объем) воздуха в смеси;
– действительная масса (или объем) воздуха в смеси;  – теоретически необходимая масса (или объем) воздуха в смеси.
– теоретически необходимая масса (или объем) воздуха в смеси.
В производственных условиях  обычно определяют по анализу количественного состава продуктов сгорания.
обычно определяют по анализу количественного состава продуктов сгорания.
100 = СО2 + СО + О2 + SO2 +N2, (2.1.9)
где СО2, СО, О2, SO2,N2 – компоненты продуктов сгорания топлива в двигателе, % (объем.).
N2 = 100 – (СО2 + СО + О2 + SO2). (2.1.10)
Если в отработавших газах есть СО, то
 (2.1.11)
(2.1.11)
Если полное сгорания, то
 [1] (2.1.12)
[1] (2.1.12)
или  [5]. (2.1.13)
[5]. (2.1.13)
Теплоту сгорания горючей смеси можно рассчитать по формуле:
 . (2.1.14)
. (2.1.14)
Для газообразных топлив.
 (2.1.15)
(2.1.15)
 , (2.1.16)
, (2.1.16)
где СО, Н2, СН4, СnHm – количество компонентов топлива, % (объем.), измеренное при Т=2730К, р=101,3 кПа.
Если топливо влажное (присутствуют пары воды):
 , (2.1.17)
, (2.1.17)
где 0,805 – масса 1 м3 водяного пара, кг; d – содержание паров воды в 1 м3 газа, кг.
 , (2.1.18)
, (2.1.18)
где СО,Н2, СnHm, О2 – содержание компонентов топлива, % (объем.); 21 – содержание кислорода в воздухе, % (объем.).
2.2. Исправление качества ТСМ, снижение которого произошло
при хранении и транспортировке.
2.2.1. Соотношение нефтепродуктов, необходимых для смешения при исправлении показателей: октановое и цетановые числа топлив, фракционный состав, плотность, содержание серы, фактических смол, кислотное число – определяется следующим образом:
Соотношение нефтепродуктов, необходимых для смешения, определяют по формуле:
 , (2.2.1)
, (2.2.1)
где  – масса нефтепродукта, имеющего запас качества по исправляемому показателю;
– масса нефтепродукта, имеющего запас качества по исправляемому показателю;  – масса нестандартного нефтепродукта; Х – значение показателя, которое нужно получить после смешения; ХА – значение показателя нефтепродукта, имеющего запас качества; ХБ – значение показателя качества нестандартного нефтепродукта.
– масса нестандартного нефтепродукта; Х – значение показателя, которое нужно получить после смешения; ХА – значение показателя нефтепродукта, имеющего запас качества; ХБ – значение показателя качества нестандартного нефтепродукта.
При необходимости получить искомую пропорцию в процентах по массе пользуются формулой:
 . (2.2.2)
. (2.2.2)
2.2.2. Для исправления вязкости нефтепродуктов необходимо пользоваться формулой:
 , (2.2.3)
, (2.2.3)
где Х – искомая кинематическая вязкость смеси, мм2/с; ХА, ХБ – кинематическая вязкость компонентов, вовлекаемых в смесь, при этом ХА – большая величина по значению вязкости, мм2/с; РА, РБ – доля компонентов в смеси, % (масс); К – поправочный коэффициент, его значения приведены в таблице 2.1.
Таблица 2.1
Значения поправочного коэффициента К при определении
вязкости смеси моторных масел
| Соотношение компонентов, % масс | Значение коэффициента К | |
| А – масло с запасом качества | Б – масло, имеющее ухудшенный показатель | |
| –– |
2.3. Определение жесткости воды
Жесткость (Ж) воды измеряется в миллимолях эквивалентов ионов кальция и магния на литр воды (ммоль экв/л).
Один ммоль экв/л жесткости соответствует содержанию 20,04 мг/л ионов кальция (Са2+) или 12,16 мг/л ионов магния (Mg2+).
ЖО = ЖВ + ЖП, (2.3.1)
где ЖО – общая жесткость обуславливается содержанием в воде всех растворимых солей кальция и магния; ЖВ – временная (карбонатная) жесткость, зависит от количества растворенных в воде кислых солей Са и Мg – Ca(HCO3)2 и Mg(HCO3)2. Эти соли при температуре выше 80 – 850С разлагаются и выпадают в осадок в виде накипи и шлака.
Реакции протекают по следующей схеме:
Са(HCO3)2  СаCO3
СаCO3  + CO2
+ CO2  + Н2О
+ Н2О
ЖП – постоянная (некарбонатная) жесткость зависит от количества растворенных в воде солей: CaCl2, MgCl2, CaSO4, MgSO4, CaSiO3, MgSiO3 и др.. Эти соли при кипячении воды в осадок не выпадают, если их концентрация не превышает предела насыщения. Общую жесткость воды можно посчитать по формуле:
 . (2.3.2.)
. (2.3.2.)
3. Задания для контрольных работ
3.1. Контрольная работа № 1
1. Нефть как сырье для производства топлив и масел.
2. Групповой состав нефти. Влияние химического состава нефти на свойства получаемых топлив и масел.
3. Современные методы получения топлив и смазочных материалов их нефти, очистка нефтепродуктов.
4. Общие требования к моторным топливам и их основные эксплуатационные свойства.
5. Классификация топлив. Эксплуатационные свойства топлив.
6. Автомобильные топлива. Марки, состав, характеристики качества.
7. Автомобильные бензины. Эксплуатационные требования к свойствам.
8. Свойства бензинов прямой и деструктивной переработки. Ассортимент бензинов.
9. Карбюрационные свойства бензинов (плотность, вязкость, испаряемость, давление насыщенных паров, низкотемпературные).
10. Испаряемость бензинов. Пусковые свойства. Прогрев, приемистость, износ и экономичность работы двигателя.
11. Нормальное и детонационное сгорание бензина в двигателе внутреннего сгорания. Калильное зажигание.
12. Сгорание бензина в двигателе. Основные характеристики.
13. Сущность детонационного горения топлива. Внешние признаки. Антидетонаторы.
14. Детонация. Антидетонационные свойства бензинов. Октановое число.
15. Характеристика процессов горения бензина в двигателе. Теплота сгорания. Коэффициент избытка воздуха.
16. Влияние качества бензина на работу двигателя и расход бензина.
17. Автомобильные бензины. Марки, состав, характеристики качества.
18. Пути повышения детонационной стойкости бензинов.
19. Свойства бензинов, влияющие на образование отложений в двигателе.
20. Фракционныый и групповой состав бензинов. Горючая смесь.
21. Воспламеняемость и горючесть бензинов. Закономерности процессов воспламенения и горения, характеристики этих процессов.
22. Классификация эксплуатационных свойств автомобильных бензинов.
23. Меры борьбы с количественными и качественными потерями бензина.
24. Детонация. Причины. Методы борьбы с данным явлением.
25. Характеристика коррозионной активности бензинов, защитных свойств топлив.
26. Влияние свойств бензинов на надежность и экономичность работы двигателя.
27. Присадки к бензинам. Назначение, свойства и эффективность использования. Антидетонационные присадки и механизм их действия.
28. Влияние свойств бензинов на надежность и экономичность работы двигателей в различных эксплуатационных условиях. Стабильность бензинов.
29. Ассортимент бензинов.
30. Дизельные топлива. Эксплуатационные требования к свойствам.
31. Показатели и свойства дизельного топлива, влияющие на подачу и смесеобразование.
32. Нормальное и жесткое сгорание дизельного топлива в двигателе внутреннего сгорания. Оценка самовоспламеняемости топлива. Цетановое число.
33. Самовоспламеняемость дизельных топлив. Методы оценки самовоспламеняемости. Способы повышения самовоспламеняемости топлив. Влияние цетанового числа на рабочий процесс дизеля.
34. Коррозионные свойства дизельного топлива. Изменение качества топлива при хранении и транспортировке.
35. Низкотемпературные свойства дизельных топлив.
36. Влияние свойств дизельного топлива на образование отложений в двигателе.
37. Меры борьбы с количественными и качественными потерями дизтоплива.
38. Влияние строения углеводородов на свойства полученных топлив (бензинов и дизтоплив).
39. Совместимость топлив с материалами. Закономерности протекания коррозии.
40. Сгорание топлива в дизеле. Характеристики процесса. Охарактеризуйте фазы горения дизельного топлива.
41. Ассортимент дизельных топлив.
42. Влияние качества дизельного топлива на работу двигателя и его расход.
43. Современные и перспективные дизельные топлива.
44. Испаряемость, воспламеняемость и горючесть дизельного топлива.
45. Характеристика воспламеняемости и горючести дизельного топлива.
46. Самовоспламеняемость дизельных топлив. Цетановое число.
47. Свойства дизельных топлив, влияющие на образование отложений в двигателе.
48. Коррозионные свойства дизельных топлив.
49. Дизельные топлива. Марки, состав, характеристики качества.
50. Причины газовой и жидкостной сернистой коррозии деталей двигателей.
51. Сгорание топлива в быстроходных дизельных двигателях.
52. Причины нагарообразования в дизелях. Меры борьбы с нагарообразованием.
53. Естественные газообразные топлива.
54. Особенности применения и экономические показатели работы двигателей на газообразном топливе.
55. Свойства сжиженных газов (теплоты сгорания, критическая температура, коррозионность, нагарообразующая способность, температура кипения, детонационная стойкость).
56. Свойства сжатых газов.
57. Преимущества и недостатки газообразного топлива.
58. Газообразные топлива. Эксплуатационные требования к свойствам. Особенности применения.
59. Заменители нефтяных топлив.
60. Перспективные топлива для автомобилей. Общие характеристики и свойства.
61. При сгорании 2 кг топлива получено 93766,4 кДж теплоты и 2,9 кг паров воды. Определить максимально возможное количество теплоты (кДж), полученное при сгорании и элементарный состав топлива (% масс.), считая его углеводородным.
62. Определить количество воздуха (кг. и м3), израсходованного при сгорании 20 кг. дизельного топлива состава: О=85,7%, Н=13,3%, S=0,67%, N=0,15%, остальное ‑ кислород. Состав отработавших газов: СО2= 11,7%, О2=3,7%, СО=0,5%, SO2=0,9%.
63. Дизельное топливо, состоящее из смеси равных количеств углеводородов С16Н34 и С10Н7СН3, сгорело в двигателе с коэффициентом избытка воздуха 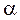 =1,3. Определить теплоту сгорания (Qвысш., Qниз.), L действительное и цетановое число.
=1,3. Определить теплоту сгорания (Qвысш., Qниз.), L действительное и цетановое число.
64. При сжигании 1,5 кг топлива получено 70481,8 кДж теплоты и 2,1 кг паров воды. Определите максимально возможное количество теплоты и количество водорода, содержащегося в топливе.
65. Газовое топливо (Пермьнефть) имеет следующий состав: СН4=38,7%, С2Н6=22,6%, С3Н8=10,7%, С4Н10=3,4%, остальное ‑ негорючие компоненты. Определить название газа, количество воздуха, необходимого для полного сгорания газа, и его теплоту сгорания.
66. Определить количество воздуха, израсходованного при сжигании 20 литров дизельного топлива С=85,4%, Н=13,2%, S=0,8%, О=0,6%,  =0,825 г/см3, если анализ продуктов сгорания дал следующие результаты: СО2=10,5%, О2=5,1%, СО=0,4%, SO2=0,85%.
=0,825 г/см3, если анализ продуктов сгорания дал следующие результаты: СО2=10,5%, О2=5,1%, СО=0,4%, SO2=0,85%.
67. Определить теплоту сгорания 3 л. нормальной смеси углеводорода С9Н12, имеющего плотность  = 0,8618 г/см3.
= 0,8618 г/см3.
68. Сколько выделилось теплоты при сжигании 5 м3 газа (месторождение Коми республика) следующего состава: СН4 = 95,7%, С2Н6=1,9%, С3Н8=0,5%, С4Н10=0,4%, N=1,3%. Какой газ сгорел в горелке?
69. Определить количество воздуха (кг), израсходованного при сжигании 10 литров дизельного топлива и количество теплоты, которое при этом выделилось. Состав топлива: С=86,1%, Н=12.9%, S=0.57%, О=0,43%,  =0,841 г/см3. Анализ продуктов сгорания дал следующие результаты: СО2= 11,8%, О2=6,2%, СО=0,5%, SO2=0,83%.
=0,841 г/см3. Анализ продуктов сгорания дал следующие результаты: СО2= 11,8%, О2=6,2%, СО=0,5%, SO2=0,83%.
70. Вычислить массу и объем воздуха, теоретически необходимого (при н.у.) для полного сгорания бензина массой 2 кг. Примерный состав бензина (в массовых долях): С=0,86, Н=0,14.
71. Октановое число бензина А‑76 оказалось в результате анализа 72 единицы. Сколько надо взять бензина АИ‑95, чтобы исправить исходный бензин?
72. Определить теплоту сгорания горючей смеси (кДж). Состав бензина С-85,1%, Н=14,7%, S=0,1%, О=0,1%. Состав отработавших газов: СО2=10,2%, О2=4%, СО=1,0%.
73. Определить массу и объем воздуха, израсходованного на сжигание 10 кг бензина состава: С=85,6%, Н=14,2%, S=0,1%, О=0,1%. Состав отработавших газов: СО2=11,5%, О2=3%, СО=1,0%.
74. Определить теплоту сгорания горючей смеси (кДж) трех литров углеводорода 2-метил-3-этилпентана, имеющего плотность 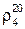 = 0,7193 г/см3. Коэффициент избытка воздуха –1,3.
= 0,7193 г/см3. Коэффициент избытка воздуха –1,3.
75. Состав нефтяного газа (в объемных долях): СО2=0,05, СО=0,08, Н2=0,24, СН4=0,40, С2Н4=0,06, N2=0,17. Сколько выделилось теплоты при сжигании 10 м3 газа?
76. Анализом установлено, что октановое число бензина АИ‑93 по моторному методу составляет 83 единицы. Сколько и какого бензина необходимо добавить, чтобы исправить исходный бензин?
77. Вычислить массу и объем воздуха, теоретически необходимого (при н.у.) для полного сгорания 15 кг бензина состава (в массовых долях): С – 0,92; Н – 0,08.
78. Анализом установлено, что октановое число бензина А‑80 составляет 78 единиц. Сколько и какого бензина необходимо добавить для того, чтобы исправить исходный бензин?
79. При сгорании 5,6 кг топлива получено 262545,9 кДж тепла и 8,12 кг паров воды. Определить максимально возможное количество полученного теплоты в кДж и элементарный состав топлива, считая его углеводородным, выразив его в процентах.
80. Определить массу и объем воздуха, необходимого для сжигания 15 кг дизельного топлива. Состав его: С – 85,7%; Н – 13,3%; S – 0,67%; N – 0,15%; О – 0,18%. Состав отработавших газов: СО2 – 12,1%, О2 – 3,8%, СО – 0,8%, SO2 – 0,1%.
81. Газовое топливо имеет следующий состав: СН4 – 38,6%, С2Н6 – 22,8%, С3Н8 – 10,5%, С4Н10 – 3,4%, остальное – негорючие компоненты. Определить название газа, объем воздуха, необходимого для полного сгорания газа, теплоту его сгорания.
82. Состав топлива: С – 0,86; Н – 0,13; S – 0.006; О – 0,0043 (даны массовые доли). Плотность топлива ρ=0,841 г/см3. Продукты сгорания: СО2 11,8%; СО – 0,05%; О2 – 6,2%; SO2 – 0,83%. Определить объем воздуха (при н.у.), израсходованный на сжигание 20 м3 топлива и количество выделившейся теплоты.
83. При сжигании 4,5 кг топлива получено 105722,66 кДж теплоты и 6,3 кг паров Н2О. Определить массовую долю водорода в топливе (топливо углеводородное) и Qвысш.
84. Сколько надо взять бензина АИ-98, чтобы исправить исходный бензин А-80, октановое число которого, как показал анализ, оказалось равным 77?
85. Определить количество воздуха, необходимого для полного сгорания 20 м3 газа следующего состава: СН4 =92,0%; СnНm =2,0%; Н2 =2,0% СО2 =3,5%; N2 =0,5%.
86. Определить действительно израсходованное количество воздуха в кг и м3 при сгорании 20 кг дизельного топлива состава: С=84,2%, Н=12,9%, S=0,80%, N=0,2%, остальное ‑ кислород. Состав отработавших газов СО2= 12,6%, О2=5,3%, СО=0,2%, SO2=0,4%.
87. Определить теплоту сгорания 8 л. нормальной смеси углеводорода С8Н10, имеющего плотность  = 0,740 г/см3.
= 0,740 г/см3.
88. При сжигании 3 кг топлива получено 129345 кДж теплоты и 3,9 кг паров воды. Определите максимально возможное количество теплоты и количество водорода, содержащегося в топливе, если считать топливо углеводородным.
89. Газовое топливо имеет следующий состав: пропан С3Н8=92%, С4Н10=3,0%, С2Н4=3,0%, остальные ‑ негорючие компоненты. Определить название газа, количество воздуха, необходимые для полного сгорания газа, и его теплоту сгорания.
90. Сколько выделилось тепла при сжигании 6 м3 газа следующего состава: СН4=90,0%, СnHm=3,0%, Н2=3,0%, СО2=3,0%, N=1,0%. Какой газ сгорел в горелке?
3.2. Контрольная работа № 2
91. Назначение смазочных материалов. Эксплуатационные требования. Виды трений.
92. Зависимость свойств смазывающих материалов от углеводородного сырья.
93. Получение масел из нефти.
94. Масла для двигателей. Понятие о трении и износе. Основные требования к качеству.
95. Моторные масла. Свойства. Эксплуатационные требования к качеству масел.
96. Процессы, происходящие с моторным маслом в работающем двигателе.
97. Физическая и химическая стабильность моторных масел. Старение, угар, смена.
98. Работа масел в узлах трения. Закоксовывание поршневых колец. Виды отложений.
99. Окисление масел. Термоокислительная стабильность. Моющие свойства. Противоизносные и антикоррозийные свойства.
100. Противоокислительные, противоизносные и диспергирующие свойства моторных масел.
101. Смазывающие и противокоррозионные свойства масел для поршневых двигателей.
102. Взаимозависимость изменений показателей качества масел и технического состояния двигателя.
103. Срабатываемость моторных масел.
104. Пути повышения экономии моторных масел, снижение расхода.
105. Классификация моторных масел.
106. Контроль качества и оценка старения моторных масел. Пути снижения расхода масла.
107. Пути улучшения эксплуатационных свойств моторных масел.
108. Контроль качества моторных масел. Браковочные показатели.
109. Старение, угар и смена моторных масел. Взаимозаменяемость масел.
110. Система смазки поршневых двигателей. Требования к качеству масел.
111. Трансмиссионные масла. Система смазки трансмиссий. Требования к качеству.
112. Трансмиссионные масла. Свойства. Эксплуатационные требования к качеству масел.
113. Сущность классификации трансмиссионных масел.
114. Влияние на эксплуатационные характеристики смазочных материалов вязкости, поверхностного натяжения, плотности, температуры. Индекс вязкости.
115. Склонность масел к образованию отложений.
116. Закономерности процессов образования отложений.
117. Роль присадок в улучшении качества работы масел (моторных и трансмиссионных).
118. Противоокислительные, диспергирующие, защитные и антикоррозиионые свойства масел.
119. Пути снижения расхода масел.
120. Оценка качества масел в процессе работы.
121. Синтетические масла. Особенности, свойства и применение.
122. Роль синтетических масел в улучшении обеспечения автомобильного транспорта маслами.
123. Влияние изменений свойств топливосмазочных материалов на работу автомобиля.
124. Пластичные смазки. Сведения о структуре, составе и принципах производства смазок. Назначение. Ассортимент.
125. Особенности строения и эксплуатационные свойства пластичных смазок.
126. Основные эксплуатационные требования к свойствам пластичных смазок. Методы их оценки. Ассортимент и применение.
127. Состав и коллоидная структура смазок. Назначение и классификация смазок.
128. Основы применения пластичных смазок. Назначение, классификация.
129. Назначение и классификация смазок. Требования к качеству смазок.
130. Свойства пластичных смазок.
131. Ассортимент пластичных смазок и их применение.
132. Антифрикционные и консервационные смазки. Назначение, классификация, подбор и совместимость.
133. Антифрикционные, консервационные и уплотнительные смазки. Требования и свойства
134. Масла для гидравлических систем. Эксплуатационные требования. Классификация.
135. Особенности работы масел в гидравлических передачах. Ассортимент. Взаимозаменяемость.
136. Жидкости для гидравлических систем. Марки, состав, характеристики качества.
137. Особенности работы масел в гидромеханических передачах. Ассортимент.
138. Тормозные и амортизаторные жидкости. Эксплуатационные требования. Ассортимент.
139. Тормозные жидкости. Эксплуатационные требования. Ассортимент.
140. Технические жидкости. Эксплуатационные требования. Назначение.
141. Охлаждающие жидкости. Условия применения и требования к качеству.
142. Этиленгликолевые охлаждающие жидкости. Достоинства и недостатки.
143. Вода как охлаждающая жидкость. Жесткость воды. Методы ее устранения.
144. Охлаждающие низкозамерзающие жидкости, основные свойства, маркировка, рекомендации по применению, замене и технике безопасности.
145. Антифризы. Эксплуатационные требования. Ассортимент.
146. Пусковые жидкости. Эксплуатационные требования. Ассортимент.
147. Коррозия автомобилей в процессе эксплуатации. Методы защиты.
148. Организация рационального применения топливо-смазочных материалов по экономии ТСМ.
149. Резины, обивочные, уплотнительные и изоляционные материалы, применяемые на автомобиле.
150. Пластические материалы. Классификация и состав пластмасс. Особенности применения пластмасс на автомобилях.
151. Определить марку моторного масла, если известны следующие данные:  =11,2 сСТ, ИВ 95, щелочность 6,0 мг/г, зольность - 1,15%, температура вспышки 223 0С, температура застывания ‑ (-19 0С). В каких двигателях и в какое время года можно использовать данное масло?
=11,2 сСТ, ИВ 95, щелочность 6,0 мг/г, зольность - 1,15%, температура вспышки 223 0С, температура застывания ‑ (-19 0С). В каких двигателях и в какое время года можно использовать данное масло?
152. В результате анализа установлено, что кинематическая вязкость моторного масла М‑10Г2 равна 11,3 мм2/с (стандартного), а нестандартного ‑ 9,8 мм2/с. Чему будет равна вязкость смеси данных масел, взятых в соотношении 60:40? Можно ли ее использовать для эксплуатации?
153. Определить индекс вязкости моторного масла, если известно, что кинематические вязкости его при 1000С и 50 0С равны соответственно 11сСт и 60 сСТ. В каких двигателях и в какое время года можно использовать данное масло, если его зольность 1,3%, а щелочность составляет 7,5 мг/г.
154. Имеются два масла с одинаковой вязкостью при 100 0С (10 мм2/с). Вязкость первого масла при 50 0С ‑ 62 мм2/с, второго‑ 46 мм2/с. Какое масло более пригодно для зимней эксплуатации и какой у него индекс вязкости?
155. Определить марку масла, если известны следующие данные:  - 12,2 мм2/с, ИВ 90, щелочность 8,7 мг/г, зольность 1,1 %, температура вспышки 220 0С, температура застывания ‑18 0С. В каких двигателях и в какое время года можно использовать данное масло?
- 12,2 мм2/с, ИВ 90, щелочность 8,7 мг/г, зольность 1,1 %, температура вспышки 220 0С, температура застывания ‑18 0С. В каких двигателях и в какое время года можно использовать данное масло?
156. Двигатель работает в зимних условиях, когда температура окружающего воздуха равна ‑ 30 0С. Какое должно быть процентное содержание этиленгликоля в охлаждающей жидкости, чему равна плотность данного раствора?
157. Двигатель работает в зимних условиях, когда температура окружающего воздуха равна ‑20 0С. Какое должно быть процентное содержание этиленгликоля в охлаждающей жидкости. Чему равна плотность данного раствора?
158. Установлено, что кинематическая вязкость масла  = 9 мм2/с, при 50 0С ‑37 мм2/с. ИВ‑120, t0(вспышки) 160 0С, температура застывания ‑20 0С. Определить марку масла и его назначение.
= 9 мм2/с, при 50 0С ‑37 мм2/с. ИВ‑120, t0(вспышки) 160 0С, температура застывания ‑20 0С. Определить марку масла и его назначение.
159. Определить индекс вязкости моторного масла, если известно, что кинематические вязкости его при 100 0С и 50 0С равны соответственно 10сСт и 46 сСт. В каких двигателях и в какое время года можно использовать данное масло, если его зольность не более 0,9%, а щелочное число составляет 5,0 мг/г.
160. В результате анализа установлено, что кинематическая вязкость стандартного моторного масла М‑10В2 при 100 0С равна 11,4 сСт, а нестандартного ‑ 10,2 сСт. Сколько надо добавить стандартного масла к нестандартному для продолжения его эксплуатации.
161. Определить марку трансмиссионного масла, если известны следующие данные: 
 =15 сСТ, ИВ 80, температура вспышки не ниже 180 0С, температура застывания ‑ (-20 0С). Где и когда можно использовать данное масло?
=15 сСТ, ИВ 80, температура вспышки не ниже 180 0С, температура застывания ‑ (-20 0С). Где и когда можно использовать данное масло?
162. Двигатель работает в зимних условиях, когда температура окружающего воздуха равна ‑400С. Какое должно быть процентное содержание этиленгликоля в охлаждающей жидкости, чему равна плотность данного раствора?
163. Имеются два масла с одинаковой вязкостью при 100 0С (9 мм2/с). Вязкость первого масла при 50 0С ‑ 40 мм2/с, второго ‑ 50 мм2/с. Какое масло более пригодно для зимней эксплуатации и какой у него индекс вязкости?
164. Установлено, что кинематическая вязкость моторного масла  = 8 сСТ, при 50 - 40 сСТ. ИВ‑95, температура вспышки 2100С, температура застывания ‑ (-300С), щелочное число 4,6 мг/г, зольность – 0,90%. Определить марку масла и его назначение.
= 8 сСТ, при 50 - 40 сСТ. ИВ‑95, температура вспышки 2100С, температура застывания ‑ (-300С), щелочное число 4,6 мг/г, зольность – 0,90%. Определить марку масла и его назначение.
165. В результате анализа установлено, что кинематическая вязкость стандартного трансмиссионого масла ТМ‑3‑18 при 100 0С равна 15 сСТ, а нестандартного ‑ 13,4 сСТ. Сколько надо добавить стандартного масла к нестандартному для продолжения его эксплуатации?
166. Двигатель работает в зимних условиях, когда температура окружающего воздуха равна ‑ 150С. Какое должно быть процентное содержание этиленгликоля в охлаждающей жидкости, чему равна плотность данного раствора?
167. При кипячении 250 мл. воды, содержащей гидрокарбонат кальция, выпал осадок массой 3,5 мг. Чему равна жесткость воды?
168. В 4 литрах воды содержится 38 мг. Mg2+ и 108 мг. Са2+. Вычислить общую жесткость воды.
169. Образец воды объемом 2 литра содержит 48,6 мг. гидрокарбоната кальция и 29,6 мг. сульфата магния. Какое количество Са2+ и Mg2+ содержится в 1 литре образца воды? Чему равна общая жесткость воды?
170. Какую массу гашеной извести надо прибавить в 2,5 литра воды, чтобы устранить ее временную жесткость, равную 4,43 ммоль экв/л?
171. Чему равна временная жесткость воды, в 2 литрах которой содержится 0,146 г. гидрокарбоната магния?
172. Определить жесткость минеральной воды “Нарзан”, если в объеме 4 литра содержится ионов кальция массой 1,5936 г. и ионов магния массой 0,3536 г.
173. Чему равна жесткость воды, если для ее устранения в воде объемом 20 литров добавлено карбоната натрия массой 3,71 г.?
174. Определить карбонатную жесткость, если на осаждение карбонатов из 500 мл. воды израсходовано 0,265 г. карбоната натрия.
175. Определить временную жесткость воды, в 5 литрах которого содержится 0,405 г гидрокарбоната кальция.
176. Рассчитать жесткость воды, в 10 литрах которой содержится 4,44 г. хлорида кальция.
177. Определить массу гашеной извести которую необходимо добавить к 1000 л. воды, чтобы устранить ее временную жесткость, равную 1,45 ммоль экв/л.
178. Чему равна жесткость воды, если для ее устранения в воде объемом 20 литров добавлено карбоната натрия массой 3,71 г.
179. Определите жесткость воды, если в 200 мл содержится кальция массой 20 мг. и иона магния массой 8 мг.
180. Минеральная вода содержит 0,3894 г/л ионов кальция и 0,0884 г/л ионов магния. Какова общая жесткость этой воды? Какова масса этих ионов в 5 л воды? Какие соли обуславливают жесткость минеральной воды?
3.3. Варианты контрольных работ
3.3.1. Варианты контрольных работ для студентов, обучающихся
по полным учебным программам
| Контрольная работа № 1 | Контрольная работа № 2 | |||||
| Номер варианта | Номера заданий, относящихся к данным работам | |||||
| 01 02 03 04 05 06 07 08 09 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 | 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 | 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 | 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 89 90 | 91 92 93 94 95 96 97 98 99 100 101 102 103 104 105 106 107 108 109 110 111 112 113 114 115 116 117 118 119 120 | 121 122 123 124 125 126 127 128 129 130 131 132 133 134 135 136 137 138 139 140 141 142 143 144 145 146 147 148 149 150 | 151 152 153 154 155 156 157 158 159 160 161 162 163 164 165 166 167 168 169 170 171 172 173 174 175 176 177 178 179 180 |
3.3.1. Варианты контрольных работ для студентов, обучающихся
по сокращенным учебным программам
| Номер варианта | Номера заданий, относящихся к контрольной работе | |||
| 01 02 03 04 05 06 07 08 09 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 | 1 2 3 5 7 9 10 11 13 14 15 18 20 25 29 30 31 33 35 36 38 41 44 48 55 56 57 58 59 60 | 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 89 90 | 91 92 95 97 100 101 105 108 112 113 114 117 120 121 122 123 125 126 127 130 134 138 140 141 143 145 146 147 149 150 | 151 152 153 154 155 156 157 158 159 160 161 162 163 164 165 166 167 168 169 170 171 172 173 174 175 176 177 178 179 180 |
4. Примеры решения задач
Пример 1.
При сжигании 1 кг топлива получено 43124 кДж теплоты и 1,3 кг паров воды. Определить максимально возможное количество теплоты (в кДж), полученное при сгорании (Qвыс), количество водорода, содержащегося в топливе, и состав топлива, если считать его углеводородным.
Решение.
1. Известно, что Qниз.=Qвыс. -2512,08×q (кДж/кг) (2.1.4), следовательно, Qвыс. = Qниз. + 2512,08×q. В нашей задаче Qниз. = 43124 кДж/кг, а q=1,3 кг;
Qвыс. = 43124 + 2512,08×1,3=46389,7 (кДж/кг).
2. В состав 1 моля воды (H2O) входит 2 моля атомов H
М(Н)=1 г/моль; М(Н2О)=18 г/моль.
Составим соотношение:
18 г H2O образуется из 2 г H
1,3×103 х
x = m(H) =  = 144 (г) = 0,144 кг.
= 144 (г) = 0,144 кг.
Это масса водорода, содержащегося в топливе.
3. По условию задачи масса сгоревшего топлива 1 кг, в нем содержалось 0,144 кг водорода и, следовательно, 0,856 кг углерода, что составляет 14,4% водорода (Н) и 85,6% углерода (С) соответственно.
Дата добавления: 2015-07-11; просмотров: 127 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Для студентов заочной формы обучения | | | Решение. |