
Читайте также:
|
1. До начала титрования, т.е. в чистом растворе одноосновной слабой кислоты концентрации  и
и  равны между собой, а концентрация
равны между собой, а концентрация  практически равна концентрации исходной кислоты при условии, что степень диссоциации достаточно мала.
практически равна концентрации исходной кислоты при условии, что степень диссоциации достаточно мала.
В соответствии с этим константа диссоциации представлена в виде:
Кк-ты= 



pH
2. В промежуточных точках титрования слабой кислоты сильным основание образуется буферный раствор, содержащий одновременно свободную слабую кислоту и соль этой кислоты.
Расчет величины рН в этом случае так же рассчитывается из Кк-ты, которая в присутствии соли может быть представлена в виде:
К= 
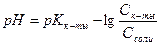
50%: 
90%: 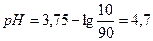
99%: 
99,9%: 
3. В точке эквивалентности.
Образуется соль, гидролиз которой обуславливает щелочную реакцию среды. Значит


4. После точки эквивалентности концентрацию избытка рабочего раствора (щелочи) рассчитывают аналогично расчету точек при f>1 для титрования сильной кислоты сильным основанием, т.к. присутствие сильной щелочи подавляет гидролиз соли, что определяет величину рН в этом случае присутствующей в растворе свободной щелочью.
 =
=  ;
;  ;
; 
100,1%:  =
= 


101%:  =
= 
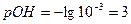

110%:  =
= 


На основе полученных данных строим кривую титрования (рис.1)
Дата добавления: 2015-07-11; просмотров: 225 | Нарушение авторских прав