
Читайте также:
|
Химизм процесса. Наиболее распространенной теорией, объясняющей механизм каталитического крекинга на алюмосиликатных катализаторах, является теория карбоний-иона. Эта теория была впервые предложена для объяснения механизма полимеризации над кислотными катализаторами (H2SO4, H3PO4, AlCl3). Теперь эта теория распространяется и на каталитический крекинг в присутствии алюмосиликатного катализатора, так же имеющего кислотный характер. В основе этой теории лежат следующие представления:
Ионы карбония аналогичны ионам аммония и содержат трехвалентный положительно заряженный атом углерода. Легче всего они образуются при взаимодействии протона катализатора с олефинами.

Путем внутренней перегруппировки или взаимодействия с другими молекулами сырья, неустойчивые ионы карбония стремятся перейти в более устойчивые формы. Они отличаются очень большой реакционной способностью и могут вступать в самые разнообразные реакции. Это:
а) Перегруппировка атомов в молекуле с перемещением водорода или метильных групп (иначе говоря, скелетная изомеризация, приводящая к образованию изомерного иона)
б) Взаимодействие с нейтральными молекулами с образованием новых ионов карбония и новых молекул как предельных, так и непредельных.
в) Распад карбоний-иона с большим числом углеродных атомов. Расщепление, как правило, происходит по β-связи, считая от заряженного атома углерода. Продукты распада – это олефин и меньший карбоний-ион.
В целом, согласно теории ионов карбония, механизм каталитического крекинга представляется в виде цепных реакций. Зарождение цепи происходит под действием иона водорода катализатора
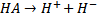
Здесь под HA подразумевается алюмосиликатный катализатор.
Развитие цепи идет по линии разнообразных превращений ионов карбония и водородного обмена с нейтральными молекулами. Наконец, обрыв цепи происходит в результате реакции между ионом карбония (катион) и анионом алюмосиликата.
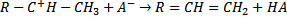
Катализатор в конечном итоге регенерируется в исходное состояние и процесс может начинаться снова. Если поверхность катализатора еще сохраняет свою активность. Химизм каталитического крекинга значительно отличается. На это влияют как кинетические факторы, так и специфические свойства катализатора. Основные особенности химизма каталитического крекинга следующие:
| Термический крекинг | Каталитический крекинг |
| Парафины | Олефины |
| Олефины | Ароматические углеводороды с большим числом боковых цепей |
| Нафтены | Нафтены |
| Алкиллированные ароматические углеводороды | Парафины |
| Голоядерные ароматические углеводороды | Голоядерные ароматические углеводороды |
1. Склонность к превращениям у различных классов углеводородов при каталитическом и термическом крекинге различны. Выше в таблице расположены для сравнения основные группы углеводородов в ряды, возрастающие по термической стабильности. Особенно характерно при каталитическом крекинге высокая реакционная способность олефинов и малая парафинов. Указанная последовательность объясняется избирательной адсорбцией различных углеводородов на поверхности катализатора. В первую очередь катализатор адсорбирует ненасыщенные богатые энергией соединения. Это диолефины, олефины, ароматические соединения. Адсорбция парафинов при работе с сырьем сложного состава незначительна. Именно поэтому ускорение реакции крекинга в присутствии катализаторов для олефинов и ароматических углеводородов в сотни и даже тысячи раз превышает ускорение распада парафинов. Однако, по мере обеднения реакционной смеси ненасыщенными углеводородами, парциальное давление предельных углеводородов над катализатором увеличивается. Это приводит к усилению адсорбции и увеличению скорости превращений. Селективная адсорбция служит причиной ступенчатого последовательного хода процесса, при котором углеводороды, сильно сорбирующиеся катализатором, тормозят реакции слабо сорбирующихся углеводородов. При термическом крекинге все компоненты сырья претерпевают превращения одновременно и кажущаяся селективность процесса объясняется лишь различием в величине констант скорости тех или иных реакций.
2. Наиболее характерной особенностью химических превращений углеводородного сырья при каталитическом крекинге является значительное развитие реакции изомеризации. Изомерные превращения хорошо объясняются с точки зрения теории карбоний-иона. В результате изомеризации ненасыщенных осколков и дальнейшего их насыщения их водородом, в продуктах крекинга накапливаются изопарафиновые углеводороды. В частности весьма характерно высокое содержание изобутана в крекинг-газе.
Связь продуктов каталитического крекинга с механизмом и кинетикой процесса.
Химический состав продуктов каталитического крекинга имеет характерные особенности:
1. Этот бензин содержит много изопарафинов и ароматических
2. Газ получается тяжелый с высокой концентрацией изобутана и олефинов
3. Газойлевые фракции богаты полициклическими и ароматическими углеводородами
Это своеобразие химического состава объясняется следующими причинами:
1. Различие механизма реакции термического и каталитического крекинга. Реакции термического крекинга протекают по радикально-цепному механизму, а каталитического через карбоний-ион.
2. Способностью активной поверхности катализатора селективно ускорять некоторые реакции (например, изомеризацию олефинов, скорость которой при термическом крекинге очень мала). Однако в присутствии катализатора может повыситься скорость только тех реакций, которые для данного интервала температур термодинамически вероятны.
Физико-химические явления процесса. Применительно к каталитическому крекингу необходимо рассматривать не только химизм протекания процесса, но и сопровождающие его физико-химические явления. Постадийно процесс каталитического крекинга может быть представлен следующим образом:
1. Поступление сырья к поверхности катализатора (внешняя диффузия)
2. Движение сырья в поры катализатора (внутренняя диффузия)
3. Хемосорбция на активных центрах катализатора
4. Химические реакции на поверхности катализатора
5. Десорбция продуктов крекинга и непрореагировавшего сырья с поверхности и диффузия из пор катализатора
6. Удаление продуктов крекинга и неразложившегося сырья из зоны реакции.
В зависимости от режима процесса, качества сырья и степени дисперсности катализатора, роль диффузионных и адсорбционных процессов может быть больше или меньше. Так установлено, что при нормальном режиме реактора каталитического крекинга с кипящим слоем порошкообразного катализатора при температурах от 480 до 535°С решающее значение имеют адсорбция и химические реакции на поверхности катализатора. При крекинге на крупногранулированном катализаторе скорость реакции тормозится диффузией молекул сырья к внутренней поверхности катализатора. Глубина превращения сырья возрастает, если увеличивается время контакта его с катализатором. Это условие определяется величиной объемной скорости подачи сырья.
Объемной скоростью подачи сырья называется отношение расхода сырья к объему загруженного в реактор катализатора.
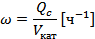
Величина обратная – это время контакта сырья с катализатором.

Закоксовывание и регенерация катализатора каталитического крекинга.
По мере подачи сырья, активность катализатора падает, так как поверхность его покрывается слоем смолисто-коксовых отложений. Катализатор приобретает интенсивно-темную окраску уже при поступлении первых порций сырья. Условно эти смолисто-коксовые отложения называют коксом, хотя элементарный анализ показывает, что содержание водорода в них довольно значительно (от 5 до 7% массовых, а может достигать и 10%). Источником образования кокса на катализаторе являются в первую очередь смолисто-асфальтеновые вещества, содержащиеся в сырье.
Так, например, в производственных условиях при переработке легкий керосиногазойлевых фракций, выход кокса составляет от 2-3% до 4-5% на сырье, а при крекинге тяжелых вакуумных газойлей – до 5-6% массовых, однако, большую роль играет и углеводородный состав сырья. Максимальные выходы кокса получаются при наличии ароматических углеводородов би- и трициклического строения. Известна склонность к коксообразованию сырья вторичного происхождения, например, газойлей коксования, содержащих ароматические углеводороды с непредельными боковыми цепями.
Длительность пребывания катализатора в зоне реакции, то есть, продолжительность работы катализатора между двумя периодами регенерации составляет на современных промышленных установках от 2 до 30 минут. Естесственно, что чем меньше продолжительность работы катализатора, тем выше его средняя активность за этот период. Регенерация катализатора обычно значительно сложнее, чем проведение самого крекинга.
Сущность регенерации заключается в сгорании коксовых отложений при их контактировании с кислородом воздуха. В результате такого контакта происходит значительное выделение тепла (от 6000 до 7500 ккал/кг кокса), которое необходимо отводить из зоны регенерации, чтобы не перегреть всю массу катализатора. При этом продолжительность регенерации не должна быть очень большой, чтобы регенератор был приемлемых размеров.
Исследование кинетики регенерации позволило определить пути интенсификации этого процесса в промышленных условиях. Было показано, что в области умеренных температур (450-500°С) регенерация протекает в кинетической области, то есть интенсивность её определяется скоростью реакции окисления. Энергия активации процесса регенерации в кинетической области составляет от 31 до 35 ккал/моль. С повышением температуры до 500-550°С процесс переходит во внешнюю или внутреннюю диффузионную область.
Варианты промышленных процессов каталитического крекинга.
В настоящее время имеется много схем и промышленных процессов каталитического крекинга, различающихся технологическим и аппаратурным оформлением:
1. Процесс со стационарным слоем катализатора.
2. Процесс с подвижным гранулированным или сферическим катализатором.
3. Крекинг с пылевидным или микросферическим движущимся катализатором.
В этом варианте крекинга в аппарате образуется псевдокипящий слой катализатора. Установка работает непрерывно благодаря непрерывной циркуляции катализатора. Транспорт катализатора осуществляется по принципу газлифта, что значительно упрощает установку. Применение пылевидного катализатора, образующего кипящий слой, дает ряд особых преимуществ. Принцип кипящего слоя твердого измельченного материала в настоящее время широко применяется во всех новых областях химической технологии.
Дата добавления: 2015-08-02; просмотров: 334 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Катализаторы каталитического крекинга | | | Режимы работы установок |