Ориентационное взаимодействие
Основной причиной, определяющей образование химической связи является стремление системы, состоящей из отдельных атомов к понижению полной энергии. | Ковалентной называется связь, которая образуется между двумя атомами за счет одной или нескольких общих электронных пар, одновременно принадлежащих им обоим. | История развития представлений об образовании химической связи | Метод валентных связей | Гибридизация – это прием построения одинаковых по энергии и форме гибридных валентных орбиталей путем линейной комбинации АО в методе валентных связей | Sp-Гибридизованное состояние свойственно атому, если сумма числа связанных с ним атомов и числа его неподеленных электронных пар равна 2 | Электронов при этом антипараллельны:ывающую МО. Спина мума энергии, принципом Паули и правилом Хунда. Так, два электрона молекВодородная связь | Решение типовых задач | Задачи для самостоятельного решения |
Полярные молекулы, в которых центры тяжести положительного и отрицательного зарядов не совпадают, т.е. молекулы, дипольный момент которых отличен от нуля, например HCl, H2O, NH3, ориентируются таким образом, чтобы рядом находились концы с противоположными зарядами (но не так сильно и не так жестко ориентированы, как при водородной связи). Между ними возникает притяжение. Это диполь-дипольное взаимодействие постоянных диполей.
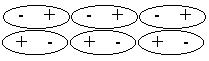
Диполь-дипольное взаимодействие проявляется в полярных жидкостях (вода, фтороводород).
Дата добавления: 2015-08-10; просмотров: 97 | Нарушение авторских прав
mybiblioteka.su - 2015-2024 год. (0.006 сек.)

