
|
Читайте также: |
Лабораторная работа. Коррозия железа в контакте с углеродом в растворе NaCl.
Цель работы:
изучение условий возникновения электрохимической коррозии железа, находящегося в контакте с углеродом, влияние концентрации дополнительного окислителя на скорость коррозии.
Теоретическая часть
Коррозия – это необратимое самопроизвольное разрушение металла в результате его физико-химического взаимодействия с окружающей средой.
По механизму протекания различают химическую и электрохимическую коррозию.
Химическая коррозия металла представляет собой гетерогенную окислительно-восстановительную реакцию и наблюдается в средах, не проводящих электрический ток, например, при прямом взаимодействии металла с сухим газом (окислителем) при высокой температуре или в среде агрессивных жидких неэлектролитов.
Электрохимическая коррозия характерна для сред, имеющих ионную проводимость, и представляет собой гетерогенную окислительно-восстановительную реакцию, протекающую по электрохимическому механизму. Электрохимическая коррозия может протекать: 1) в водных растворах солей, кислот, щелочей, в морской воде; 2) в атмосфере влажного газа; 3) в почве.
При электрохимической коррозии на энергетически неоднородной поверхности металла или сплава возникает множество локальных микрогальванических элементов, в которых катодные и анодные участки находятся в непосредственном контакте, то есть накоротко замкнуты. На участках с более отрицательным потенциалом (анодные участки) идет анодное растворение металла, а на участках с более положительным потенциалом (катодные участки) - катодное восстановление окислителя Ох.
На анодных участках: М → Мn+ + nе
На катодных участках: Ox + nе→ Red
Коррозия металла термодинамически возможна при условии, что потенциал окислителя положительнее потенциала металла.
 , где
, где
ЕРOx/Red- равновесный потенциал окислителя в данной среде,
ЕРMn+/M - равновесный потенциал металла в данной среде.
Окислителями при электрохимической коррозии чаще всего являются молекулы кислорода воздуха и ионы водорода из среды. При коррозии с участием кислорода, называемой коррозией с поглощением кислорода, или коррозией с кислородной деполяризацией, на катодных участках протекает процесс:
O2 + 4H+ + 4  → 2H2O при pH < 7
→ 2H2O при pH < 7
O2 + 2H2O + 4  → 4OH- при pH ³ 7.
→ 4OH- при pH ³ 7.
Равновесный потенциал окислителя О2 при 298К описывается уравнением:
 = 1,227 + 0,0147 lg
= 1,227 + 0,0147 lg  – 0,059рН.
– 0,059рН.
При коррозии с участием ионов водорода, называемой коррозией с выделением водорода или коррозией с водородной деполяризацией на катодных участках протекает процесс:
2H+ + 2  → H2 при pH < 7
→ H2 при pH < 7
2H2O + 2  → H2 + 2OH– при pH ³ 7.
→ H2 + 2OH– при pH ³ 7.
Равновесный потенциал системы Н+/Н2 при 298К описывается уравнением:
 = – 0,059рН - 0,0295 lg
= – 0,059рН - 0,0295 lg 
Графически зависимость потенциалов водородного и кислородного электродов от рН приведена на рисунке 1.
 |
Разные металлы корродируют по-разному, в зависимости от их стандартного потенциала и рН среды:
а) если потенциал металла положительнее потенциала кислородного электрода в данной среде (область 3 рис.1), то коррозия металла невозможна. Например, золото, платина не могут корродировать ни с поглощением О2, ни с выделением Н2, так как Е ок <  ;
;
б) если потенциал металла положительнее потенциала водородного электрода и отрицательнее потенциала кислородного электрода в данной среде (область 2), то коррозия возможна с поглощением кислорода и невозможна с выделением водорода, например:
 и
и  ;
;
в) если потенциал металла отрицательнее потенциала водородного электрода, то возможна коррозия как с поглощением кислорода, так и с выделением водорода (область 1). Например, щелочные, щелочно-земельные металлы, магний, алюминий, цинк и др.
Сравнение равновесных потенциалов окислителя и восстановителя позволяет установить возможность коррозионного процесса, но не дает информации о его скорости. Скорость коррозии можно характеризовать плотностью коррозионного тока iкор.

Рисунок 2. Коррозионная диаграмма для коррозии с поглощением кислорода
Если скорость коррозии определяется лимитирующей стадией катодного восстановления кислорода, то она ограничена скоростью диффузии растворенного кислорода к поверхности металла (рис.2)., при этом коррозионный ток iкор равен предельной плотности тока idО2 восстановления кислорода:
id =  , где
, где
 - коэффициент диффузии кислорода;
- коэффициент диффузии кислорода; 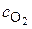 - концентрация кислорода в растворе; d -
- концентрация кислорода в растворе; d -
толщина диффузионного слоя. iкор возрастает при перемешивании раствора и увеличении концентрации растворенного кислорода и имеет экстремальную зависимость от температуры.
Если лимитирующей катодной стадией коррозии является выделение водорода (рис.3), то скорость коррозии определяется скоростью восстановления водорода. На рис.3 iкор зависит вравной мере от катодного и анодного процессов и возрастает с увеличением температуры и концентрации ионов водорода. При работе микрогальванических коррозионных элементов потенциал анодного процесса смещается в более положительную сторону, а катодного - в более отрицательную (как в гальваническом элементе). При некотором токе iкор кривые пересекаются. При этом на поверхности металла устанавливается стационарный потенциал Е с, или потенциал коррозии Е кор. (Ток анодного растворения металла равен току катодного восстановления окислителя. Омическое падение потенциала практически равно нулю, так как анодные и катодные участки непосредственно контактируют друг с другом.).
На скорость коррозии влияет также природа материала катодных участков. Такие примеси, как платина, кобальт, никель, палладий, катализируют выделение водорода, поэтому скорость катодного процесса на них будет выше, а поляризация меньше, чем на чистом М (i ’ – на рис.3). Другие металлы(например, ртуть, свинец, кадмий), напротив, увеличивают перенапряжение водорода (поляризация катодной кривой увеличится i ” – на рис.3).

Рисунок 3. Коррозионная диаграмма для коррозии с выделением водорода.
Скорость коррозии может лимитироваться и анодной реакцией, например, при коррозии металлов, способных переходить в пассивное состояние (хром, никель, алюминий, железо и другие) после контакта с окислителем. Пассивность металла – это состояние повышенной коррозионной стойкости, вызванное торможением анодной реакции в результате образования на поверхности металла оксидных, гидроксидных или иных защитных слоёв. Так, например, железо и стали пассивируют в основных средах при рН 9-12 в присутствии растворенного кислорода. Также железо переходит в пассивное состояние в концентрированных кислотах H2SO4 и HNO3.Однако наличие ионов Cl- препятствует образованию пассивных пленок на железе и многих других металлах, ионы Cl- являются активаторами коррозии.
Вопросы и задания для самоподготовки.
2.1.Что называют коррозией металлов?
2.2. В чём отличие электрохимической коррозии от химической?
2.3. Каковы причины возникновения коррозионных микрогальванических элементов?
2.4. Как определить термодинамическую возможность протекания коррозии металла с выделением водорода?
2.5. Как определить термодинамическую возможность протекания коррозии металла с поглощением кислорода?
2.6. Как можно замедлить скорость коррозии с поглощением кислорода?
2.7. Какие факторы влияют на скорость коррозии с выделением водорода?
2.8. Какое состояние металла называют пассивным?
2.9. Объясните, почему в атмосферных условиях медь корродирует, а золото нет?
2.10. Объясните, почему в стальных цистернах можно перевозить концентрированные азотную и серную кислоты, и нельзя перевозить соляную кислоту.
Дата добавления: 2015-07-11; просмотров: 156 | Нарушение авторских прав