
Читайте также:
|
HCl- сильная кислота;
NaOH- сильное основание.
1. При вычислении значение pH в растворах сильных кислот и оснований, являющихся сильными электролитами, концентрацию ионов Н+ или ОН- принимают практически равной общей концетрации кислот или оснований.
Тогда значение рН в исходном растворе кислоты определяется

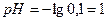
2. Концентрация остаточной кислоты, а, следовательно, и концентрацию ионов водорода в промежуточных точках титрования (до точки эквивалентности) рассчитывается по формуле:
 =
=  ;
; 
50%:  =
= 

90%:  =
= 

99%:  =
= 

99,9%:  =
= 
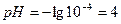
2. В точке эквивалентности.
 =
=  =10-7
=10-7

3. После точки эквивалентности.
Теперь проводят расчет концентрации избытка реагента (щелочи):
 =
=  ;
;  ;
; 
100,1%:  =
= 


101%:  =
= 
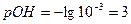

110%:  =
= 


На основе полученных данных строим кривую титрования (рис. 1)
Дата добавления: 2015-07-11; просмотров: 62 | Нарушение авторских прав