
Читайте также:
|
При переработке титановой губки (крицы и гарниссажной части) в первую очередь отделяют более качественный металл от менее качественного. При разделке блока губки от кричной (центральной части блока) отделяют низ и верх блока. Благодаря такому методу сортировки удается получить часть металла высших сортов, в которых содержание примесей меньше, чем в среднем по блоку.
Кроме разделения блока губки на соответствующие части, качество улучшают с помощью рассева губки после дробления по фракциям крупности. В самые мелкие фракции губки (менее 2 мм) попадает наиболее хрупкий металл.
В технологическую схему переработки блоков губчатого титана в товарную продукцию входят следующие основные операции:
1) подрезка гарниссажной части губки в реакторах;
2) выемка губки из реторты;
3) очистка блока губки от поверхностных пленок и загрязнений;
4) разрушение блоков губки на куски с доведением их крупности до требуемого размера товарной продукции;
5) рассев с выделением товарных фракций;
6) сортировка товарных фракций с извлечением некондиционных кусков, обогащенных примесями;
7) усреднение товарного губчатого титана;
8) пробоотбор;
9) комплектация товарной партии губчатого титана, распределение губки одной крупности и одного химического состава по упаковочным местам и затаривание.
Перед извлечением блока губки из реактора освобождают его проходное сечение от гарниссажной губки, для чего используют отбойные молотки или специализированные механизмы.
Блоки губки из реторт извлекают с помощью выталкивающих прессов (рис), вибровстряхивающих машин либо механических захватов.

|
Рис. 76. Пресс для выталкивания блоков губки из реторт:
1- гидроцилиндр; 2 - шток; 3 - блок губки; 4 - гарниссажная губка; 5 -
реторта; 6 -ложное днище; 7 - опорное кольцо; 8 - самоустанавливающаяся
пята; 9- подвижной люнет; 10 - приемная платформа; 11 - регулируемые опоры
 Разделка блока проводится с помощью различных механизмов. На рис. представлены прессножницы.
Разделка блока проводится с помощью различных механизмов. На рис. представлены прессножницы.

Рис. 77. Прессножницы для разрушения блоков губчатого титана: 1 - станина; 2 -рама с поперечиной; 3 - клиновидный нож; 4 -режущая кромка; 5 - блок губки; 6 - подвижный стол; 7 - плунжерный привод рамы; 8 - гидроцилиндры; 9- двусторонний клапан
Эти прессы целесообразно использовать для получения кусков губки
крупностью не менее 300 мм. Кусковый материал крупностью менее 300 мм измельчают на дробилках различных конструкций. Наиболее производительно измельчение в дробилках ударного действия. В щековых и конусных дробилках может быть достигнута большая степень измельчения,
Дробленую губку рассеивают на барабанных либо вибрационных грохотах для сортировки по фракциям
3.2.7. Плавка титана и его сплавов
Высокая реакционная способность, склонность к активному химическому взаимодействию с кислородом, азотом, углеродом и другими элементами не позволяют плавить титан и его сплавы в обычных металлургических печах. Плавку титана необходимо производить в условиях, предохраняющих жидкий металл от насыщения газами и другими вредными примесями. Технически чистый титан имеет сравнительно низкую прочность, поэтому в промышленности используют главным образом сплавы титана.
Высокая температура плавления титана (~ 1660 °С) в сочетании с высокой химической активностью создает большие трудности при плавке и литье сплавов на основе титана. Чтобы титан не стал хрупким в результате загрязнения газами, плавку и литье проводят в высоком вакууме или в атмосфере инертного газа высокой чистоты, а также не допускают соприкосновения металла с огнеупорными материалами.
В настоящее время разработано несколько методов получения титана, предотвращающих загрязнение металла газами или огнеупорными материалами:
1) вакуумная дуговая плавка;
2) плавка в печи с гарниссажем;
3) плавка в электрошлаковой печи;
4) плазменно - дуговая плавка;
5) индукционная плавка в графитовом тигле.
6) электронно - лучевая плавка.
Для всех видов плавок, за исключением индукционной, при плавлении титана применяют для формирования слитка медный водоохлаждаемый кристаллизатор, а при гарниссажной плавке - также графитовый тигель.
В электрошлаковой плавке источником нагрева служит джоулево тепло, выделяющееся при прохождении тока через слой флюса (фторида кальция), который является элементом сопротивления. Процесс осуществляется по схеме расходуемого электрода. При этой плавке параметры плавлении легко регулируются, поверхность слитков получается такой, что их можно использовать для дальнейших переделов без обточки. Кроме того, можно получать слитки плоского и квадратного сечения, что очень удобно для прокатки.
Способ плазменно-дуговой плавки позволяет переплавить сыпучую шихту с добавкой любого количества отходов. Источником тепла в этом процессе служит поток ионизированного газа-плазмы, подаваемого в зону плавки специальными устройствами - плазмотронами. При плазменной плавке, которая может осуществляться также и по схеме расходуемого электрода, повышается безопасность процесса, поверхность слитков лучше, чем при дуговой плавке.
Способ индукционной плавки предусматривает использование главным образом графитового тигля, при этом весь переплавляемый металл находится в расплавленном виде в отличие, например, от вакуумно-дуговой плавки, когда формирование слитка из жидкой ванны.

Рис. 19. Схема вакуумно-дуговой печи с расходуемым электродом:
1 - расходуемый электрод; 2 - охлаждаемый водой кристаллизатор; 3 - слиток титана; 4 - расплавленный металл; 5 - медный охлаждаемый поддон; 6 - вакуумная камера; 7 – токоподвод
Выплавку слитков первого и второго переплавов производят и однотипных печах. Схема вакуумной дуговой печи приведена на рис. 19, Основные узлы печи: изложница, поддон, электрододержатель, рабочая камера, вакуумная система.
Изложница - самая важная часть печи. В ней происходит горение дуги, плавление электрода, кристаллизация слитка. Изложница состоит из медного кристаллизатора, обычно цилиндрической формы, и корпуса, изготовляемого из коррозионностойкой стали. При работе печи в кольцевой зазор между кристаллизатором и корпусом полается вода под давлением для охлаждения кристалл и затора. Высокая теплопроводность и пластичность меди обеспечивает длительную работу кристаллизатора в условиях термических напряжений, возникающих при воздействии жидкого металла и излучения дуги. На корпус изложницы наматывают соленоид, который создаст внутри кристаллизатора продольное магнитное поле. При взаимодействии электрической дуги с магнитным полем оно стабилизирует горение дуги и вращает ванну жидкого металла, улучшая условия перемешивания жидкой ванны.
Другой важный узел - поддон. Он закрывает кристаллизатор снизу и в начальный период плавки испытывает большие тепловые нагрузки. Поддон изготавливают из меди и также охлаждают водой, подаваемой под давлением.
Электрододержатель предназначен для вертикального перемещения расходуемого электрода в печи и подачи напряжения на дугу. Его обычно изготавливают из стали. Он представляет собой две коаксиально расположенные трубы, но во внутреннюю подается вода для охлаждения.Электрододержатель вводят в рабочее пространство через кольцевое уплотнение. Снизу к наружной трубе приварен хвостовик с резьбой. На хвостовик навинчивают титановый отрок, который служит для крепления (припарки) расходуемого электрода.
Рабочая камера предназначена для размещения части расходуемого электрода, который обычно длиннее кристаллизатора, и для соединения кристаллизатора с вакуумной системой. В верхней части камеры расположены смотровые окна, через которые при помощи перископов ведут визуальное наблюдение за ходом плавки. Камеру изготавливают из коррозионностойкой стали, она испытывает относительно небольшие тепловые нагрузки,
Вакуумная система состоит из вакуумных насосов, вакуумпроводов, запорной арматуры и приборов контроля. Система должна обеспечивать быструю откачку воздуха из печи перед планкой до давления 13,3 Па и поддержание во время плавки давления < 26,6 Па. Для откачки используют один или несколько механических форвакуумных насосов типа ВН-6Г и механических бустерпых насосов типа 2ДВН-150О или 2ДВН-ЗООО.
Плавление металла происходит под действием тепла, выделяемого электрической дугой, которая горит между расходуемым электродом и поверхностью ванны жидкого металла. Для планки титана используют постоянный ток: отрицательным полюсом является расходуемый электрод, положительным - наплавляемый слиток. В качестве источников питания используют машинные генераторы или вентильные кремниевые выпрямители. В современных промышленных печах используют силу тока до 37,5 кА при напряжении 30-80 В.
Плавление слитков происходит следующим образом. Расходуемый электрод помещают в печь и сваривают с огарком. Затем, подняв электрод, зажигают дугу между нижним торцом электрода и поддоном. При выплавке крупных слитков второю переплава на поддон обычно кладут темплет из того же сплава для защиты поддона от прямого воздействия дуги. Конец электрода разогревается дугой до температуры, превышающей температуру плавления, на торце образуются капли жидкого металла. Когда масса капли превысит силы поверхностного натяжения, капля отрывается и падает на поддон. Постепенно электрод подают вниз, а слиток нарастает вверх, при этом в верхней части слитка образуется ванна жидкого металла. Таким образом, одновременно идут плавление и кристаллизация слитка.

Рис. Вид расплавного тигля и верхнего слитка титана
Для получения сплавов титана с алюминием, марганцем, ванадием, хромом и другими металлами легирующие добавки примешивают к губке, поступающей на изготовление электрода для первой плавки.
Продукция изделий из титана и его сплавов.

Титановое литье

Титановое литье

Титановые изделия

Рис. Виды титановой продукции
3.3. Производство меди
3.3.1. Свойства меди и области потребления
Медь является самым древним металлом, значение которого и в настоящее время трудно переоценить.
Медь – мягкий, вязкий и ковкий металл красного цвета. Он легко прокатывается в тонкие листы и проволоку. Широкое применение меди связано с хорошей электропроводностью и теплопроводностью, высокой пластичностью и способностью образовывать технологичные сплавы, которые отлично обрабатываются и обладают хорошими механическими свойствами.

Рис. Медь
Температура плавления меди 1083 °С, кипения 2360 °С. Предел прочности чистой меди не очень высок и составляет 220 МПа (22 кгс/мм2). Плотность меди 8,93 г/см3, а твердость почти в 2 раза меньше, чем у железа.
При обычной температуре сухой воздух и влага в отдельности не действуют на медь, но во влажном воздухе, содержащем СО2, медь окисляется и покрывается зеленой пленкой основного карбоната (CuCO3* Cu(OH)2), являющегося ядовитым веществом.
В растворах кислот, как соляная и серная, в отсутствие окислителя медь не растворяется. В азотной, горячей концентрированной серной кислоте медь растворяется легко. В присутствии кислорода и при нагреве медь хорошо растворяется в аммиаке.
При температуре красного каления медь окисляется с образованием Cu2 O, CuO.
C серой медь образует два сульфида: сернистую (СuS) и полусернистую (Cu2S) медь.
Медь способна сплавляться со многими металлами, образуя многочисленные сплавы.
Основными потребителями меди и ее соединений являются:
1) Электротехника и электроника (провода, кабели, обмотки электродвигателей, токоподводящие шины, детали радиоэлектронных приборов, фольга для печатных схем и др.);
2) Машиностроение (теплообменники, оросительные установки и др.);
3) Транспорт (детали и узлы железнодорожных вагонов, автомобилей, самолетов, морских и речных судов, тракторов и т.д.);
4) Строительные материалы (кровельные листы, детали декоративных
5) архитектурных украшений);
6) химическая промышленность (производство солей, красок, катализаторов);
7) Изделия и приборы бытового назначения (детали часов, посуда, скобяныеизделия, детали холодильников, стиральных машин и бытовых электроприборов, декоративные изделия и украшения и др.);
8) сельское хозяйства (ядохимикаты).
3.3.2 Медные руды и схема их переработки
В настоящее время главнейшим источником для получения меди (~ 80 % мировой добычи) служат сульфидные руды, содержащие чаще всего халькопирит (CuFeS2), называемый медным колчеданом, или другие сернистые минералы меди, например, халькозин (CuS) и др. В этих рудах обычно находится много пирита (FeS2) и сульфидов цинка, свинца, никеля, а нередко серебро и золото.

Рис. 1. Минерал куприт

Халькопирит

Рис. 2. Минерал малахит

Рис. 3. Самородная медь

Рис.4. Малахит

Рис. 5.Халькозин

Рис. 6. Куприт
Другим источником для получения меди являются окисленные медные руды, содержащие медь в виде куприта (Cu2O) или азурита (2СuСО3*Сu (ОН)2). Встречаются также смешанные сульфидно-окисленные медные руды.
Содержание меди в комплексных рудах незначительно (часто 1-2 %), перед их переработкой почти всегда подвергают обогащению, которое позволяет выделить из руды отдельно медный концентрат, содержащий 11-35 % Сu, и цинковый или пиритный концентрат.
Для получения меди из руд можно использовать пирометаллургические способы (плавка на штейн, восстановительная плавка) и гидрометаллургические способы, например, выщелачиванием серной кислотой.
Примерный состав медного концентрата, %: Cu-13,5; Zn-0,5; Fe- 36,5; S- 39?0; SiO2 – 2,7; Al2O3- 3,4; CaO- 0,5.
Рассмотрим один из наибольшее распространенных способов извлечения меди из сульфидных концентратов - плавку на штейн (рис. 7).

Рис. 7. Упрощенная схема получения меди из сульфидных руд пирометаллургическим способом
3.3.3. Получение медных штейнов из концентратов
Цель плавки на штейн - отделение сернистых соединений меди и железа от содержащихся в руде примесей, присутствующих в ней в виде окисленных соединений. Процесс осуществляется при высокой температуре 1550оС, что приводит к плавлению материалов и образованию жидкотекучих штейна и шлака.
По мере нагревания шихты начинаются реакции частичного восстановления высших окислов железа и меди, окисления серы и шлакообразования. Например,


Сульфид меди расплавляясь формирует штейн.
Штейн в застывшем виде - это сплав сульфидов, главным образом меди и железа (обычно 80 - 90 %) и сульфидов цинка, свинца, никеля. Они хорошо растворяют в себе золото и серебро, и, поэтому, почти полностью концентрируются в штейне.
Одним из способов переработки медных концентратов является плавка в отражательных печах с получением штейна, шлака и газов. Отражательные печи (рис. 8) обычно бывают длиной 35 - 40, шириной 7 - 10 и высотой 3,5 - 4,5 м. Стены и под выкладывают из динасового или магнезитового кирпича.
Отражательные печи отапливают мазутом, угольной пылью или газом, вдувая топливо форсунками (4 - 10 шт.) (5) через окна, имеющиеся в торце печи. Максимальная температура в головной части печи 1550 °С, в хвостовой части обычно 1250 - 1300 °С. Шихту в эти печи загружают через отверстия в своде (1), расположенные вдоль печи у боковых стенок. При загрузке шихта ложится откосами вдоль стен, предохраняя кладку от прямого воздействия шлаков и газов.



Рис. 8. Отражательная печь для плавки медных концентратов:
1 - загрузочные отверстия; 2 - окно для слива шлака; 3 - дымоход; 4 - шпуровые отверстия для выпуска штейна; 5 — отверстия для топливных форсунок
Штейн, имеющий плотность ~ 5 г/см3, собирается на поду печи, шлак образует второй верхний жидкий слой (плотность ~ 3,5 г/см3); его выпускают по мере накопления через шлаковое окно (2), расположенное в хвостовой части печи. Отверстия для выпуска штейна (обычно два) (4) находятся в одной из боковых стенок печи. Выпуск штейна производят по мере его образования и потребности в нем последующего конвертерного передела.
Штейны содержат 23 -28 % S, 16 - 60 % Си и 50 - 15 % Fe. Состав шлаков изменяется в широких пределах, но главными его составляющими всегда являются кремнезем (45 - 30 %) и закись железа (25 - 45 %).
3.3.4. Переработка медного штейна
Переработка медного штейна осуществляется методом конвертирования. Основная цель процесса – получение черновой меди за счет окисления железа и серы и некоторых сопутствующих компонентов.
Переработка штейна протекает в два периода. В конвертер загружают кусковой кварц, заливают расплавленный штейн и продувают его воздухом. Воздух, энергично перемешивая штейн, окисляет сульфиды меди и железа:
2 FeS + 3 O2 = 2 FeO + 2 SO2
2 CuS + 3 O2 = 2 Cu2O + 2 SO2
при этом закись меди, благодаря обменному взаимодействию, вновь превращается в сульфид:

Поэтому в первом периоде идет практически окисление только железа, а закись железа шлакуется кварцем:
2 FeO + SiO2 = 2 FeO* SiO2
Получили распространение цилиндрические бочкообразные конвертеры (рис. 9). Наружный диаметр конвертера обычно 2,3 - 4 м, длина 4,3 -10 м. Воздух в конвертер подается через ряд фурм, расположенных по образующей цилиндра. Цилиндр опирается двумя прочными бандажами на четыре пары роликов, что позволяет поворачивать его на необходимый угол для заливки штейна в горловину и выпивки продуктов плавки. Внутри конвертер футерован магнезитовым и хромомагнезитовым кирпичем.

|
Рис. 9. Конвертер для получения черновой меди
1- Горловина; 2 – окно для загрузки флюсов; 3 – воздушный коллектор; 4- фурмы

Здесь производят медь
Образующийся шлак периодически сливают и в конвертер добавляют свежие порции медного штейна и кускового кварца. Температура процесса от 1200 до 1280 о С.
Первый период заканчивается, когда в продуваемом штейне окислится сернистое железо. После этого тщательно удаляют шлак и продолжают продувку без добавки штейна и кварца. Воздух окисляет теперь только Cu2S, и образовавшаяся закись меди способствует появлению в конвертере металлической меди по реакции:
Cu2S + 2 Cu2O = 6 Cu + SO2
Второй период заканчивается, когда в конвертере весь штейн превращается в медь, на что обычно уходит 2 -3 ч. В конвертере и во втором периоде образуется небольшое количество богатого медью шлака, который остается в нем после выливания черновой меди и перерабатывается в следующем цикле. Конвертерные шлаки первого периода направляют для переработки в отражательные печи.
Конвертерные газы содержат 12 - 17 % SO2, и после очистки от пыли их используют для получения серной кислоты.
Черновую медь по окончании процесса, наклоняя конвертер, выпускают в ковш и разливают в изложницы. Полученную в конвертере медь называют черновой, т. е. еще не готовой медью, так как в ней содержится 1 - 2 % железа, цинка, никеля, мышьяка, сурьмы, кислорода, серы и других примесей; в ней также растворены благородные металлы, ранее находившиеся в штейне.
3.3.5. Рафинирование меди
3.3.5.1. Огневое рафинирование
Черновая медь всегда подвергается рафинированию для удаления из нее примесей, ухудшающих ее свойства, а также для извлечения из нее золота и серебра. В современной практике рафинирование проводят последовательно двумя принципиально различными методами: пирометаллургическим и электролитическим.
Огневое (пирометаллургическое) рафинирование меди проводят в отражательных печах. В отличие от отражательных печей для получения штейна эти печи меньших размеров (ширина 5 м, длина 12 - 15 м, глубина ванны 0,9 м).

|
Рис.10. Отражательная печь для рафинирования меди:
1 – столбчатый фундамент; 2 – подина; 3 – газоход; 4 –распорно-подвесной свод; 5 – горелка; 6 – рабочее окно с заслонкой; 7 – шлаковое окно; 8 – щелевая летка
Весь цикл огневого рафинирования состоит из операций: загрузки и расплавления, окисления примесей, удаления газов, раскисления меди и разливки; он занимает обычно 12 - 16 ч. Примеси в черновой меди окисляют воздухом, который вдувают через стальную трубку диаметром 20 - 40 мм, футерованную огнеупорами и погружаемую в расплавленную медь.
Медь после огневого рафинирования подают на разливочные машины для отливки анодов, квадратных плит с ушками, имеющими толщину 40 - 50 мм, длину и ширину - ~ 1 м. Указанные аноды направляют на электролитическое рафинирование. Анодная медь содержит 99,4 – 99,6 % меди, остальное примеси, в том числе золото, серебро, селен и теллур. В среднем в 1 т меди содержится 30 – 100 г золота и до 1000 г серебра. Такую медь обязательно подвергают рафинированию методом электролиза.
3.3.5.2. Электролитическое рафинирование меди
Анодная медь содержит 99,4 - 99,6 % Сu; остальное приходится на долю оставшихся после огневого рафинирования примесей, включая золото, серебро, селен и теллур. В среднем в 1 т анодной меди содержится 30 - 100 г золота и до 1000 г серебра.
Одним из методов очистки от примесей является электролитическое рафинирование, основанное на различии потенциалов выделения из растворов различных элементов.
Следовательно электролитическая ячейка состоит из катода, анода и электролита, рис. 11.
|
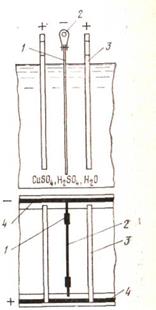
Рис. 11. Схема электролитического рафинирования меди: 1- катод; 2 – катодная штанга; 3 – анод; 4 – токоподводящие шины
Электролит – водный раствор сульфата меди (160 – 200 г/л) и серной кислоты (135 – 200 г/ л). Анод – литая черновая медь; катод – матрица – тонкие лист из электролитной меди
В черновой меди элементы подразделяются на элементы имеющие различный потенциал выделения по отношению к водороду:
1. Электроотрицательные – Fe, Ni, Co, Zn, Sn, Pb, которые практически полностью растворяются на аноде, могут попасть в раствор и выделиться на катоде совместно с медью, если их концентрация становится выше определенного предела. Для избежания их выделения необходимо не допускать повышение их концентрации выше определенного предела или предварительно от них очищаться другими методами;
2. Близкие потенциалы выделения к меди – As, Sb, Bi. Их переход в катодный металл наиболее вероятен. Для избежания их выделения электролит периодически выводится из цикла и подвергается регенерации;
3. Электроположительные - Au, Ag. В условиях электролиза не растворяются и остаются в анодном шламе.
4. Примеси химических соединений - Cu2S, Cu2Se, Cu2Te. Вследствие электрохимической нейтральности и малой растворимости в электролите переходят в шлам совместно с благородными металлами.
Механизм электролитического рафинирования меди включает следующие элементарные стадии:
1) электрохимическое растворение меди на аноде с отрывом электронов и образованием катиона:
Сu -2 е → Сu 2+;
2) перенос катиона через слой электролита к поверхности катода;
3) электрохимическое восстановление катиона меди на катоде:
Cu 2 + 2 e → Cu;
4) внедрение образовавшегося атома меди в кристаллическую решетку катода (рост катодного осадка).
Электролитическое рафинирование меди проводят в ваннах, наполненных раствором сернокислой меди, подкисленным серной кислотой. Размеры ванн зависят от размеров и числа электродов. В ваннах устанавливают до 45 катодов и 44 анода. Корпуса ванн изготовляют из бетона или дерева, стенки ванны внутри покрывают винипластом, свинцом или другим кислотоупорным материалом. Аноды соединяют с положительным полюсом источника постоянного тока (рис. 12).
Ионы меди из раствора восстанавливаются и плотными кристаллами оседают на катодных основах.


Рис. 12. Электролизная ванна для рафинирования меди:
1 — деревянный корпус ванны; 2 — аноды; 3 — катоды; 4 — отверстие для удаления шлака
Катоды, извлеченные из ванн, тщательно промывают водой, а затем их направляют для переплавки или производства сплавов в электрических или отражательных печах.

Сульфатная медь

В электролизном цехе (электролитическая ванна)
3.3.6. Медные сплавы
Наиболее распространенными и известными сплавами меди являются латуни и бронзы.
Латунями называют группу сплавов меди с цинком, получившую наиболее широкое применение в технике. В группу латуней входят томпак (90 % меди и более, остальное - цинк) и много других, не только двойных, но и более сложных сплавов. Механическая прочность латуней выше, чем меди, и они хорошо обрабатываются резанием. Латуни широко применяют в приборостроении, в общем и химическом машиностроении
Широко известны сплавы меди с оловом, называемые бронзами. Из бронзы еще в древности делали оружие и инструменты, сосуды и украшения, так как эти сплавы более прочны и коррозионностойки, чем медь. Благодаря отличным литейным качествам из этих сплавов в более позднее время стали отливать пушки и колокола. Малый коэффициент трения и устойчивость к износу делает их незаменимыми при изготовлении вкладышей подшипников, червяков и червячных колес, шестерен и других деталей ответственных и точных приборов.

Медь прокатная

Медные трубы

Прокатный медный стан

3.4. Металлургия алюминия
3.4.1. Общие сведения об алюминии
Алюминий - второй (после железа) металл современной техники. Один из легких конструкционных материалов, его плотность равная 2,7 г/см3, т. е. алюминии почти в 3 раза легче железа. Алюминий обладает хорошей электрической проводимостью (34 *104 Ом –1 *см -1), составляющая 57 % электрической проводимости меди. Температура плавления алюминия 660 °С, температура кипения ~ 2500 °С.
Кроме того, алюминий имеет высокую теплопроводность и теплоемкость, химически стоек против органических кислот и хорошо сопротивляется воздействию «холодной» азотной кислоты. При нагреве алюминий легко растворяется в разбавленных азотной и серной кислотах. Алюминий хорошо растворяется в щелочах с образованием алюминатов.Он очень быстро окисляется на воздухе, покрываясь тонкой пленкой окиси, которая, в отличие от окиси железа, не пропускает кислород в толщу металла. Однако присутствие даже небольших количеств магния, кальция, натрия, кремния и меди существенно снижает защитные свойства поверхностной пленки оксида алюминия.
Многие физические свойства алюминия существенно зависит от его чистоты. Так, чем чище алюминий, тем выше его температура плавления и электропроводность и ниже – плотностью Однако ряд свойств алюминия (прочность, обрабатываемость, литейные свойства и др.) можно значительно улучшить легирующими добавками магния, кремния, меди, цинка, марганца.
Алюминий обладает большой химической активностью по отношению к кислороду, галогенам, сере и углероду, что имеет большое практическое значение в металлургии.
Механические свойства алюминия невысоки. Предел прочности при разрыве составляет 90 -180 МПа (9 -18 кгс/мм2), твердость НВ(по Бринелю) составляет всего 20 - 40 единиц. Он очень пластичен, что позволяет прокатывать его в тонкие листы и фольгу. Однако чистый алюминий трудно обрабатывается резанием, а также имеет значительную линейную усадку (1,8 %).
Вследствие высокого сродства к кислороду алюминий восстанавливает оксиды многих металлов до металлического состояния. Это позволяет применять алюминий как восстановитель (алюмотермия)
Для улучшения этих свойств в алюминий вводят различные добавки.
Сочетание физических, механических и химических свойств алюминия определяет его широкое применение практически во всех областях техники, особенно в виде его сплавов с другими металлами.
Важнейшими потребителями алюминия и его сплавов являются авиационная и автомобильная промышленности; железнодорожный и водный транспорт, электроника, химическая промышленность, машиностроение, промышленное и гражданское строительство, производство предметов домашнего обихода.
В электротехнике алюминий успешно заменяет медь, особенно в производстве массивных проводников, например, в воздушных линиях, высоковольтных кабелях, шинах распределительных устройств, трансформаторах, и он более чем в три раза легче меди; при поперечном сечении, обеспечивающем одну и ту же проводимость, масса проводов из алюминия вдвое меньше медных.
Сверхчистый алюминий употребляют в производстве электрических конденсаторов и выпрямителей, действие которых основано на способности окисной пленки алюминия пропускать электрический ток только в одном направлении. Сверхчистый алюминий, очищенный зонной плавкой, применяется для синтеза полупроводниковых соединений, применяемых для производства полупроводниковых приборов.
Чистый алюминий используют в производстве разного рода зеркал отражателей. Алюминий высокой чистоты применяют для предохранения металлических поверхностей от действия атмосферной коррозии (плакирование, алюминиевая краска). Обладая относительно низким сечением поглощения нейтронов, алюминий применяется как конструкционный материал в ядерных реакторах.
В алюминиевых резервуарах большой емкости хранят и транспортируют жидкие газы (метан, кислород, водород и т. д.), азотную и уксусную кислоты, чистую воду, перекись водорода и пищевые масла. Алюминий широко применяют и оборудовании и аппаратах пищевой промышленности, для упаковки пищевых продуктов (в виде фольги), для производства разного рода бытовых изделии. Резко возросло потребление алюминия для отделки зданий, архитектурных, транспортных и спортивных сооружений.
В металлургии алюминий (помимо сплавов на его основе) - одна из самых распространённых легирующих добавок в сплавах на основе Сu, Mg, Ti, Ni, Zn и Fe. Применяют алюминий также для раскисления стали пред заливкой её в форму, как легирующую добавку в жароупорные стали, при термитной сварке, в процессах получения некоторых металлов методом алюминотермии. На основе алюминия методом порошковой металлургии создан САП (спечённый алюминиевый порошок), обладающий при температурах выше 300°С большой жаропрочностью.
Значительное количество алюминия расходуется на получение многочисленных сплавов (силумин- сплав алюминия с кремнием, сплавы АЛ7, АЛ19 – меди. АЛ8 и АЛ27 – магнием, дуралюмины –сплавы с медью, магнием и марганцем).
Силумины отличаются высокими литейными свойствами и хорошо поддаются сварке. Из силуминовых сплавов получают фасонные отливки любой конфигурации. Известны также подшипниковые алюминиевые сплавы на основе систем с железом, никелем, медью.
Алюминий используют в производстве взрывчатых веществ (аммонал, алюмотол). Широко применяют различные соединения алюминия.
Порошки плавленого оксида алюминия (корунда) используют в качестве исходного материала при изготовлении шлифовальных кругов, шкурки и других абразивных изделий. Из чистого оксида алюминия изготавливают жаропрочные тигли и трубы, огнеупоры, искусственные рубины, высококачественные зубные цементы.
Производство и потребление алюминия непрерывно растет, значительно опережая по темпам роста производство стали, меди, свинца, цинка.
Для развитых промышленных стран потребление алюминия по отдельным отраслям выражается следующими цифрами, % от общего потребления: транспорт – 35- 39; тара и упаковка – 27- 12; строительство – 19- 14; электротехника – 5 – 7; маштном\строение – 6- 12.
3.4.2. Сырье для получения алюминия
Алюминий — наиболее распространенный металл в земной коре (8,05 %, в пересчете на Al2O3 - ~ 15 %); в чистом виде он не встречается, зато минералов, содержащих алюминий, очень много, их больше 250. Наиболее распространены в природе соединения с кислородом
Наиболее распространенными, имеющих промышленное значение или перспективных в будущем являются следующие, табл. 1.
Таблица 1. Наиболее распространенные минералы алюминия
| Минерал | Формула | Al2O3, % |
| Корунд | Al2O3 | 100,0 |
| Диаспор,бемит | Al2O3*H2O | 85,0 |
| Гидраргилит | Al2O3* 3 H2O | 71,0 |
| Кианит | Al2O3* SiO2 | 63,0 |
| Каолинит | Al2O3 *2SiO2* 2 H2O | 39,5 |
| Алунит | K2SO4*Al2(SO)4*4Al (OH)2 | 37,0 |
| Нефелин | (Na,K)2O *Al2O3* 2SiO2 | 32,3 – 35,9 |



Корунд, нефелин, алунит

каолинит
Основным сырьем для получения алюминия служат бокситы.

|
Бокситы (Al2O3 *n H2O) - сложная горная порода, которая содержит алюминий в виде гидроокисей. Кроме того, в бокситах всегда присутствуют окиси и гидроокиси железа, кремнезем в виде кварца, каолинита, а также карбонат кальция, окись титана и др. Внешний вид и химический состав бокситов очень непостоянен. Качество бокситов определяется количеством окиси алюминия и содержанием кремнезема, вредной примеси, затрудняющей получение алюминия.

Рис. 1. Боксит
Химический состав бокситов изменяется в очень широких пределах, так содержание оксида алюминия (глинозема) колеблется от 35 до 60 %; оксида кремния (кремнезема) от десятых долей до 25 %, оксида железа от 2 до 40 %, оксида титана от следов до 11 %. По внешнему виду бокситы похожи на глину. Они могут иметь различные цвета от белого до темно –красного. Плотность в зависимости от их пористость колеблется от 1200 до 3500 кг/ м3. Важнейшими характеристиками, определяющими качество бокситов, является отношением содержания оксида алюминия к содержанию оксида кремния. Чем выше кремневый модуль, т.е. чем больше содержание оксида алюминия и меньше оксида кремния, тем выше качество боксита.
На Украине качественного глиноземсодержащего сырья весьма мало. Поэтому алюминиевая промышленность базируется на импортных, в основном Гвинейских бокситах.
Для получения алюминия недостаточно иметь только алюминиевую руду; требуется еще другой вид сырья - плавиковый шпат для получения криолита и других фтористых солей, необходимых в производстве алюминия.
Нужны также чистые углеродистые материалы для получения анодной массы и других электродных изделий, без которых невозможно электролитическое производство алюминия. Нельзя его осуществить и без большого расхода электрической энергии. Таким образом, современное производство алюминия складывается из четырех самостоятельных процессов:
производства глинозема,
получения криолита,
электродного производства
электролитического получения алюминия.
Часть электролитического алюминия подвергают дополнительному рафинированию.
На рис. 2 приведенная схема получения чистого алюминия: является типовой и лежит в основе практически всей мировой алюминиевой промышленности.

Рис.2. Принципиальная технологическая схема получения алюминия
3.4.3. Производство глинозема
Как видно из схемы на рис. 1, для производства алюминия сначала нужно получить чистую окись алюминия. Современная алюминиевая промышленность использует используют два способа переработки:
способ Байера;
способ спекания.
3.4.3.1. Получение глинозема по способу Байера
Способ Байера получил наиболее широкое распространение в мировой практике. Он был предложен в конце 19 столетия австрийским химиком К. Н. Байером, работавшим в России. По имени автора этот процесс был назван способом Байера.
Способ Байера относится к щелочным гидрохимическим процессам. В основе способа лежит обратимая химическая реакция

В условиях обработки (выщелачивания) исходной руды раствором едкого натра эта реакция идет вправо, т. е. алюминий переходит в раствор в форме алюмината натрия.
При разложении (декомпозиции) полученных растворов равновесие реакции сдвигается в обратную сторону и происходит гидролиз алюминатного раствора с образованием кристаллического осадка гидроксида алюминия.
В способе Байера технологический цикл по щелочи замкнут. Затраченная на выщелачивание щелочь освобождается при декомпозиции и возвращается в голову процесса на обработку новых порций руды.
Способ Байера обычно применяют для переработки высококачественных бокситов с относительно низким содержанием кремнезема. На рис. 3 приведена схема получения окиси алюминия по способу Байера. Согласно этой схеме исходный боксит дробят и затем измельчают в среде концентрированного оборотного раствора щелочи.
Боксит
Смешение ← NaOH
Обработка в автоклаве
2500С, 40 ат
Алюминат натрия + красный шлам
←Красный шлам Сгущение Выпаривание
→Щелочной алюминат
Декомпозиция
Охлаждение
Раствор едкого натрия +
Гидроокись алюминия
(Al(OH)3)
Затравка Фильтрация Возврат
Al(OH)3 NaOH
Гидроокись алюминия
Al(OH)3
Кальцинация
13000С
Al2O3
Рис. 3. Схема производства глинозема по способу Байера
Далее пульпу выщелачивают с целью перевода оксида алюминия в раствор.
Al2O3 * n H2O + 2 NaOH ↔ 2 NaAlO2 + (n + 1) H2O
Одновременно с природными гидроксидами алюминия со щелочью взаимодействуют свободный кремнезем и различные алюмосиликаты. Этот процесс идет вначале с образованием силиката натрия по реакции

Силикат натрия реагирует затем с алюминатом натрия с образованием нерастворимого в щелочных растворах натриевого гидроалюмосиликата:
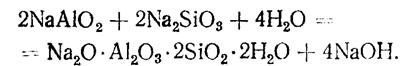
Образование больших количеств нерастворимого гидроалюмосиликата натрия при выщелачивании бокситов недопустимо, так как ведет к неизбежным потерям щелочи и к снижению извлечения в раствор алюминия. По этой причине бокситы с повышенным содержанием кремнезема перерабатывать способом Байера нецелесообразно.
Для выщелачивания бокситов и особенно бокситов, содержащих алюминий в форме моногидроксида, требуются температуры не ниже 180 -240 'С. Выщелачивание бокситов проводят в специальных аппаратах - автоклавах, работающих под давлением, рис. 4.
Вертикальный автоклав диаметром 1,6 – 2,5 м и высотой 13,5 -17,5 м, представляют собой стальные сосуды 1, работающие при давлениях до 3 МПа и температуре до 250 °С. Обогрев автоклавов может производиться острым паром, вдуваемым непосредственно в пульпу через барботер 7, или с помощью обогреваемых змеевиков.
Он снабжен трубой передавливания для разгрузки пульпы 2. Загружают пульпу в автоклав через штуцер в верхнем днище. Аппарат устанавливают на несущую конструкцию с помощью четырех опор 8, приваренных к корпусу.
Выщелачивание бокситов в автоклавах можно проводить как в периодическом, так и в непрерывном автоматизированном режимах.
При периодическом выщелачивании пульпу с начала до конца обрабатывают в одном автоклаве. Оно включает следующие операции: загрузку пульпы, нагрев ее до необходимой температуры, выщелачивание и разгрузку автоклава. Длительность процесса при этом составляет около 3 ч, в том числе на выщелачивание затрачивается 1,5 – 2 ч.
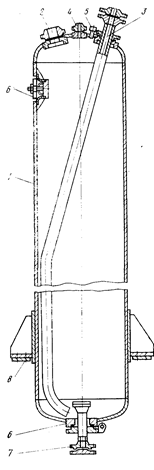
Рис .4. Автоклав для выщелачивания бокситов:
1 - корпус; 2 - загрузочный штуцер; 3 - труба передавливания (разгрузочная); 4 - штуцер сдувки; 5 - штуцер для подключения контрольно-измерительных приборов: 6 - люк; 7 - барботер; 8 - опоры
Периодическое выщелачивание в настоящее время потеряло свое практическое значение.
Непрерывный процесс осуществляется в автоматизированных автоклавных батареях (рис. 5), объединяющих в зависимости.от технологических требований по 6 - 10 автоклавов.
Бокситовая пульпа из мешалок 1 с помощью поршневого насоса 3 нагнетается в теплообменники 4, где нагревается сепараторным паром I ступени сепарации. Из теплообменника пульпа поступает в греющие реакционных автоклавов 6, в которых протекает и завершается процесс выщелачивания. Из последнего автоклава пульпа вводится в сепараторы I и 11 ступеней 7,8, где давление снижается до атмосферного (соответственно снижается и температура до 80 – 900 Савтоклавы 5 и далее передавливается последовательно через батарею
|
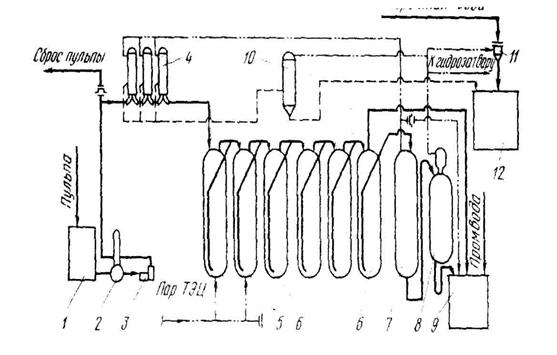
Рис. 5. Схема непрерывного выщелачивания бокситов в автоматизированной батарее:
1- мешалка; 2 - воздушный компенсатор; 3 - поршневой насос; 4 - теплообменник; 5 - греющие автоклавы; 6- реакционные автоклавы; 7 - сепаратор пульпы I ступени; 6 - сепаратор пульпы II ступени; 9 - мешалка разбавления; 10 -самоиспаритель конденсата; 11 - распределитель; 12 - бак с конденсатной водой
Вследствие резкого снижения давления пульпа в сепараторе I ступени вскипает, образовавшийся в нем пар направляют в подогреватели первичного нагрева 4 исходной пульпы. Низкотемпературный пар сепаратора второй ступени используют для подогрева воды, необходимой для промывки шлама.
Время пребывания пульпы в автоклавах составляет около 2 ч. Из сепаратора пульпа, состоящая из алюминатного раствора и красного шлама, поступает на разбавление в мешалку 9, а затем в отделение сгущения и промывки красного шлама. Сгущение пульпы проводят чаще всего в однокамерных сгустителях диаметром 30 - 40 м.
Выпущенный из сгустителей шлам подвергают многократной промывке по принципу противотока, что позволяет более полно отмыть его от остатков алюминатного раствора и получить промывные воды более высокой концентрации. Промытый красный шлам откачивают в хранилище. Выход шлама в зависимости от вида и качества перерабатываемого боксита составляет 20—50 % от исходной массы. Примерный состав красного шлама следующий, %: 12-15 А1203; 45-50 Fe2O3; 6 -11 SiO2.
На Николаевском глиноземном заводе внедрена новая технология высокотемпературного трубчатого выщелачивания, позволяющая повысить извлечение глинозема из боксита на 1,5%, повысить производительность на 140 тыс.т глинозема в год и снизить капитальные затраты на строительство на 10 – 15 %. Особенность процесса заключается в том, что выщелачивание трудновскрываемых бокситов проводят при температуре 270 0С и нагрев пульпы проводят глухим паром с использованием кожухотрубных теплообменников специальной конструкции, рассчитанных на высокое давление с площадью теплообмена F = 100 м2; и в перспективе 400 м2, работающих в режиме «глухого» нагрева.


Рис. Установка высокотемпературного выщелачивания на ООО НГЗ
Рис. Модель установки высокотемпературного выщелачивания
Алюминатный раствор после сгущения обрабатывают на фильтрах, работающих под давлением или под разрежением. Раствор после фильтрации должен содержать Fe2O3 не более 10 г / м3 и SiO2 не более 5 -6 г / м3. Температура раствора около 90 °С. Далее раствор подвергают декомпозиции (разложению).
Процесс декомпозиции, получивший название «выкручивание». основан на обратимой реакции:

Его цель - кристаллизация из раствора А1(ОН)3. Для того чтобы осуществить процесс разложения алюминатного раствора, т. е. сдвинуть равновесие реакции вправо, необходимо разбавить раствор, охладить его, ввести «затравку» (ранее полученные мелкие кристаллы гидроксида алюминия) и перемешивать пульпу в течение 50 - 90 ч, чтобы вырастить достаточно крупные кристаллы.
Выкручивание алюминатных растворов проводят в аппаратах, называемых декомпозерами рис. 6 и 7, с механическим или пневматическим (воздушным) перемешиванием в периодическом или непрерывном режимах
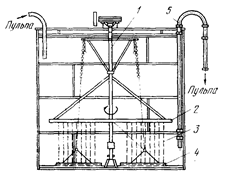
Рис. 6. Декомпозер смеханическим перемешиванием:
1 - вал; 2 - лопасть; 3 - цепь; 4 - волокуша; 5 - сифон
Декомпозер с механическим перемешиванием (рис. 6) представляет собой стальной бак высотой и диаметром по 8 м, внутри которого вращается цепная мешалка 3, состоящая из вала с лопастями и свободно подвешенных на них цепей с волокушами 4.
Декомпозеры с воздушным перемешиванием (рис. 7) являются наиболее совершенными и крупными аппаратами 1 вместимостью до 3000 м3. Для перемешивания пульпы, обеспечивающей хорошую циркуляцию затравки, служит циркуляционный аэролифт (пневмоподъемник) 2. Он состоит из двух концентрически установленных вертикальных труб. По внутренней трубе сверху в коническую часть декомпозера, где оседает кристаллизующийся гидроксид алюминия, подают сжатый воздух. Выходя из центральной трубы, воздух способствует образованию воздушно-пульповой взвеси, которая, обладает значительно меньшей плотностью, устремляется в кольцевой зазор аэролифта и, поднимаясь, сливается через верхний открытый конец наружной трубы.

|
Рис. 7. Схема декомпозера с воздушным перемешиванием:
1 - корпус; 2 - аэролифт для перемешивания; 3 - транспортный аэролифт;
4 - боковая барботажная трубка; 5 - водяные рубашки; 6 - люк; 7 - разгрузочный клапан; 8 - вытяжная труба
Кроме циркуляционного аэролифта в пневматическом декомпозере имеется транспортный аэролифт, с помощью которого осущечтвляется переток пульпы из одного декомпозера в другой.
После декомпозиции пульпа поступает в сгустители, где гидрооксид отделяют от раствора.
Полученный гидрооксид в гидросепараторах разделяют на фракции с размером частиц – 40- 100 мкм и мелкую фракцию (размером меньше 40 мкм), которую используют в качестве затравки при декомпозиции. Крупную фракцию промывают, фильтруют и направляют на кальцинацию.
Цель кальцинации – обезвоживание гидроксида алюминия по реакции:
2 Al(OH)3 → Al2O3 + 3 H2O
Это достигается сушкой и прокалкой гидроксида при температуре ~ 12000С. При этом получают негигроскопический α – глинозем.
На большинстве заводов кальцинацию глинозема осуществляют в трубчатых вращающихся печах длиной 35 – 110 м и диаметром 2,5 – 4,5 м Прокаленный глинозем охлаждают в трубчатых холодильниках длиной 25- 50 м и диаметром 2, 5 – 3,5 м. Конструктивная суть установки для кальцинации аналогична для спекания глиноземсодержащего сырья, рассматривается позже.

Рис. Печи прокалки глинозема


Рис. Глинозем металлургический; кристаллы гидроксида алюминия, мелкодисперсный глинозем
3.4.3.2. Получение глинозема способом спекания.
Способ применяют для получения глинозема из высококремнистых
(больше 6 - 8 % диоксида кремния) бокситов с кремниевым модулем менее 5 – 7. Способ пригоден также для переработки любого алюминиевого сырья.
Сущность способа заключается в получении твердых алюминатов натрия путем их спекания при высоких температурах (1250 - 1300 0С) и последующим выщелачивании спека.
Основные стадии этого процесса:
подготовка к спеканию;
спекание;
выщелачивание спека;
обескремнивание алюминатного раствора;
отделения алюминатного раствора от красного шлама;
карбонизация алюминатного раствора с получением гидроксида алюмния;
отделение гидрооксида алюминия от содового раствора;
кальцинации гидроксида алюминия.
При проведении процесса спекания глиноземсодержащего сырья кроме щелочного реагента, в качестве которого используют соду, в шихту добавляют известь, цель добавки которой заключается в связывании оксида кремния в малорастворимый в содовом растворе кальциевые силикаты по реакциям:
Al2O3 + Na2CO3 = 2 NaAlO2 + CO2
2 CaCO3 + SiO2 = 2 CaO* SiO2 + 2 CO2
Примерная схема спекания боксито – содово - известковой шихты, рис. 8.
Сода Боксит Известняк
ДРОБЛЕНИЕ ДРОБЛЕНИЕ
МОКРОЕ ИЗМЕЛЬЧЕНИЕ
Пульпа
СПЕКАНИЕ
Спек Газы
ДРОБЛЕНИЕ Вода
ВЫЩЕЛАЧИВАНИЕ
Алюминатный раствор Красный шлам
ОБЕСКРЕМНИВАНИЕ В отвал
Белый шлам КАРБОНИЗАЦИЯ
Гидратная пульпа
ОТДЕЛЕНИЕ И ПРОМЫВКА ГИДРОКСИДА АЛЮМИНИЯ
Маточный раствор и промводы Al(OH) 3
ВЫПАРИВАНИЕ КАЛЬЦИНАЦИЯ
Содовый раствор Глинозем
Рис. 8. Схема производства глинозема из бокситов по способу спекания
Спекание ведут в трубчатых вращающиеся печи, имеющие длину 80 -185 м и диаметр 2,5 - 5 м (рис. 9). Полученную пульпу подают в холодный конец печи, где она встречается с отходящими печными газами, имеющими температуру ~ 400 °С. В результате влага испаряется; высохшая шихта перемещается в горячую зону, в которой температура достигает 1250 - 13000С. По мере нагревания в шихте протекают ранее указанные реакции. Полученный в печи спек охлаждают, дробят и подвергают выщелачиванию, сущность которого заключается в воздействии на спек слабых растворов соды. В результате выщелачивания из спека в раствор переходит алюминат натрия (Na2O*Al2O3 или NaAlO2), а нерастворившаяся часть, называемая красным шламом, содержащий оксиды железа, кремния, кальция и частично алюминия отправляется в отвал.

Рис. 9. Трубчатая вращающаяся печь:
1 - труба; 2 - форсунка; 3 - разгрузочная головка; 4 - венцовая шестерня; 5 - опорные бандажи; 6 - загрузочная головка; 7 – редуктор
Несмотря на то, что основная масса кремния переходит в раствор в виде растворимого двукальциевого силиката, в раствор переходит немного кремния в виде гидросиликатов, в связи с чем раствор подвергают обескремниванию.
Обескремнивание алюминатного раствора осуществляют в батарее автоклавов длительной (около 2,5 ч) выдержкой при температуре 150 - 170 0С. В этих условиях вырастают кристаллы нерастворимого в воде соединения Na2O*Al2O3* 2SiO2* 2 H2O (иногда к раствору добавляют известь, в этом случае образуются кристаллы CaO* Al2O3* 2 SiO2*2H2O). Из автоклавов выходит пульпа, состоящая из алюминатного раствора и осадка – белого шлама. Далее раствор отделяют от белого шлама путем сгущения, а раствор направляют на карбонизацию.
Назначение операции карбонизации - выделение из раствора гидроокиси алюминия, не загрязненной другими веществами; ее проводят в цилиндрических баках с мешалками, в которых углекислый газ (обычно очищенные печные газы) продувают через раствор. Под действием СО2 алюминатный раствор разлагается, из него выпадает белый осадок - гидрат окиси алюминия, который отделяется от раствора соды фильтрацией:

Оставшийся оборотный раствор соды после добавления в него некоторого количества свежей соды возвращается на подготовку шихты для очередного спекания, а гидрат окиси алюминия прокаливается (кальцинация) в трубчатых вращающихся печах аналогично процессу кальцинации способа Байера.
На практике кальцинацию глинозема осуществляют в трубчатых вращающихся печах, футерованных шамотным кирпичом (рис. 10). Печи для кальцинации имеют наклон 2,5 - 3 % к длине, длину 35 - 110 м, диаметр 3 - 4 м.
| Рис. 10. Схема кальцинации гидроксидаалюминия: 1 - бункер; 2 - шнековый питатель; 3 - трубчатая вращающаяся печь; 4 -трубчатый холодильник; 5 - камерный насос; 6 - батарейные циклоны; 7- электрофильтр |

Скорость вращения печи 1 - 2 об / мин. Охлаждение прокаленного глинозема проводят в орошаемых водой трубчатых холодильниках длиной 25 - 50 м, диаметром 2,3 - 3,5 со скоростью вращения 2 - 3 об / мин. Холодильник по своей конструкции аналогичен трубчатым вращающимся печам. Отличие заключается в отсутствии футеровки на нижнему разгрузочном конце барабана.
3.4.3.3. Электролитическое производство алюминия
Получить алюминий из водного раствора, как это, например, делается для меди и некоторых других металлов, методом электролиза невозможно, ввиду того что алюминий имеет более отрицательный потенциал выделения, чем водород.
Алюминий получают путем электролитического разложения глинозема, растворенного в расплавленном электролите (криолите – Na3AlF6).
Расплавленный криолит диссоциирует по следующей схеме:
Na3AlF6 ↔ 3 Na+ + AlF3-6
Глинозем, растворенный в расплавленном криолите, диссоциирует на алюминий и кислородсодержащие ионы. Диссоциацию глинозема можно представить в виде следующей схемы:
Al2 O3 ↔ 2 Al 3+ + 3 O2-
Если через расплавленный электролит пропустить постоянный ток, то на различных полюсах электроподводящих электродов будет происходит: выделение алюминия - на отрицательном электроде (катоде), кислорода – на положительном электроде (аноде).
На катоде в первую очередь разряжаются ионы А13 +, так как в электролите нет других более электроположительных ионов (а ионы натрия имеют более отрицательный потенциал).
Процесс электролиза проводят в электролизере, рис. 11.
Электролизер состоит из стального корпуса, футерованного внутри угольными блоками 9, в подовую часть которого с помощью шин 7 и токоподводящих стержней подведен отрицательный полюс источника тока.
Для того чтобы защитить токоподводящие стержни от разрушения на подину укладывают угольные блоки 9.
Над корпусом подвешены угольные аноды 3, к которым с помощью шин 2 подведен положительный полюс. Если в электролизер залить расплав 10, состоящий из криолита и глинозема, опустить в этот расплав аноды и пропускать через расплав постоянный ток большой силы и необходимого напряжения, то через определенное время на дне электролизера можно обнаружить расплавленный алюминий 8 под слоем расплавленного электролита 10, состоящего из криолита Na 3AIF6, в котором при температуре, близкой к 1000 °С, обычно растворено 1-10 % глинозема.

Рис. 11. Схема алюминиевого электролизера с верхним подводом тока к самообжигающемуся аноду:
1 - токоподводящие стержни; 2 - анодные шины; 3 - анодный угольный блок; 4 - газоотсосная система; 5 - слой глинозема;6 - гарнисаж; 7 - катодные шины; 8 - жидкий алюминий у катода; 9 - угольный катод; 10 - жидкий электролит; 11 - чугунный сборник анодных газов; 12 - твердожидкая анодная масса
Процесс электролиза сводится к разряду ионов Al3 + + О2 -, из которых состоит непрерывно расходуемый глинозем. Криолит не подвергается непосредственному электролизу и расходуется мало.
В результате чего на дне ванны образуется слой металлического алюминия 8. На аноде 3 преимущественно разряжаются ионы кислорода, который немедленно окисляет угольный анод, образуя СО и СО2.
Для того чтобы не происходило разрушение боковых графитовых блоков футеровки производят наращивание гарниссажа 6 из застывшего электролита и глинозема.
Электролит поддерживается в расплавленном состоянии только за счет теплоты, выделяющейся при прохождении через него электрического тока, поэтому часть электролита всегда настывает на холодных стенках и образует твердую застывшую корку, на которую сверху насыпают порошкообразную окись алюминия 5.
Алюминий извлекают из электролизера, пробивая корку электролита и опуская на дно футерованную огнеупором стальную трубку, через которую алюминий откачивают в вакуумный ковш.
По мере извлечения алюминия постепенно опускают анод и тщательно регулируют напряжение и межполюсное расстояние электролизера. Поскольку нижняя часть анода сгорает и он постепенно опускается, его необходимо наращивать в верхней части. В кожух анода систематически загружают анодную массу, которая постепенно коксуется на горячем конусе анода за счет теплоты, выделяющейся из ванны. Токоподводящие стальные штыри постепенно опускаются с анодом и во избежание их расплавления и загрязнения алюминия железом в очередной последовательности они выдергиваются из тела анода и поднимаются на более высокий уровень, а в образовавшуюся полость затекает анодная масса и затем коксуется.
3.5. Металлургия магния
3.5.1 Общие сведения о магнии
Магний - серебристо-белый металл. Важнейшее его физическое свойство
Дата добавления: 2015-09-02; просмотров: 123 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Магниетермическое получение титана из тетрахлорида титана | | | Запорожский алюминиевый комбинат (г.Запорожье) |