
|
Читайте также: |
Якщо робочому тілу (газу) надати кількість тепла  , відбувається зміна його внутрішньої енергії на величину
, відбувається зміна його внутрішньої енергії на величину  , і газ виконує елементарну роботу
, і газ виконує елементарну роботу  , причому виконується рівність, яка є наслідком закону збереження енергії:
, причому виконується рівність, яка є наслідком закону збереження енергії:
 . (18)
. (18)
Елементарна робота визначена формулою (13), а зміна внутрішньої енергії для ідеального газу є повним диференціалом:
 . (19)
. (19)
( – зміна температури). Звернемо увагу: зміна внутрішньої енергії визначається виключно параметрами початкового та кінцевого стану газів; значення роботи, яка виконана газом при переході із стану 1 до стану 2, залежить від ходу кривої p(T), тобто від характеру термодинамічного процесу.
– зміна температури). Звернемо увагу: зміна внутрішньої енергії визначається виключно параметрами початкового та кінцевого стану газів; значення роботи, яка виконана газом при переході із стану 1 до стану 2, залежить від ходу кривої p(T), тобто від характеру термодинамічного процесу.
В інтегральному вигляді перший закон термодинаміки можна представити для відомих ізопроцесів: кількість тепла, передана газу при переході із стану 1 до стану 2, визначається таким чином:
Ізобарний процес
(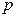 =const) =const)
|  = =  + + 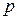 ∙( ∙(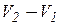 ) )
| (20) |
Ізотермічний процес
(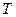 =const) =const)
|

| (21) |
Ізохорний процес
(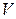 =const) =const)
|  = = 
| (22) |
Теплоємністю тіла у даному термодинамічному процесі називають кількість тепла, яку необхідно надати тілу для збільшення його температури на 1 К
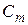 =
=  . (23)
. (23)
Для газів вводять молярні теплоємності (для одного молю, тобто ν =1 моль)
При  =const =const
| 
| (24) |
При 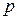 =const =const
| 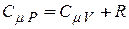 = = 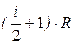
| (25) |
При  =const =const 
| 
| (26) |
Внутрішня енергія довільної кількості газу (енергія теплового руху молекул) таким чином може бути записана з використанням молярної теплоємності при сталому об’ємі:
 =
= 

 . (27)
. (27)
Підкреслимо, що молярна теплоємність визначається виключно числом ступенів свободи молекули газу.
Питома теплоємність газу 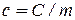 (для одного кг, тобто m = 1 кг) зв’язана з молярною теплоємністю
(для одного кг, тобто m = 1 кг) зв’язана з молярною теплоємністю  співвідношенням
співвідношенням
 =
=  . (28)
. (28)
Дата добавления: 2015-07-12; просмотров: 102 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Елементи термодинаміки. | | | Адіабатний процес. |